Образование углерода из ацетилена по Штеллингу, Фрей- зи, Андерсону
Ф. С. Штеллинг, И. Д. Фрейзи и Р. С. Андерсон исследовали образование углерода в пламени разложения ацетилена, где возможно протекание чрезвычайно разнообразных реакций. Одна из таких реакций, например, – полимеризация ацетилена:
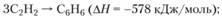
другая – образование свободных радикалов с ароматической структурой:
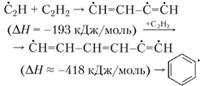
Выделяющаяся при горении энергия достаточна для протекания реакций
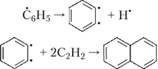
Образование зародышей углерода может происходить в реакциях свободных радикалов с непредельными соединениями с нормальной цепью:
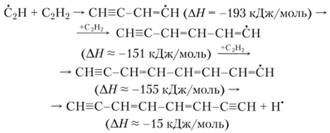
Эти реакции, по мнению данных авторов, возможны, хотя вряд ли они протекают через обычные устойчивые продукты.
Имеющиеся данные по структурам ацетилена и бутадиена показывают, что эти реакции вполне возможны. В ходе этих реакций может отщепляться молекулярный водород Н2, но образование свободных радикалов представляется более вероятным, о чем говорит сравнение тепловых эффектов
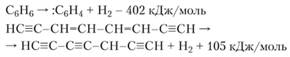
с реакцией
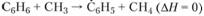
В реакциях образования углерода могут участвовать О, Н и другие активные атомы и радикалы. Если концентрации и температуры таковы, что довольно легко происходит отщепление водорода, реакции могут привести к образованию таких структур, как октатриен, который далее способен давать полирадикал:
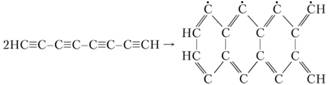
Активные частицы с четырьмя и шестью атомами углерода также могут участвовать в таких реакциях. Очевидно, реакция пойдет по пути теплового взрыва, образуя пластинки соединений с конденсированной кольцевой структурой, установленной для частиц углерода, образующихся из газов.
Реакции полимеризации и реакции свободных радикалов в пламенах ароматических и ненасыщенных соединений с прямой цепью также приводят к образованию разнообразных продуктов, аналогичных продуктам в пламени разложения ацетилена. Как правило, низкие температуры и присутствие разбавителей благоприятствуют простой полимеризации, протекающей вплоть до образования жидких углеводородов. Высокие температуры и концентрации, наличие источников свободных радикалов должны способствовать реакциям образования свободных радикалов и отщепления водорода, которые приводят к образованию твердого углерода.
А. Д. Кокурин (1967) считает, что механизм образования углерода существенно изменяется при возрастании температуры и изменении скорости прогрева. При сравнительно невысоких температурах (до 1000-1100°С) и небольших скоростях прогрева углерод образуется в основном через полициклические и ароматические углеводороды. При более высоких температурах углерод образуется в основном через ацетилен. Превращение бензола при этом происходит с разрывом кольца и образованием радикалов •С2Η, С2 и ацетилена.
Образование углерода по Хоманну и Вагнеру
К. Н. Хоманн и Н. Вагнер[1] исследовали аспекты образования углерода в пламенах ацетилен- и бензол-кислородных смесей. Ацетилен был выбран как модельное вещество для алифатических топлив; в них он всегда образуется до образования твердого углерода. Образование углерода в ацетилен-кислородном пламени происходит на некотором расстоянии от зоны окисления. Хотя ацетилен и полиацетиленовые углеводороды составляют значительную часть углеводородов в горящем газе, они не единственны. Много других веществ с молекулярной массой, большей чем у полиацетиленовых углеводородов, и достаточно низким давлением паров конденсируются вместе с ними или адсорбируются на частицах углерода, когда происходит отбор проб посредством охлаждаемого капилляра. В зоне пламени, где присутствует углерод, обнаружены полициклические ароматические углеводороды, такие как С14П8, и другие углеводороды с молекулярной массой, превышающей 200.
В области максимального образования углерода отношение числа атомов водорода к числу атомов углерода в конденсированных продуктах (Н/С) составляет 0,33-0,25 (соответствует элементарному составу между С6Н2 и С8Н2), понижаясь далее по потоку в несколько раз. К. II. Хоманн н Н. Вагнер отмечают, что, если отбор пробы не происходит в условиях высокого вакуума, отношение числа атомов Н/С значительно выше, вплоть до единицы, благодаря одновременной конденсации или адсорбции углеводородов с достаточно низким давлением паров.
В противоположность ацетиленовому пламени в бензольном пламени образование углерода начинается уже в зоне окисления (если границу этой зоны определять такой высотой пламени, где исчезает молекулярный кислород), скорость образования углерода выше, и процессы заканчиваются раньше. В обоих пламенах, тем не менее, образование углерода имеет место в относительно узкой зоне пламени, которая в бензол-кислородном пламени перекрывается частично с зоной окисления.
В пламенах бензола образуются как полиацетиленовые углеводороды (и, конечно, ацетилен), так и полициклические ароматические углеводороды. Концентрация последних примерно в 100 раз выше, чем в пламенах алифатических соединений с тем же отношением углерода к кислороду в несгоревшем газе. Максимум их концентрации лежит в пределах зоны окисления и понижается к концу ее, где образуется большая часть углерода.
Как и в случае пламени ацетилена, масс-спектроскопические анализы образцов сажи и газа, взятых прямо из бензольного пламени, показали, что углеводороды с молекулярной массой больше 250 существуют в области начата образования углерода и исчезают вдоль по потоку в горящем газе, тогда как углеводороды с меньшей молекулярной массой некоторое время еще сохраняются вдоль потока.
Экспериментальные данные[2] исследований образования углерода показали, что в пламенах как ароматических, так и алифатических углеводородов существуют три главные группы продуктов, которые принимают участие в процессе образования углерода. Ими являются: 1) ацетилен и полиацетиленовые углеводороды с молекулярной массой от 20 до 146; 2) полициклические ароматические углеводороды с молекулярной массой от 78 до 300; 3) реакционноспособные полициклические углеводороды, возможно, с боковыми цепями, содержащие больше водорода, чем ароматические (молекулярная масса от 150 до 550). Относительные количества этих групп, так же как количество образованного углерода, различно в ацетиленовых и бензольных пламенах.
На основании результатов исследования концентрационных профилей углеводородов, скорости образования и роста частиц углерода К. Н. Хоманн и Н. Вагнер (1965) предложили следующую схему образования углерода в ацетиленовом пламени (рис. 1.21). Важными в этой схеме являются реакции радикалов. Максимальная концентрация радикалов наблюдается внутри зоны окисления. По-видимому, скорость образования углерода сильно зависит от количества подходящих углеводородных радикалов.
Изучение пиролиза ацетилена в проточной системе показывает, что скорость образования тяжелых углеводородов в этих условиях много меньше, чем в пламени, из-за низкой концентрации радикалов (по сравнению с концентрацией в реакционной зоне пламени). Образование поли- ацетиленовых углеводородов может быть объяснено только радикальными реакциями, схема которых представлена на рис. 1.21.
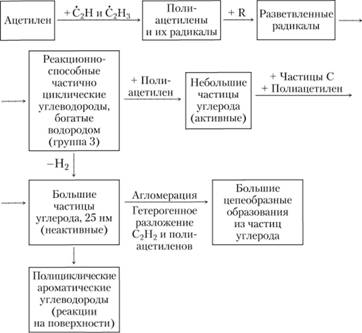
Рис. 1.21. Схема образования полиацетиленовых углеводородов
Большая часть полиацетиленовых углеводородов образуется внутри зоны окисления. Винилацетилен H2С=СН–СºСН образуется в пламени при низких температурах, но исчезает в зоне окисления. Очень реакционноспособные углеводороды третьей группы имеют радикальный характер, присоединяют полиацетилены и, возможно, становятся небольшими частицами (ядрами) углерода. Преобладающее присоединение полиацетилена па последней стадии роста частиц подтверждается тем фактом, что ОГЛАВЛЕНИЕ водорода в саже понижается, в то время как частицы сажи продолжают расти. Кроме того, эти реакционноспособные промежуточные углеводороды могут образовать полициклические ароматические углеводороды вследствие молекулярных перегруппировок или расщепления части своих молекул, в которых ароматическая структура уже предварительно образована.
В противоположность ацетиленовым пламенам, в которых образование углерода начинается тогда, когда отношение числа атомов С/О в несгоревшем газе равно -0,95, бензол-кислородные пламена образуют углерод уже при отношении С/О, равном 0,75. Это означает, что при тех же отношениях С/О в несгоревшем газе бензольные пламена дают значительно больше углерода, чем ацетиленовые пламена.
В зоне окисления ацетиленовых пламен ненасыщенные углеводороды представлены главным образом С2Н2 и С4Н2 и частично полиацстилснами. В реакционной зоне бензольных пламен основными непредельными продуктами являются углеводороды С6Н6 (бензол) и полициклические ароматические углеводороды, полиацетилены также присутствуют здесь, по не играют столь важной роли, как в ацетиленовых пламенах. Полициклические ароматические углеводороды образуются в зоне окисления (в отличие от ацетиленовых пламен). Их профили концентраций проходят через максимум и понижаются в зоне образования углерода. В образовании полициклических ароматических углеводородов бензол, по-видимому, играет более важную роль, чем углеводороды третьей группы (в пламени ацетилена, где концентрация бензола небольшая, – наоборот).
Поскольку полициклические ароматические углеводороды содержат в среднем больше углерода, чем поли ацетилены, образованные из них радикалы оказываются более эффективными "строительными кусками". В бензольных пламенах полициклические ароматические углеводороды присоединяются вместе с другими углеводородами к любому углеводородному радикалу, образуя небольшие частицы сажи.
Область образования углерода в бензольных пламенах сильно перекрывается с зоной окисления. Поэтому в этих пламенах для образования углерода имеется больше углеводородных радикалов, чем в ацетиленовых пламенах. Более эффективные углеводородные "строительные куски" сажи в бензольных пламенах находятся в зоне максимальной концентрации углеводородных радикалов. Поэтому количество углерода в бензольных пламенах больше, чем в пламенах ацетилена.
К. Н. Хоманн и Н. Вагнер рассматривают полициклические ароматические углеводороды в ацетиленовых пламенах в большей мере побочными продуктами и в меньшей мере промежуточными частицами для ядер углерода. В бензольных пламенах, по их мнению, как полиацетилены, так и полициклические ароматические углеводороды, которые всегда имеются в сравнительно высокой концентрации в зоне окисления, могут быть присоединены к радикалам любого размера, среди которых фенильный радикал, возможно, играет главную роль.