Глава 5. Три этапа в развитии термодинамики
Поток и сила.Приращение энтропии допускает разложение в сумму двух членов: члена deS, связанного с обменом между системой и остальным миром, и члена diS, описывающего производство энтропии вследствие необратимых процессов внутри системы. Второй член всегда положителен, за исключением термодинамического равновесия, когда он обращается в нуль. Для изолированной системы (deS = 0) состояние равновесия соответствует состоянию с максимумом энтропии.
Могут ли химические процессы дать нам ключ к постижению различия между поведением кристалла и клетки? Нельзя не отметить принципиальное концептуальное различие между физикой и химией. В классической физике мы можем, по крайней мере, представлять себе обратимые процессы, такие, как движение маятника без трения. Пренебрежение необратимыми процессами в динамике всегда соответствует идеализации, но, по крайней мере, в некоторых случаях эта идеализация разумна. В химии все обстоит совершенно иначе. Процессы, изучением которых она занимается (химические превращения, характеризуемые скоростями реакций), необратимы. По этой причине химию невозможно свести к лежащей в основе классической или квантовой механики идеализации, в которой прошлое и будущее играют эквивалентные роли.
Линейная термодинамика.Линейная термодинамика описывает стабильное, предсказуемое поведение систем, стремящихся к минимальному уровню активности, совместимому с питающими их потеками. Из того, что линейная неравновесная термодинамика так же, как и равновесная термодинамика, допускает описание с помощью потенциала, а именно производства энтропии, следует, что и при эволюции к равновесию, и при эволюции к стационарному состоянию система «забывает» начальные условия. Каковы бы ни были начальные условия, система рано или поздно перейдет в состояние, определяемое граничными условиями.
Вдали от равновесия.До тех пор пока состояние-аттрактор определяется минимумом потенциала (например, производство энтропии), его устойчивость гарантирована. Правда, флуктуация может вывести систему из этого минимума. Но тогда второе начало термодинамики вынудит систему вернуться в исходный минимум. Таким образом, существование термодинамического потенциала делает систему «невосприимчивой» к флуктуациям. Располагая потенциалом, мы описываем «стабильный мир», в котором системы, эволюционируя, переходят в статичное состояние, установленное для них раз и навсегда. Но когда термодинамические силы, действуя на систему, становятся достаточно «большими» и вынуждают ее покинуть линейную область, гарантировать устойчивость стационарного состояния или его независимость от флуктуации было бы опрометчиво.
В таких состояниях определенные флуктуации вместо того, чтобы затухать, усиливаются и завладевают всей системой, вынуждая ее эволюционировать к новому режиму, который может быть качественно отличным от стационарных состояний, соответствующих минимуму производства энтропии. Такого рода явления хорошо известны в гидродинамике — теории течений. Например, давно известно, что при определенной скорости ламинарное течение может смениться турбулентным.
Долгое время турбулентность отождествлялась с хаосом или шумом. Сегодня мы знаем, что это не так. Хотя в макроскопическом масштабе турбулентное течение кажется совершенно беспорядочным, или хаотическим, в микроскопическом масштабе оно высокоорганизованно. Множество пространственных и временных масштабов, на которых разыгрывается турбулентность, соответствует когерентному поведению миллионов и миллионов молекул. С этой точки зрения переход от ламинарного течения к турбулентности является процессом самоорганизации. Принцип порядка Больцмана устанавливает связь энтропии с вероятностью (числом комплексов Р). Применимо ли это соотношение в данном случае? Когерентное движение означает, что многие молекулы движутся почти с одинаковыми скоростями (разброс скоростей мал). Такому распределению соответствует столь малое число комплексов Р, что вероятность возникновения самоорганизации почти равна нулю. В сильно неравновесных условиях понятие вероятности, лежащее в основе больцмановского принципа порядка, становится неприменимым: наблюдаемые структуры не соответствуют максимуму комплексов. Тенденция к выравниванию и «забыванию» начальных условий перестает быть общей тенденцией.
Мы ввели новое понятие — диссипативная структура, чтобы подчеркнуть тесную и на первый взгляд парадоксальную взаимосвязь, существующую в таких ситуациях, с одной стороны, между структурой и порядком, а с другой — между диссипацией, или потерями.
За порогом химической неустойчивости.Еще раз подчеркнем, как сильно спонтанное образование пространственных структур противоречит законам равновесной физики и принципу порядка Больцмана. Число комплексов, соответствующих таким структурам, чрезвычайно мало по сравнению с числом комплексов, отвечающих равномерному распределению. Но неравновесные процессы могут приводить к ситуациям, кажущимся немыслимыми с классической точки зрения.
Первое знакомство с молекулярной биологией.Образование колоний коллективных амеб — типичный пример того, что можно было бы назвать «порядком через флуктуации»: возникновение «центра притяжения», испускающего циклическую АМФ,[5] сигнализирует о потере устойчивости нормальной питательной среды, т.е. об исчерпании запаса питательных веществ. То, что при нехватке пищевого ресурса любая амеба может начать испускание химических сигналов — циклической АМФ — и, таким образом, стать «центром притяжения» для остальных амеб, соответствует случайному характеру флуктуации. В данном случае флуктуация усиливается и организует среду.
Бифуркации и нарушение симметрии.Рассмотрим более подробно, как возникает самоорганизация и какие процессы начинают происходить, когда ее порог оказывается превзойденным. В равновесном или слабо неравновесном состоянии существует только одно стационарное состояние, зависящее от значений управляющих параметров. Обозначим управляющий параметр через λ (им может быть, например, концентрация вещества В в брюсселяторе.[6] Проследим за тем, как изменяется состояние системы с возрастанием значения В. Увеличивая концентрацию В, мы как бы уводим систему все дальше и дальше от равновесия. При некотором значении В мы достигаем порога устойчивости термодинамической ветви. Обычно это критическое значение называется точкой бифуркации.
Рассмотрим некоторые типичные бифуркационные диаграммы. В точке бифуркации В термодинамическая ветвь становится неустойчивой относительно флуктуации (рис. 1). При критическом значении λС управляющего параметра λ система может находиться в трех различных стационарных состояниях: С, Е и D. Два из них устойчивы, третье неустойчиво. Очень важно подчеркнуть, что поведение таких систем зависит от их предыстории. Начав с малых значений управляющего параметра λ и медленно увеличивая их, мы с большой вероятностью опишем траекторию ABC. Наоборот, начав с больших значений концентрации Х и поддерживая постоянным значение управляющего параметра λ, мы с высокой вероятностью придем в точку D. Таким образом, конечное состояние зависит от предыстории системы. До сих пор история использовалась при интерпретации биологических и социальных явлений. Совершенно неожиданно выяснилось, что предыстория может играть роль и в простых химических процессах.
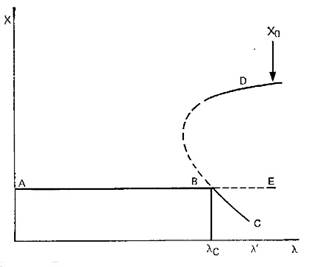
Рис. 1. Бифуркационная диаграмма. Стационарные значения переменной X представлены на диаграмме как функции параметра бифуркации λ. Сплошные линии соответствуют устойчивым, штриховые — неустойчивым стационарным состояниям. Чтобы достичь ветви D, необходимо выбрать начальную концентрацию Х0 выше значений Х, соответствующую ветви Е.
Рассмотрим бифуркационную диаграмму, изображенную на рис. 2. От предыдущей диаграммы она отличается тем, что в точке бифуркации появляются два устойчивых решения. В связи с этим, естественно, возникает вопрос: по какому пути пойдет дальнейшее развитие системы после того, как мы достигнем точки бифуркации? У системы имеется «выбор»: она может отдать предпочтение одной из двух возможностей, соответствующих двум неравномерным распределениям концентрации X в пространстве.

Рис. 2. Симметричная бифуркационная диаграмма. X как функция параметра бифуркации λ. При λ < λС существует только одно стационарное состояние, которое устойчиво. При λ > λС существуют два стационарных состояния при любом значении X (прежнее устойчивое стационарное состояние теряет устойчивость).
Каскады бифуркаций и переходы к хаосу.В некоторых случаях последовательность бифуркаций приводит к необратимой эволюции и детерминированность характеристических частот порождает все большую случайность, обусловленную огромным числом частот, участвующих в процессе. Сравнительно недавно внимание ученых привлек необычайно простой путь к хаосу, получивший название последовательность Фейгенбаума. Обнаруженная Фейгенбаумом закономерность относится к любой системе, поведение которой характеризуется весьма общим свойством, а именно: в определенной области значений параметров система действует в периодическом режиме с периодом Т; при переходе через порог период удваивается и становится равным 2Т, при переходе через следующий порог период в очередной раз удваивается и становится равным 4Т и т.д. Таким образом, система характеризуется последовательностью бифуркаций удвоения периода. Последовательность Фейгенбаума — один из типичных маршрутов, ведущих от простого периодического режима к сложному апериодическому, наступающему в пределе при бесконечном удвоении периода. Фейгенбаум открыл, что этот маршрут характеризуется универсальными постоянными, значения которых не зависят от конкретных особенностей механизма, коль скоро система обладает качественным свойством удвоения периода. (Подробнее о работе Фейгенбаума см. Джеймс Глейк. Хаос. Создание новой науки.)
При значении управляющего параметра порядка λС система может находиться в большом числе устойчивых и неустойчивых режимов, «историческая» траектория, по которой эволюционирует система при увеличении управляющего параметра характеризуется чередованием устойчивых областей, где доминируют детерминистические законы, и неустойчивых областей вблизи точек бифуркации, где перед системой открывается возможность выбора одного из нескольких вариантов будущего. И детерминистический характер кинетических уравнений, позволяющих вычислить заранее набор возможных состояний и определить их относительную устойчивость, и случайные флуктуации, «выбирающие» одно из нескольких возможных состояний вблизи точки бифуркации, теснейшим образом взаимосвязаны. Эта смесь необходимости и случайности и составляет «историю» системы.
От Евклида к Аристотелю. Одной из наиболее интересных особенностей диссипативных структур является их когерентность. Система ведет себя как единое целое и как если бы она была вместилищем дальнодействующих сил. Несмотря на то что силы молекулярного взаимодействия являются короткодействующими (действуют на расстояниях порядка 10–8 см), система структурируется так, как если бы каждая молекула была «информирована» о состоянии системы в целом. Жизнь — результат спонтанной самоорганизации, происходящей при благоприятных условиях.
Сильно неравновесная система может быть названа организованной не потому, что в ней реализуется план, чуждый активности на элементарном уровне или выходящий за рамки первичных проявлений активности, а по противоположной причине: усиление микроскопической флуктуации, происшедшей в «нужный момент», приводит к преимущественному выбору одного пути реакции из ряда априори одинаково возможных. Следовательно, при определенных условиях роль того или иного индивидуального режима становится решающей. Обобщая, можно утверждать, что поведение «в среднем» не может доминировать над составляющими его элементарными процессами. В сильно неравновесных условиях процессы самоорганизации соответствуют тонкому взаимодействию между случайностью и необходимостью, флуктуациями и детерминистическими законами. Мы считаем, что вблизи бифуркаций основную роль играют флуктуации или случайные элементы, тогда как в интервалах между бифуркациями доминируют детерминистические аспекты.