Структура воды: новые экспериментальные данные
Воде дана таинственная власть
Быть соком жизни на Земле.
Леонардо да Винчи
Структура воды: новые экспериментальные данные
Кандидат химических наук Александр Смирнов, профессор МИРЭА.
Воду принято рассматривать и как практически нейтральный растворитель, в котором протекают биохимические реакции, и как субстанцию, разносящую по телу живых организмов различные вещества. Вместе с тем вода — непременный участник всех физико-химических процессов и, в силу своей огромной важности, самое изучаемое вещество. Изучение свойств воды не раз приводило к неожиданным результатам. Казалось бы, какие неожиданности может таить в себе несложная реакция окисления водорода 2H2 + O2 2H2O? Но работы академика Н. Н. Семёнова показали, что реакция эта — разветвлённая, цепная. Было это более семидесяти лет назад, и про цепную реакцию деления урана ещё не знали. Вода в стакане, реке или озере не просто огромные количества отдельных молекул, а их объединения, надмолекулярные структуры — кластеры. Для описания структуры воды предложен ряд моделей, которые более или менее правильно объясняют только некоторые её свойства, а в отношении других противоречат эксперименту.
Теоретически кластеры рассчитывают обычно только для нескольких сотен молекул или для слоёв вблизи межфазной границы. Однако ряд экспериментальных фактов свидетельствует, что в воде могут существовать гигантские, по молекулярным масштабам, структуры (работы члена-корреспондента РАН Е. Е. Фесенко).
В тщательно очищенной дважды дистиллированной воде и некоторых растворах нам удалось методом акустической эмиссии обнаружить и с помощью лазерной интерферометрии визуализировать структурные образования, состоящие из пяти фракций размерами от 1 до 100 мкм. Эксперименты позволили установить, что каждый раствор имеет свою, присущую только ему структуру (рис. 1, 2).
Надмолекулярные комплексы образованы сотнями тысяч молекул воды, сгруппированных вокруг ионов водорода и гидроксила в виде ионных пар. Для этих надмолекулярных комплексов мы предлагаем название «эмулоны», чтобы подчеркнуть их сходство с частицами, образующими эмульсию. Комплексы состоят из отдельных фракций размерами от 1 до 100 мкм, причём фракций, имеющих размеры 30, 70 и 100 мкм, значительно больше остальных.
Содержание отдельных фракций эмулонов зависит от концентрации ионов водорода, температуры, концентрации раствора и предыстории образца (рис.3). В бидистиллированной воде при 4оС комплексы плотно упакованы и образуют текстуру, напоминающую паркет. Как известно, вода при этой температуре имеет максимальную плотность. При повышении температуры до 20оС в структуре воды происходят существенные изменения: количество свободных эмулонов становится наибольшим. При дальнейшем нагреве они постепенно разрушаются, число их уменьшается, и этот процесс в основном заканчивается при 75оС, когда скорость звука в воде достигает максимума.

Рис. 1. Структура воды при температуре 20 0 С, размер по горизонтали — 400 мкм. Белые пятна — это эмулоны.<br><br>

Рис. 2. Структура водных растворов при 20 0 С: А — дистиллированная вода; Б — дегазированная минеральная вода боржоми; В — спиртовая настойка 70%.
Содержание отдельных фракций эмулонов зависит от концентрации ионов водорода, температуры, концентрации раствора и предыстории образца (рис. 3).

Рис. 3. Эмулоны в бидистиллированной воде при температурах 40С (А), 200 С (Б), 80 0С (В). Размеры снимков 1,5 Х 1,5 мм
В бидистиллированной воде при 4оС комплексы плотно упакованы и образуют текстуру, напоминающую паркет. Как известно, вода при этой температуре имеет максимальную плотность. При повышении температуры до 20оС в структуре воды происходят существенные изменения: количество свободных эмулонов становится наибольшим. При дальнейшем нагреве они постепенно разрушаются, число их уменьшается, и этот процесс в основном заканчивается при 75оС, когда скорость звука в воде достигает максимума.
За счёт дальнодействия электростатических сил эмулоны в воде образуют довольно стабильную сверхрешётку, которая, однако, чутко реагирует на электромагнитные, акустические, тепловые и другие внешние воздействия.
Обнаруженные надмолекулярные комплексы непротиворечиво включают в себя все ранее полученные сведения об организации воды в нанообъёмах и позволяют объяснить многие экспериментальные факты, которые не имели стройного, логичного обоснования. К ним относится, например, образование «парящего водяного мостика», описанного в ряде работ.
Суть эксперимента заключается в том, что если поставить рядом два небольших химических стакана с водой, опустить в них платиновые электроды под постоянным напряжением 15—30 кВ, то между сосудами образуется водяная перемычка диаметром 3 мм и длиной до 25 мм. «Мостик» парит длительное время, имеет слоистую структуру, и по нему происходит перенос воды от анода к катоду. Этот феномен и все его свойства — следствие наличия в воде эмулонов, которые, по-видимому, обладают дипольным моментом. Можно предсказать и ещё одно свойство явления: при температуре воды выше 75оС «мостик» не возникнет.
Легко объясняются и аномальные свойства талой воды. Как отмечалось в литературе, многие свойства талой воды — плотность, вязкость, электропроводность, показатель преломления, растворяющая способность и другие — отличаются от равновесных параметров. Сведéние этих эффектов к удалению из воды дейтерия в результате фазового перехода (температура плавления «тяжёлого льда» D2O 3,82оС) несостоятельно, поскольку концентрация дейтерия крайне незначительна — один атом дейтерия на 5—7 тыс. атомов водорода.
Изучение плавления льда методом акустической эмиссии позволило впервые установить, что после полного расплавления льда талая вода, находящаяся в метастабильном состоянии, становится источником акустических импульсов, что служит экспериментальным подтверждением образования в воде надмолекулярных комплексов (рис. 4).
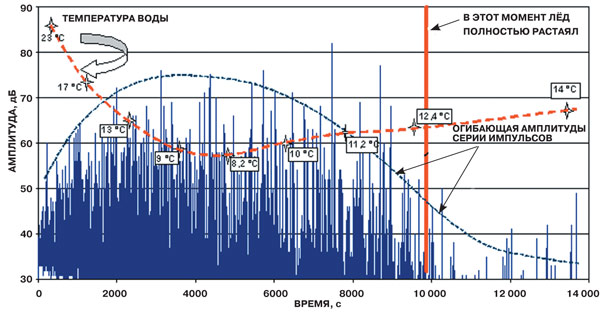
Рис. 4. Изменение амплитуды сигналов акустической эмиссии и температуры воды в процессе таяния льда
Эксперименты показывают, что талая вода на протяжении почти 17 часов может находиться в активном метастабильном состоянии (после плавления льда его микрокристаллики сохраняются только доли секунды и совсем не определяют свойства талой воды). Это загадочное явление объясняется тем, что при разрушении гексагональной кристаллической решётки льда резко меняется структура вещества. Кристаллы льда разрушаются быстрее, чем перестраивается в устойчивое равновесное состояние образовавшаяся из него вода.
Уникальность фазового перехода лёдвода заключается в том, что в талой воде концентрация ионов водорода H+ и гидроксила OH– непродолжительное время сохраняется неравновесной, какой она была во льду, то есть в тысячу раз меньшей, чем в обычной воде. Через некоторое время концентрация ионов H+ и OH– в воде принимает своё равновесное значение. Поскольку ионы водорода и гидроксила играют решающую роль в формировании надмолекулярных комплексов воды (эмулонов), вода на некоторое время остаётся в метастабильном состоянии. Реакция её диссоциации H2O H+ + OH– требует значительной затраты энергии и протекает очень медленно. Константа скорости этой реакции составляет всего 2,510–5 c–1 при 20оС. Поэтому время возвращения талой воды в равновесное состояние теоретически должно составлять 10—17 часов, что и наблюдается на практике. Исследования динамики изменения концентрации ионов водорода в талой воде во времени подтверждают это. Необычные свойства талой воды служат причиной разговоров о «памяти» воды. Но под «памятью» воды следует понимать зависимость её свойств от предыстории и ничего больше. Можно разными способами — замораживанием, нагреванием, кипячением, обработкой ультразвуком, воздействием различных полей и др. — перевести воду в метастабильное состояние, но оно будет неустойчивым, недолго сохраняющим свои свойства. Оптическим методом мы обнаружили в талой воде присутствие лишь одной фракции надмолекулярных образований с размерами 1—3 мкм. Возможно, что пониженная вязкость и более редкая пространственная сетка из эмулонов в талой воде увеличивают растворяющую способность и скорость диффузии.
Реальность существования эмулонов подтверждает классический метод термического анализа (рис.5).
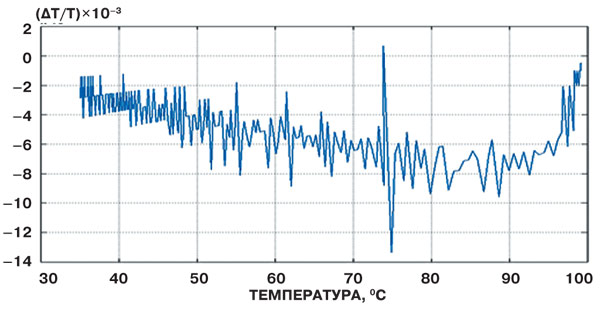
На графике наблюдаются чётко выраженные пики, свидетельствующие о структурных перестройках в воде. Наиболее значимые соответствуют 36оC — температуре минимальной теплоёмкости, 63оC — температуре минимальной сжимаемости, и особенно характерен пик при 75оC — температуре максимальной скорости звука в воде. Их можно трактовать как своеобразные фазовые переходы, связанные с разрушением эмулонов. Это позволяет сделать вывод: жидкая вода — очень своеобразная дисперсная система, включающая как минимум пять структурных образований с различными свойствами. Каждая структура существует в определённом, характерном для неё температурном интервале. Превышение температуры над пороговым уровнем, критичным для данной структуры приводит к ее распаду.
Литература
Зацепина Г. Л. Физические свойства и структура воды. — М.: Изд-во Московского университета. — 1998. — 185 с.
Кузнецов Д. М., Гапонов В. Л., Смирнов А. Н. О возможности исследования кинетики фазовых переходов в жидкой среде методом акустической эмиссии // Инженерная физика, 2008, № 1, с. 16—20.
Кузнецов Д. М., Смирнов А. Н., Сыроешкин А. В. Акустическая эмиссия при фазовых превращениях в водной среде // Российский химический журнал — М.: Рос. хим. об-во им. Д. И. Менделеева, 2008, т. 52, № 1, с. 114—121.
Смирнов А. Н. Структура воды: новые экспериментальные данные. // Наука и технологии в промышленности, 2010, № 4, с. 41—45.
Смирнов А. Н. Акустическая эмиссия при протекании химической реакции и физико-химических процессов // Российский химический журнал. — М.: Рос. хим. об-во им. Д. И. Менделеева, 2001, т. 45, с. 29—34.
Смирнов А. Н., Сыроешкин А. В. Супранадмолекулярные комплексы воды // Российский химический журнал. — М.: Рос. хим. об-во им. Д. И. Менделеева, 2004, т. 48, № 2, с. 125—135.