СОСТАВ И СВОЙСТВА ПЛАСТОВЫХ ВОД
Природные воды всегда содержат определенное количество примесей и представляют собой сложные многокомпонентные системы. В результате взаимодействия воды с включающими ее породами и газообразными составляющими земной коры часть их переходит в воду, образуя растворы. В природных водах, в том числе в пластовых водах нефтяных и газовых месторождений, могут содержаться следующие компоненты.
1 Вещества, находящиеся в воде в истинно-растворенном состоянии и образующие вследствие электролитической диссоциации ионы. Основными веществами, растворенными в природных водах, являются хлориды, сульфаты и карбонаты щелочных и щелочноземельных металлов. Диссоциируя в воде, соединения образуют ионы Na+, K+ Са2+, Mg2+, Cl-, SО42-, HCО3-, СО32-, называемые главными ионами. Количественные соотношения между этими ионами определяют тип природной воды. Кроме главных ионов, в пластовых водах присутствуют и другие, встречающиеся обычно в малых количествах – NO3-, NH4+ , Вr-, I-, Li+, Fe2+, Fe3+ и др.
В пластовых водах нефтяных и газовых месторождений может содержаться в растворенном состоянии некоторое количество нефтяных фракций, а также щелочных солей нафтеновых кислот.
2 Газообразные вещества, растворенные в воде. В водах нефтяных и газовых месторождений могут встречаться CO2, H2S, CH4, H2, N2 и др.
3 Вещества, находящиеся в воде в коллоидно-растворенном состоянии: SiO2, Fe2O3, Al2O3.
Систематические гидрохимические исследования проводят на нефтяных и газовых месторождениях от начала разведочных работ до полной их выработки, при анализе вод для характеристики их свойств принято проводить:
1 определение общей минерализации воды и ее жесткости;
2 определение содержания главных шести ионов для отнесения исследуемой воды к тому или иному типу;
3 определение концентрации водородных ионов;
4 анализ растворенных в воде газов;
5 определение некоторых физических свойств воды: температуры, плотности, запаха, вкуса, цвета, прозрачности, объемного коэффициента, коэффициента термического расширения, вязкости, поверхностного натяжения.
ОБЩАЯ МИНЕРАЛИЗАЦИЯ ВОДЫ
Минерализация воды – суммарная массовая концентрация растворенных и коллоидных веществ в растворе (пластовой воде).
Наиболее употребительная форма выражения минерализации – число миллиграмм-эквивалентов солей, находящихся в 1 л воды.
Минерализацию воды также выражают в процентах, т.е. сколько грамм растворенных веществ содержится в 100 г раствора.
От степени минерализации пластовая вода подразделяется на 4 типа:
- пресная вода, содержание солей до 1 г/л;
- солоноватая вода, до 10 г/л;
- соленая вода, до 50 г/л;
- рассолы, 50 и более г/л.
Вернадский В.И. в зависимости от массовой доли растворенных солей подразделил природные воды на три класса:
1 пресные воды с содержанием солей 0,001 – 0,1 %;
2 минерализованные воды с содержанием солей 0,1 – 5 %;
3 рассольные воды с содержанием солей 5 – 35 %.
Об общей минерализации воды можно судить по ее плотности. Общую минерализацию воды измеряют плотностью в градусах Боме. При этом способе измерения плотность нуль градусов шкалы Боле соответствует плотности дистиллированной воды; 15 0 – плотности 15 %-ного раствора хлорида натрия.
Для определения плотности воды по величине в градусах Боме (Ве 0) используют формулы:
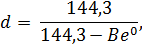
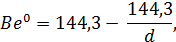
где d – плотность воды, г/мл.