НАНОМАТЕРИАЛЫ И ИХ ОСНОВНЫЕ СВОЙСТВА
НАНОМАТЕРИАЛЫ
Наночастицами принято называть объекты, состоящие из атомов, ионов или молекул и имеющие размер менее 100 нм. Примером могут служить частицы металлов. Известно, что вода, находящаяся в контакте с серебром, способна убивать болезнетворные бактерии. Целебная сила такой воды объясняется содержанием в ней мельчайших частиц серебра, это и есть наночастицы! Благодаря малому размеру эти частицы отличаются по свойствам как от отдельных атомов, так и от объемного материала, состоящего из многих миллиардов миллиардов атомов, например слитка серебра.
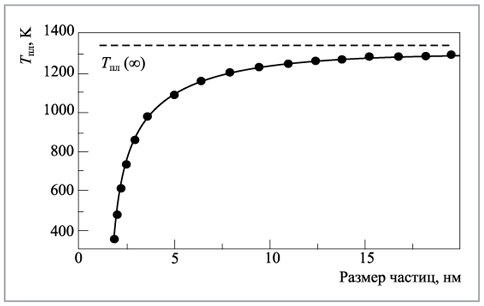
Многие физические свойства вещества, например его окраска, тепло- и электропроводность, температура плавления зависят от размера частиц. Например, температура плавления наночастиц золота размером 5 нм оказывается на 250° ниже, чем у обычного золота (рис. 5.1). По мере увеличения размера наночастиц золота температура плавления возрастает и достигает значения 1337 К, характерного для обычного материала .
|
| Рис. 5.1. Зависимость температуры плавления золота от размера частиц.Точками обозначены экспериментальные данные, сплошная кривая рассчитана по уравнению Гиббса–Томсона |
Далее, стекло приобретает окраску, если содержит частицы, размеры которых сопоставимы с длиной волны видимого света, т.е. имеют наноразмер. Именно этим и объясняется яркая окраска средневековых витражей, в составе которых находятся различной величины наночастицы металлов или их оксидов. А электропроводность материала определяется длиной свободного пробега – расстоянием, которое проходит электрон между двумя соударениями с атомами. Оно также измеряется в нанометрах. Если размер наночастицы металла оказывается меньше этого расстояния, то у материала следует ожидать появления особых электрических свойств, не характерных для обычного металла.
Таким образом, нанообъекты характеризуются не только малым размером, но и особыми свойствами, которые они проявляют, выступая как составная часть материала. Например, окраска стекла «золотой рубин» или коллоидного раствора золота вызвана не одной наночастицей золота, а их ансамблем, т.е. большим количеством частиц, расположенных на определенном расстоянии друг от друга.
| Рис.5. 2. Зависимость доли атомовв объеме и на поверхности от размера частиц |
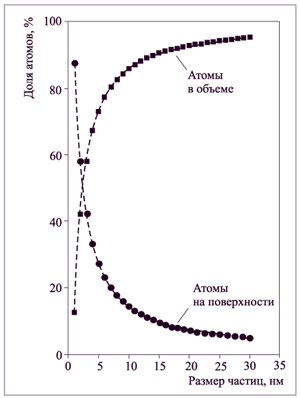 Отдельные наночастицы, содержащие не более 1000 атомов, называют нанокластерами. Свойства таких частиц значительно отличаются от свойств кристалла, в котором содержится огромное число атомов. Это объясняется особой ролью поверхности. Действительно, реакции с участием твердых тел происходят не в объеме, а на поверхности. Примером может служить взаимодействие цинка с соляной кислотой. Если внимательно присмотреться, то можно увидеть, что пузырьки водорода образуются на поверхности цинка, а атомы, находящиеся в глубине, не участвуют в реакции. Лежащие на поверхности атомы обладают большей энергией, т.к. у них меньше соседей в кристаллической решетке. Постепенное уменьшение размера частиц приводит к увеличению общей площади поверхности, росту доли атомов на поверхности (рис. 2) и возрастанию роли поверхностной энергии. Особенно велика она у нанокластеров, где на поверхности находится большинство атомов. Поэтому неудивительно, что, например, нанозолото по химической активности во много раз превосходит обычное. Так, например, наночастицы золота, содержащие 55 атомов (диаметр 1,4 нм), нанесенные на поверхность TiO2, служат хорошими катализаторами селективного окисления стирола кислородом воздуха до бензальдегида (Nature, 2008):
Отдельные наночастицы, содержащие не более 1000 атомов, называют нанокластерами. Свойства таких частиц значительно отличаются от свойств кристалла, в котором содержится огромное число атомов. Это объясняется особой ролью поверхности. Действительно, реакции с участием твердых тел происходят не в объеме, а на поверхности. Примером может служить взаимодействие цинка с соляной кислотой. Если внимательно присмотреться, то можно увидеть, что пузырьки водорода образуются на поверхности цинка, а атомы, находящиеся в глубине, не участвуют в реакции. Лежащие на поверхности атомы обладают большей энергией, т.к. у них меньше соседей в кристаллической решетке. Постепенное уменьшение размера частиц приводит к увеличению общей площади поверхности, росту доли атомов на поверхности (рис. 2) и возрастанию роли поверхностной энергии. Особенно велика она у нанокластеров, где на поверхности находится большинство атомов. Поэтому неудивительно, что, например, нанозолото по химической активности во много раз превосходит обычное. Так, например, наночастицы золота, содержащие 55 атомов (диаметр 1,4 нм), нанесенные на поверхность TiO2, служат хорошими катализаторами селективного окисления стирола кислородом воздуха до бензальдегида (Nature, 2008):
C6H5–CH=CH2 + O2 —> C6H5–CH=O + H2O,
тогда как частицы диаметром более 2 нм, а тем более обычное золото совсем не проявляют каталитической активности.
Алюминий устойчив на воздухе, а наночастицы алюминия мгновенно окисляются кислородом воздуха, превращаясь в оксид Al2O3. Исследования показали, что наночастицы алюминия диаметром 80 нм на воздухе обрастают слоем оксида толщиной от 3 до 5 нм. Другой пример: хорошо известно, что обычное серебро не растворимо в разбавленных кислотах (кроме азотной). Однако совсем маленькие наночастицы серебра (не больше 5 атомов) будут растворяться с выделением водорода даже в слабых кислотах типа уксусной, для этого достаточно создать кислотность раствора pH = 5.
Зависимость физических и химических свойств наночастиц от их размера называют размерным эффектом. Это – один из важнейших эффектов в нанохимии. Он уже нашел теоретическое объяснение с позиций классической науки, а именно – химической термодинамики. Так, зависимость температуры плавления от размера объясняется тем, что атомы внутри наночастиц испытывают дополнительное поверхностное давление, которое изменяет их энергию Гиббса (см. лекцию № 8, задача 5). Анализируя зависимость энергии Гиббса от давления и температуры, легко можно вывести уравнение, связывающее температуру плавления и радиус наночастиц – его называют уравнением Гиббса–Томсона:
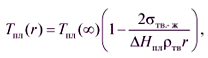
где Tпл(r) – температура плавления нанообъекта с радиусом наночастиц r, Tпл( 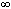 ) – температура плавления обычного металла (объемной фазы), тв.-ж – поверхностное натяжение между жидкой и твердой фазами,
) – температура плавления обычного металла (объемной фазы), тв.-ж – поверхностное натяжение между жидкой и твердой фазами, 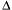 Hпл – удельная теплота плавления,
Hпл – удельная теплота плавления,  тв – плотность твердого вещества.
тв – плотность твердого вещества.
Используя это уравнение, можно оценить, начиная с какого размера свойства нанофазы начнут отличаться от свойств обычного материала. В качестве критерия возьмем отличие в температуре плавления 1 % (для золота – это около 14 °С). В «Кратком химическом справочнике» (авторы – В.А.Рабинович, З.Я.Хавин) находим для золота: 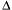 Hпл = 12,55 кДж/моль = 63,71 Дж/г,
Hпл = 12,55 кДж/моль = 63,71 Дж/г,  тв = 19,3 г/см3. В научной литературе для поверхностного натяжения приводится значение
тв = 19,3 г/см3. В научной литературе для поверхностного натяжения приводится значение  тв.-ж = 0,55 Н/м = 5,5–10–5Дж/см2. Решим с этими данными неравенство:
тв.-ж = 0,55 Н/м = 5,5–10–5Дж/см2. Решим с этими данными неравенство:

Эта оценка, хотя и довольно грубая, отлично коррелирует со значением 100 нм, которое обычно используют, говоря о предельных размерах наночастиц. Разумеется, здесь мы не учитывали зависимость теплоты плавления от температуры и поверхностного натяжения от размера частиц, а последний эффект может быть вполне значимым, о чем свидетельствуют результаты научных исследований [ ].
Интересно, что нанокластеры присутствуют даже в обычной воде. Они представляют собой агломераты из отдельных молекул воды, соединенных друг с другом водородными связями. Подсчитано, что в насыщенном водяном паре при комнатной температуре и атмосферном давлении на 10 миллионов одиночных молекул воды приходится 10000 димеров (Н2О)2, 10 циклических тримеров (Н2О)3 и один тетрамер (Н2О)4. В жидкой воде обнаружены и частицы гораздо большей молекулярной массы, образованные из нескольких десятков и даже сотен молекул воды. Некоторые из них существуют в нескольких изомерных модификациях, различающихся формой и порядком соединения отдельных молекул. Особенно много кластеров содержится в воде при низкой температуре, вблизи точки плавления. Такая вода характеризуется особыми свойствами – она имеет большую плотность по сравнению со льдом и лучше усваивается растениями. Это еще один пример того, что свойства вещества определяются не только его качественным или количественным составом, т.е. химической формулой, но и его строением, в том числе и на наноуровне.
Среди других нанообъектов наиболее полно изучены нанотрубки. Так называют протяжные цилиндрические структуры, имеющие размеры нескольких нанометров. Впервые углеродные нанотрубки были открыты в 1951 г. советскими физиками Л.В.Радушкевичем и В.М.Лукьяновичем, однако их публикация, появившаяся год спустя в отечественном научном журнале, прошла незамеченной. Вновь интерес к ним возник после работ зарубежных исследователей в 1990-е гг. Углеродные нанотрубки в сто раз прочнее стали, многие из них хорошо проводят тепло и электрический ток.
Недавно ученым удалось синтезировать нанотрубки нитрида бора, а также некоторых металлов, например золота (рис. 7, см. с. 14). По прочности они существенно уступают углеродным, но, благодаря гораздо большему диаметру, способны включать в себя даже сравнительно крупные молекулы. Для получения нанотрубок золота нагревание не требуется – все операции проводят при комнатной температуре. Через колонку, заполненную пористым оксидом алюминия, пропускают коллоидный раствор золота с размером частиц 14 нм. При этом кластеры золота застревают в порах, имеющихся в структуре оксида алюминия, объединяясь друг с другом в нанотрубки. Чтобы освободить образовавшиеся нанотрубки от оксида алюминия, порошок обрабатывают кислотой – оксид алюминия растворяется, а на дне сосуда оседают нанотрубки золота, на микрофотографии напоминающие водоросли.
Примером одномерных нанообъектов служат нанонити, или нанопроволоки – так называют протяженные наноструктуры с сечением менее 10 нм. При таком порядке величин объект начинает проявлять особые, квантовые свойства. Сравним нанопроволоку из меди длиной 10 см и диаметром 3,6 нм с такой же проволокой, но диаметром 0,5 мм. Размеры обычной проволоки во много раз больше расстояний между атомами, поэтому электроны свободно перемещаются во всех направлениях. В нанопроволоке электроны способны свободно двигаться лишь в одном направлении – вдоль проволоки, но не поперек, т.к. ее диаметр всего лишь в несколько раз превышает расстояние между атомами. Физики говорят, что в нанопроволоке электроны в поперечных направлениях локализованы, а в продольном – делокализованы.

|
| Рис. 5. 3. Микрофотографии золотых нанотрубок |
Известны нанопроволоки металлов (никеля, золота, меди) и полупроводников (кремния), диэлектриков (оксида кремния). При медленном взаимодействии паров кремния с кислородом в особых условиях удается получить нанопроволоки оксида кремния, на которых как на веточках висят шаровидные образования из кремнезема, напоминающие ягоды вишни. Размер такой «ягоды» составляет всего 20 микрон (мкм). Несколько особняком стоят молекулярные нанопроволоки, примером которых служит молекула ДНК – хранитель наследственной информации. Небольшое количество неорганических молекулярных нанопроволок представляют собой сульфиды или селениды молибдена. Фрагмент структуры одного из этих соединений приведен на рис. 4. Благодаря наличию d-электронов в атомах молибдена и перекрыванию частично заполненных d-орбиталей это вещество проводит электрический ток.

|
| Рис. 5.4. Структура нанопроволоки селенида молибдена, состоящей из семи слабо взаимодействующих молекулярных цепочек |
Полупроводниковые нанопроволоки подобно обычным полупроводникам могут быть допированы** по р- или n-типу. Уже сейчас на основе нанопроволок созданы p–n-переходы с необычайно малым размером. Так постепенно создаются основы для развития наноэлектроники.
Высокая прочность нановолокон делает возможным армирование ими различных материалов, в том числе полимеров, с целью увеличения их жесткости. А замена традиционного угольного анода в литий-ионных батареях стальным анодом, покрытым нанонитями кремния, позволила на порядок увеличить емкость этого источника тока.
Примером двумерных нанообъектов служат нанопленки. Благодаря очень малой толщине (всего в одну или две молекулы) они пропускают свет и незаметны для глаза. Полимерные нанопокрытия из полистирола и других полимеров надежно защищают многие предметы, используемые в быту, – экраны компьютеров, окошки сотовых телефонов, линзы очков.
Одиночные нанокристаллы полупроводников (например, сульфида цинка ZnS или селенида кадмия CdSe) размером до 10–50 нм называют квантовыми точками. Их считают нуль-мерными нанообъектами. Такие нанообъекты содержат от ста до ста тысяч атомов. При облучении квантового полупроводника возникает пара «электрон–дырка» (экситон), движение которой в квантовой точке ограничено по всем направлениям. Благодаря этому энергетические уровни экситона дискретны. Переходя из возбужденного состояния в основное, квантовая точка испускает свет, причем длина волны зависит от размера точки. Эту способность используют для разработки лазеров и дисплеев нового поколения. Квантовые точки можно использовать и в качестве биологических меток (маркеров), соединяя их с определенными белками. Кадмий довольно токсичен, поэтому при производстве квантовых точек на основе селенида кадмия их покрывают защитной оболочкой сульфида цинка. А для получения водорастворимых квантовых точек, что необходимо для биологических приложений, цинк соединяют с органическими лигандами небольшого размера.
Магнитные свойства. Свойства наночастиц магнитных материалов существенно отличаются от свойств макрочастиц. Размерный эффект проявляется в значительном понижении точки Кюри. Для наночастиц Fe, Co, Ni размером менее 10 нм точка Кюри находится на сотни градусов ниже, чем для макроскопических образцов.
Магнитные размерные эффекты проявляются очень ярко у кластеров Pd. Макроскопические образцы Pd обладают парамагнетизмом и их магнитная восприимчивость почти не зависит от температуры вплоть до температуры жидкого He.
При значительном уменьшении размеров кластера они становятся диамагнитными. Размер дисперсных частиц влияет также на коэрцитивное поле или силу (Нс, А/м), являющейся одной из важнейших характеристик ферромагнитных материалов. При Нс 100 А/м материалы считаются магнитомягкими, при Нс 100 А/м магнитожесткими.
Коэрцетивное поле нанокластеров (d 4 нм) железа почти нулевое. Такие низкие значения обусловлены тепловыми колебаниями. При комнатной температуре для железа коэрцитивное поле максимально для кристаллов размером 20-25 нм. Поэтому нанокристаллические ферромагнетики можно использовать для получения запоминающих устройств с большой памятью. Очень перспективно использование нанодисперсных намагниченных частиц диаметром около 10 нм для приготовления ферромагнитных жидкостей – коллоидных растворов, в которых дисперсной фазой являются наномагнитные частицы, а дисперсионной средой – жидкость, например вода или керосин. При наложении внешнего магнитного поля наночастицы начинают двигаться и включают в движение окружающую жидкость. Перспектива промышленного использования этого эффекта весьма велика (например, для охлаждения мощных трансформаторов в электротехнике, для магнитного обогащения руд, для очистки водных бассейнов от нефтяных загрязнений). В области медицины магнитные наночастицы могут использоваться, в частности, в качестве доставщиков лекарственных средств направленного действия.
Каталитические свойства.Высокодисперсные и особенно нанодисперсные твердые частицы металлов и оксидов металлов имеют высокую каталитическую активность, что позволяет проводить различные химические реакции при сравнительно невысоких температурах и давлениях. Приведем пример, показывающий каталитические свойства высокодисперсных частиц.
Наночастицы Au размером 3 - 5 нм обладают высокоспецифической каталитической активностью. Ее появление сопряжено с переходом кристаллической структуры золота от гранецентрированной кубической в более крупных частицах к икосаэдрической структуре наночастиц. Важнейшие характеристики этих нанокатализаторов (активность, избирательность, температура) зависят от материала подложки, на которую их наносят. Кроме того, очень сильно влияют даже следы влаги. Наноразмерные частицы Au эффективно катализируют окисление монооксида углерода при низких (до -70 °С) температурах. Вместе с тем они обладают очень высокой избирательностью при восстановлении оксидов азота при комнатной температуре, если частицы золота нанесены на поверхность оксида алюминия
Наночастицы различных материалов применяются повсеместно – от лакокрасочной до пищевой промышленности. Наиболее «популярными» наночастицами являются частицы, из углерода (нанотрубки, фуллерены, графен), наночастицы оксида кремния, золота, серебра, а также оксида цинка и диоксида титана. Коротко обсудим, как они применяются и какими биологическими эффектами могут обладать.
Углеродные наночастицы, в частности, углеродные нанотрубки (УНТ) имеют уникальные электропроводные, теплопроводные, механические свойства, они находят широкое применение в электронике, входят в состав композиционных материалов, применяющихся для самых различных целей – от производства материалов для теннисных ракеток до деталей для космических кораблей. Недавно было установлено, что агломераты УНТ могут образовываться в результате процессов сгорания углеводородов, в том числе бытового газа, и содержатся в пыли и воздухе. Способность УНТ преодолевать биологические мембраны, их способность проникать через гематоэнцефалический барьер служат основой для проведения исследований по использованию УНТ в качестве носителей для адресной доставки лекарств. Исследования о токсичности УНТ дают часто противоречивые результаты, и на сегодняшний момент данный вопрос является открытым.
Большую часть производимого наноразмерного SiO2 составляют нанопорошки аморфного диоксида кремния (НАДК). Они широко применяются в промышленности – в процессе изготовления теплоизоляторов, в производстве оптоэлектроники, как компонент для получения термостойких красок, лаков и клеев, а так же как стабилизаторы эмульсий. Также НАДК добавляют в покрытия для защиты от абразивных повреждений и царапин. Для того чтобы покрытие было прозрачным, используются нанопорошки со средним размером частиц менее 40 нм. Системная токсичность наночастиц диоксида кремния для животных и человека изучена слабо, однако широта спектра их применений ставит их на одно из первых мест в списке наночастиц, требующих детального изучения их биологических свойств.
Началом научных исследований коллоидного золота (КЗ) следует считать середину XIX века, когда вышла статья Майкла Фарадея , посвященная методам синтеза и свойствам КЗ. Фарадей впервые описал агрегацию КЗ в присутствии электролитов, защитный эффект желатина и других высокомолекулярных соединений, свойства тонких пленок КЗ. В настоящее время КЗ используется как объект для изучения оптических свойств частиц металлов, механизмов агрегации и стабилизации коллоидов. Известны примеры применения КЗ в медицине, в частности, в цветных реакциях на белки. Частицы золота применяют для изучения транспорта веществ в клетку путем эндоцитоза, для доставки генетического материала в клеточное ядро, а также для адресной доставки лекарственных веществ. Промышленности наночастицы коллоидного золота используются при фотопечати и в производстве стекла и красителей.
| Рис. 5.4. Электронная микрофотография коллоидных наночастиц серебра |
 Коллоидное наносеребро – продукт, состоящий из наночастиц серебра, взвешенных в воде, содержащей стабилизатор коллоидной системы (Рис 5). Типичный размер наночастиц серебра – 5-50 нм. Области применения наночастиц серебра могут быть различными: спектрально-селективные покрытия для поглощения солнечной энергии, в качестве катализаторов химических реакций, для антимикробной стерилизации. Последняя область применения является наиболее важной и включает в себя производство различных средств упаковки, перевязки и водоэмульсионных красок и эмалей. В настоящее время на основе коллоидного серебра выпускаются препараты - биологически активные добавки с антибактериальным, противовирусным и противогрибковым действием. Препараты коллоидного серебра являются одними из наиболее распространенных и широко используемых в индустрии наночастиц. Слоем наночастиц серебра покрывают столовые приборы, дверные ручки и даже клавиатуру и «мышки» для компьютеров. Наночастицы серебра используют при создании новых покрытий и косметики. Так же наноразмерное серебро используется для очистки воды и уничтожения болезнетворных микроорганизмов в фильтрах систем кондиционирования воздуха, в бассейнах, душах и других местах. Однако вопрос о влиянии наночастиц серебра на окружающую среду остается открытым.
Коллоидное наносеребро – продукт, состоящий из наночастиц серебра, взвешенных в воде, содержащей стабилизатор коллоидной системы (Рис 5). Типичный размер наночастиц серебра – 5-50 нм. Области применения наночастиц серебра могут быть различными: спектрально-селективные покрытия для поглощения солнечной энергии, в качестве катализаторов химических реакций, для антимикробной стерилизации. Последняя область применения является наиболее важной и включает в себя производство различных средств упаковки, перевязки и водоэмульсионных красок и эмалей. В настоящее время на основе коллоидного серебра выпускаются препараты - биологически активные добавки с антибактериальным, противовирусным и противогрибковым действием. Препараты коллоидного серебра являются одними из наиболее распространенных и широко используемых в индустрии наночастиц. Слоем наночастиц серебра покрывают столовые приборы, дверные ручки и даже клавиатуру и «мышки» для компьютеров. Наночастицы серебра используют при создании новых покрытий и косметики. Так же наноразмерное серебро используется для очистки воды и уничтожения болезнетворных микроорганизмов в фильтрах систем кондиционирования воздуха, в бассейнах, душах и других местах. Однако вопрос о влиянии наночастиц серебра на окружающую среду остается открытым.
Наночастицы вещества часто обладают свойствами, которых нет у образцов этих веществ, имеющих обычные размеры. Так, наночастицы серебра и золота становятся хорошими катализаторами химических реакций, а так же непосредственно участвуют в них. Наночастицы серебра проявляют способность генерировать активные формы кислорода [2]. Поэтому по сравнению с серебром макроразмеров его наночастицы могут проявлять большую токсичность. В организме человека наночастицы серебра могут приводить к целому спектру ответов тканей организма, например, к активации клеток, их смерти, генерации активных форм кислорода, воспалительным процессам в разных тканях и органах.
Наиболее интересными свойствами, благодаря которым наночастицы оксида цинка и диоксида титана получили свое распространение, являются их антибактериальных и фото-каталитические свойства. На настоящий момент частицы ZnO и TiO2 используются в качестве антисептиков в зубной пасте и косметике, краске, пластике и текстиле. Благодаря фотокаталитической активности и поглощению света в УФ диапазоне оксид цинка и диоксид титана получили широкое распространение в солнцезащитных кремах [3]. Сравнительный анализ солнцезащитных кремов показал, что из 1200 кремов 228 содержат оксид цинка, 363 содержат диоксид титана и 73 содержат оба этих элемента [4]. При этом в 70% кремов, содержащих диоксид титана, и в 30% кремов, содержащих оксид цинка, эти элементы находились в форме наночастиц. Фотокаталитическая активность частиц ZnO и TiO2заключается в том, что под действием света эти частицы способны захватывать электроны близлежащих молекул. Если наночастицы находятся в водном растворе, то этот процесс ведет к образованию активных форм кислорода, преимущественно гидроксил радикалов [6, 7]. Эти свойства обуславливают антисептические свойства наночастиц, а также могут быть использованы для направленной модификации поверхности наночастиц или молекул, находящихся на их поверхности [6]. Несмотря на широкую распространенность наночастиц ZnO и TiO2 в косметических средствах и продуктах питания, в последнее время появляется все больше работ, в которых показано, что фотокаталитическая активность может оказывать токсическое воздействия на клетки и ткани [5]. Так, показано, что TiO2 является генотоксичным, т.е. вызывает разрывы нитей ДНК, в клетках человека и рыб, под действием света [8, 9] и может способствовать старению организма за счет образования активных форм кислорода.
При использовании наноразмерных материалов в промышленности не следует забывать о экотоксичности наночастиц. Простой подсчет показывает, что в 2 г наночастиц размером 100 нм, содержится столько наночастиц, что на каждого человека на земле придется примерно по 300 000 тысяч [5]. Применение наночастиц в промышленности и, значит, содержание их в нашем окружении, с каждым годом продолжает увеличиваться. С одной стороны, преимущество использования наночастиц очевидно. С другой стороны, на настоящий момент проблема обнаружения наночастиц не изучена, и возможность влияния их на организм человека остается открытой. Данные, полученные в различных исследованиях о влиянии наночастиц на организмы достаточно противоречивы, но забывать об актуальности данной проблемы не стоит. Необходимо продолжать исследовать влияние наночастиц на живые организмы и создавать методы детекции наночастиц в окружающей среде.
Мир наноструктур, уже созданных учеными, очень богат и разнообразен. Пока лишь небольшая часть достижений нанонауки доведена до уровня нанотехнологий, однако процент реализации все время растет, и через несколько десятков лет наши потомки будут недоумевать – как же мы могли существовать без нанотехнологий!