ФаРМАЦЕВТИЧЕСКИЕ ФАКТОРЫ, ИХ ОПРЕДЕЛЕНИЕ, РОЛЬ И ЗНАЧЕНИЕ.
Избранные лекции по биофармации и современным достижениям фармацевтической технологии
Рассмотрены ЦМС ЗГМУ
(протокол № ___от
______________)
и рекомендованы в качестве учебного пособия студентам фармацевтических вузов, провизорам-интернам, слушателям последипломного повышения квалификации специалистов фармации
Запорожье
Издательство ЗГМУ
УДК 615.015.4:57+615.4.012/.014(042)
Авторы: д-р фарм. наук, проф. В.А. Головкин, канд. фарм. наук, доцент В.П. Соловьева, д-р фарм. наук, проф. В.В. Гладышев.
Рецензенты: д-р фарм. наук, проф. Е.Е. Борзунов (Киевская медицинская академия последипломного образования им. П.Л. Шупика); д-р фарм. наук, проф. Е.Г. Кныш (Запорожский государственный медицинский университет).
В соответствии с программой по технологии лекарств рассмотрены теоретические и практические аспекты современ-ного направления в лекарствоведении – биофармации, а также достижения фармацевтической технологии, основанные на биофармацевтической концепции о биологической значимости переменных (фармацевтических) факторов. При изложении материала уделено внимание стандартизации лекарственных средств, в соответствии с существующими региональными и международными требованиями к качеству и эффективности продукции фармацевтической отрасли.
Для студентов, интернов - провизоров и слушателей отделений последипломного повышения квалификации специа-листов фармации.
Оглавление
| Лекция 1. Введение в биофармацию. Цель и задачи дисциплины…………….…………………… Лекция 2. Фармацевтические факторы. Их определение, роль и значение ……….....…. Лекция 3. Параметры фармацевтической доступности. Методы и устройства для ее определения... Лекция 4. Транспорт лекарственных веществ в организме ………………………………..… Лекция 5. Понятие биологической доступности лекарств. Методы ее исследования .....…… Лекция 6. Общие сведения о фармакокинетике. Всасывание лекарственных веществ и факторы, влияющие на этот процесс …...... Лекция 7. Взаимодействие ингредиентов лекарственных препаратов и биологическая доступность …………………………….… Лекция 8. Достижения фармацевтической технологии по созданию лекарственных препаратов с регулируемым высвобождением ингредиентов и направленным фармакотерапевтическим действием. Твердые терапевтические системы ….……. Лекция 9. Макромолекулярные терапевтические системы с регулируемым высвобождением лекарственных веществ. Терапевтические системы …………………………………..…. Лекция 10. Солюбилизация. Терапевтические системы направленного транспорта лекарственных веществ в организме ……… Лекция 11.Магнитоуправляемые терапевтические системы …………………..…………………. Лекция 12.Проблемы повышения стабильности готовых лекарственных препаратов ….…… Лекция 13. Современные методы определения стабильности готовых лекарственных препаратов ………………………………….. Список литературы ……………………………………. Приложения……………………………………………... |
Лекция 1
ВВЕДЕНИЕ В БИОФАРМАЦИЮ. Цель и задачи дисциплины
Из истории фармации известно, что еще в 1838 году профессор А.А. Иовский впервые применил в науке об изготовлении лекарств понятие "технология", подразумевая под этим термином науку о способах производства лекарств. Еще в начале прошлого столетия отмечалось большое значение технологии производственного процесса, процесса превращения исходных лекарственных веществ в лекарственную форму, призванную помочь организму ослабить, уничтожить или предупредить заболевание.
Интенсивное развитие фармацевтического производства, проникновение в фармацию новых идей и методов научно-технического прогресса заставило пересмотреть некоторые концепции и представления в ведущей отрасли фармации - технологии лекарств.
Получение и внедрение в практику новых лекарственных веществ, обладающих сильным фармакологическим эффектом, введение их в традиционные лекарственные формы, способствовало повышению удельного веса вспомогательных веществ. Достижение химии позволили значительно расширить ассортимент вспомогательных веществ: растворителей, салюбилизаторов, стабилизаторов, поверхостно-активных веществ, загустителей, эмульгаторов, красителей, корригентов, различного рода основ и формообразователей, в частности различных соединений из группы природных и синтетических полимеров - МЦ, NaКМЦ, ПВП, ПЭГ, амилопектин, циклодестрин и другие.
Уже к 50 г. XX столетия усовершенствование промышленной технологии позволило интенсифицировать различные стадии фармацевтического производства (микронизация, ультраэмульгирование, ультразвуковая и др. виды стерилизации и т.д.), это сказалось на поверхностных свойствах и образовании метастабильных модификаций лекарственных и вспомогательных веществ.
Именно введение в практику новых высокоактивных лекарственных веществ, вспомогательных материалов и совершенных технологических процессов и составило материальную основу того необычного феномена, который получил в научной литературе название "терапевтической неэквивалентности или неадекватности лекарств". Сущность такой неэквивалентности (неадекватности) состоит в том, что одинаковые дозы (часто высокоактивных) лекарственных веществ, назначенные в идентичных лекарственных формах, приготовленных различными предприятиями оказывают различное фармакотерапевтическое действие. Например, таблетки содержащие равные дозы хлорамфеникола, фенил бутазона, дигоксина, тетрациклина, преднизона, тироидина и др., произведенные одним заводом, оказывают лечебное действие, произведенные другим заводом - токсическое, а третьим – вообще не оказывают должного действия. Хотя все заводы готовили таблетки по утвержденным прописям и лекарственные формы соответствовали требованиям фармакопеи или других нормирующих документов.
Тщательное исследование известных случаев терапевти-ческой неэквивалентности лекарств, показали, что активность действующего вещества, его поведение в процессе высвобож-дения из лекарственной формы, диффузия к месту всасывания, да и сам процесс всасывания находятся в теснейшей зависимос-ти от природы и количества вспомогательных веществ и технологических операций, имеющих место при получении лекарств.
Проведенные исследования случаев терапевтической неэквивалентности лекарств в огромной степени способствовали утверждению новых представлений, биофармацевтических, в основу которых положено признание биологической (медицинс-кой) значимости всех компонентов лекарственной формы и рассмотрение лекарства как сложной физико-химической систе-мы, состоящей из диалектического единства лекарственных веществ и переменных факторов, сопровождающих приготовление лекарства.
В конце 50-х годов и утвердилось новое направление в фармации - биофармацевтическое. А сам термин биофармация был сформулирован Wagner W. и Levy G. в 1961 г.
Биофармацию определяют как науку, изучающую биологическое действие лекарств в зависимости от физико-химических свойств, вида лекарственной формы, технологии приготовления, и других переменных факторов. Основным в биофармации является признание биологического значения фармацевтических процессов, протекающих при получении лекарств и рассмотрение лекарств, в качестве сложных физико-химических систем, способных вступить в определенные взаимодействия с системой живого организма.
Хотя биофармация, как новейшая ветвь фармацевтической науки и медицины, возникла сравнительно недавно, многие экспериментальные данные этой науки были получены отечественными и зарубежными учеными еще в XIX столетии и послужили фактически отправным пунктом для ее развития.
Так, на заре создания технологии лекарств профессор Московского университета А.А.Иовский (I796-I858 гг.) в своем руководстве "Начертание фармации" в 1838 г. писал: "Фармацевтическая наука отыскивает приличные формы с целью сделать лекарство безопаснее и полезнее для здоровья".
О сложном взаимодействии лекарственной формы, как особой физико-химической системы и макроорганизма, как биологической системы и факторах, обуславливающих такое взаимодействие, указывали в своих работах отечественные ученые Боткин С.П. (1897 г.), Манассеин В.А. (в своих лекциях "Лекции по общей терапии" 1879 г.), Засецкий Н.А. (1880 г.). В отдельных учебниках по технологии лекарств Шубин С.Ф. (1948 г.), Коган Г.Я. (1952 г.) отмечалось влияние вспомогательных веществ, степени измельчения лекарственных веществ на процессы всасывания лекарств.
Всe факты, предположения о взаимодействии лекарства и биологических систем организма были обобщены, систематизи-рованы биофармацией как новейшей фармацевтической дисциплиной, предметом изучения которой и является комплекс переменных факторов, сопутствующих созданию лекарств, влияющих на транспорт и взаимодействие лекарственных веществ с системами живого организма.
НАПРАВЛЕНИЯ ИССЛЕДОВАНий ПО БИОФАРМАЦИИ
1. Исследование влияния простой химической модифика-ции на процессы высвобождения веществ из лекарственной формы, их фармакокинетику, а также стабильность самой лекарственной формы.
2. Исследование влияния физического состояния лекарственных веществ на скорость высвобождения и всасывания лекарственных веществ, на стабильность лекарственной формы.
3. Исследование влияния природы и количества вспомогательных веществ на высвобождение и фармакокине-тику лекарственных веществ, а также на стабильность лекарственной формы в процессе их хранения и применения.
4. Исследование влияния производственных процессов - методов приготовления лекарств, на выделение из лекарствен-ной формы и кинетику в организме лекарственных веществ, а также стабильность лекарственной формы.
5. Исследование влияния вида лекарственной формы на высвобождение и фармакокинетику лекарственных веществ.
Таким образом, круг исследований охватывает широкий комплекс взаимосвязанных проблем, определяющих в конечном итоге эффективность лекарственного вмешательства.
За период своего существования биофармация обогатилась новыми открытиями и заняла прочное место в системе современного лекарствоведения.
В биофармацевтические исследования включают также изучение влияния возраста, биологических ритмов, взаимо-действия медикаментов, применяемых одновременно, состава пищи на процессы всасывания и метаболизма лекарств.
Представляем выдающихся отечественных ученых, внесших вклад в развитие биофармации:
И.С. Ажгихин - профессор, зав. отделом Института моря и океана АН РФ, впервые (совместно с проф. А.И.Тенцовой) издавший в 1975 г. монографию по биофармацевтическим исследованиям "Лекарственная форма и терапевтическая эффективность лекарств".
А.И.Тенцова - профессор кафедры заводской технологии лекарств I Московской медицинской академии, создатель отечественной школы ученых по проблемам биофармации.
И.А. Муравьев - профессор кафедры технологии лекарств Пятигорской фармацевтической академии, создатель школы отечественных технологов фитохимиков. Им и его школой разрабатываются проблемы по установлению значения различных переменных (фармацевтических) факторов в повышении качества и эффективности экстракционных препаратов.
Плодотворно в области биофармации в настоящее время работают профессора: Перцев И.И.(мази), Борзунов Е.Е. (таблетки), Башура Г.С. (аэрозоли), Головкин В.А. (ректальные и вагинальные средства).
Кафедра технологии лекарств Запорожского медицинского университета также успешно трудится над разработкой биофармацевтических проблем повышения качества и эффективности ректальных, вагинальных лекарственных форм, мазей, пленок и таблетированных препаратов. На кафедре, основываясь на биофармацевтических принципах исследований впервые предложены оригинальные составы и технология суппозиториев с сердечными гликозидами, детских микроклизм с анальгетико-спазмолитическими средствами, противовоспали-тельных и ранозаживляющих мазей. Проблема создания табле-тированных препаратов успешно решается путем локализации высвобождения лекарственных веществ в определенных отделах желудочно-кишечного тракта (энтеросолюбильные пленочные покрытия).
Сотрудниками кафедры, одними из первых в биофармацевтических исследованиях показана прямая корреляционная взаимосвязь между результатами опытов по высвобождению (выделению) некоторых лекарственных веществ (анальгетического, жаропонижающего, спазмолити-ческого действия) из мягких лекарственных форм (мазей и суппозиториев) и всасываемостью, поступлением в живой организм этих веществ в опытах in vivo.
Технологическая и биофармацевтическая терминология и понятия.
В соответствии с Законом Украины «Про лікарські засоби» приводим отдельные термины и понятия, общие для технологии лекарств и биофармации.
1. Лекарственные средства – вещества или их смеси природного, синтетического или биотехнологического проис-хождения, которые применяются для профилактики, диагности-ки и лечения заболеваний человека или изменения состояний и функций организма.
К лекарственным средствам отнесены – действующие вещества (субстанции), готовые лекарственные средства (лекарственные препараты, лекарства, медикаменты); гомеопа-тические средства; средства для выявления возбудителей заболеваний и для борьбы с этими возбудителями или паразитами; лекарственные косметические средства и лекарственные добавки к пищевым смесям.
2. Готовые лекарственные средства (лекарственные препараты, лекарства, медикаменты) – дозированные лекарст-венные средства в таком виде и состоянии, в котором их применяют.
К готовым лекарственным средствам относят капсулы, таблетки, ампульные растворы, спансулы, мази, гранулы и др.
3. Действующие вещества (субстанции) – биологически активные вещества, которые могут изменять состояние и функции организма или обладают профилактическим, диагностическим или лечебным действием и используются для производства готовых лекарственных средств.
4. Вспомогательные вещества – дополнительные вещест-ва, необходимые для приготовления готовых лекарственных средств.
5. Государственный реестр лекарственных средств Украины – нормативный документ, который содержит сведения о лекарственных средствах, разрешенных для производства и применения в медицинской практике.
6. Фармакопейная статья – нормативно-технический документ, который устанавливает требования к лекарственному средству, его упаковке, условиям и сроку хранения, методам контроля качества лекарственного средства.
7. Государственная Фармакопея Украины – правовой акт, который содержит общие требования к лекарственным средствам, монографии на лекарственные вещества и средства, а также методики контроля качества лекарственных средств.
8. Качество лекарственного средства – совокупность свойств, которые придают лекарственному средству способ-ность удовлетворять потребителей соответственно своему назначению и соответствуют требованиям, установленным законодательством.
9. Срок пригодности лекарственных средств – время, на протяжении которого лекарственное средство не теряет своего качества при условии хранения соответственно требованиям нормативно-технической документации.
СПЕЦИФИЧЕСКИЕ БИОФАРМАЦЕВТИЧЕСКИЕ ТЕРМИНЫ
1. Переменные факторы - фармацевтические факторы - иногда их называют биофармацевтическими факторами - это наиболее существенные процессы, сопровождающие изготовле-ние лекарства и отдельные компоненты лекарства, характери-зующиеся определенными свойствами. Например, физическое состояние лекарственных веществ - дисперсность, раствори-мость, характер кристаллической структуры, природа и количество вспомогательных веществ; методика приготовления лекарственной формы и применяемая при этом аппаратура и т.д.
2. Фармацевтическая доступность (ФД) - определяют степень и скорость высвобождения (выделения, растворения) лекарственных веществ из лекарственной формы, препарата).
Устанавливают ФД различными методиками in vitro (в склянке), основанными на определении концентрации высвободившегося вещества различными физико-химическими методами.
3. Биологическая доступность (БД) - определяет степень и скорость поступления (всасывания) лекарственных веществ в живой организм.
Устанавливают БД различными методиками in vivo (в живом организме), основанными на определении концентрации поступившего в живой организм лекарственного вещества или образовавшегося из него метаболита в биологической жидкости - крови, лимфе, моче, слюне, межклеточной жидкости.
Для определения БД лекарственных веществ в определенной форме или препарате иногда устанавливают также уровни (величины) фармакодинамических реакций организма в ответ на введенное вещество - частоту пульса, повышение или снижение температуры тела, мышечный тонус и др.
4. Фармакокинетические показатели (ФКП) - величины, характеризующие перемещение лекарственного вещества в живом организме от всасывания и поступления в биологичес-кую жидкость, биотрансформации и метаболизма, до выведения известными путями (с мочой, слезой, потом и др.).
Устанавливаются методами, принятыми в фармакокине-тике – области науки (лекарствоведения), изучающей движение лекарственных веществ в организме.
К наиболее существенным ФКП относятся – AUC0-¥ (или S0-¥) – площадь под кривыми изменения концентрации лекарственного вещества в биологической жидкости в зависи-мости от времени.
Квс (всасывания) – константа скорости всасывания, характеризующая интенсивность поступления лекарственного вещества в организм за единицу времени. Размерность: ч-1; мин-1, сек-1
Кэлим (константа выделения [элиминация]), характери-зующая интенсивность высвобождения организма от лекарст-венного вещества. Размерность: ч-1; мин-1, сек-1 .
Период полусуществования – Т1/2 или Т50% лекарственного вещества в организме характеризуется временем, в течение которого концентрация вещества в крови снижается на половину: 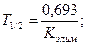 а также ряд других величин, определение которых проводят с использованием методов формализации результатов кинетических исследований.
а также ряд других величин, определение которых проводят с использованием методов формализации результатов кинетических исследований.
Биофармация использует для установления качества лекарств известные физико-химические методики, и кроме того, методы фармакокинетики, специфические биофармацевтические методики (in vitro и in vivo).
Лекция 2
ФаРМАЦЕВТИЧЕСКИЕ ФАКТОРЫ, ИХ ОПРЕДЕЛЕНИЕ, РОЛЬ И ЗНАЧЕНИЕ.
Предметом специального исследования биофармации являются фармацевтические факторы.
Условным термином "фармацевтические факторы" опреде-ляют наиболее существенные процессы, имеющие место при изготовлении лекарств, и компоненты лекарств, характеризую-щиеся теми или иными физико-химическими свойствами.
К фармацевтическим факторам относят:
1) простую химическую модификацию лекарственных и вспомогательных веществ;
2) физическое состояние лекарственных и вспомогатель-ных веществ;
3) технологические процессы получения лекарств;
4) природа, свойства вспомогательных веществ;
5) вид лекарственной формы.
В основу биофармацевтических представлений положено признание биологической (медицинской) значимости всех фармацевтических факторов и рассмотрение лекарства как сложной физико-химической системы, диалектического единст-ва лекарственных веществ и фармацевтических факторов.
Достоверно установлено, что если химическая природа и доза лекарственного вещества обуславливает биологическое действие лекарства, то уровень этого действия в значительной мере зависит от фармацевтических факторов.
Поэтомулекарства, содержащие равные дозы одних и тех же веществ, но различающиеся примененными при их изготовлении фармацевтическими факторами (видом вспомога-тельных веществ, способом приготовления, физическим состоя-нием или простой химической модификацией и др.) могут оказывать разный (неадекватный) терапевтический эффект.
Под термином "терапевтически неадекватные лекарства" подразумевают лекарства (лекарственные формы), содержащие одни и те же дозы одних и тех же действующих веществ, часто даже в одинаковой лекарственной форме, но оказывающие различный по силе, уровню терапевтический эффект.
Объяснить появление терапевтически неадекватных лекарств и найти пути устранения этого явления смогла биофармация, потребовавшая научно-обоснованного изучения и выбора фармацевтических факторов в процессе создания лекарств, тщательного учета влияния каждого из них не только на стабильность лекарств, но главным образом, прежде всего на процессыпоступления (всасывания) лекарств в организм, их распределения и выделения.
Рассмотрим отдельные примеры значимости фармацевтических факторов для качества и эффективности лекарств.
Под "простой химической модификацией" лекарственных веществ понимают использование последних в виде различных солей, кислот, оснований, в которых полностью сохраняется ответственная за фармакологический эффект часть молекулы вещества. Так, например, в случае антибиотика бензилпеницил-лина рассчитывают, что I мг натриевой соли вещества содержит 1670 ЕД бензилпенициллина; I мг калиевой соли - соответственно эквивалентны 1600 ЕД бензилпеницил-лина; I мг новокаина бензилпенициллина соответствует 1011 ЕД бензилпенициллина.
При получении таблеток, инъекций, капсул, суппозиториев и др. лекарственных форм бензилпенициллина может иметь место замена любого из трех веществ бензилпенициллина эквивалентным по активности в ЕД количеством соответствую-щего вещества.
Однако клиническое применение трех названных простых модификаций препарата бензилпенициллина - натриевой соли, калиевой соли и новокаинбензилпенициллина покажет различные результаты, проистекающие из резкой разницы во всасывании каждого вещества. Так, в случае замены натриевой соли эквивалентным по активности количеством калиевой соли бензилпенициллина концентрация антибиотика в плазме крови будет на 40-50% больше; а в случае использования эквивалент-ных по активности количеств бензилпенициллин-новокаина — в 1,5 раза меньшей, чем при применении калиевой соли антибиотика.
Аналогичные результаты имеют место при назначении эквивалентных количеств калиевой, кальциевой соли и антибиотика феноксиметилпенипиллина в кислотной форме.
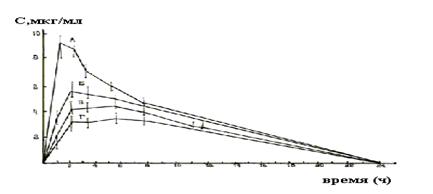 |
На рис. 2.1 приведены кинетические кривые изменения концентрации хлорамфеникола в плазме крови добровольцев после перорального назначения различных химических модификаций этого антибиотика. Очевидно, что модификация А обеспечивает значительно (почти в 2 раза) более высокий уровень вещества в биологической жидкости и, следовательно, может назначаться для достижения терапевтического эффекта в значительно меньших дозах сравнительно с модификациями Г, В или Б.
Рис. 2.1.
Концентрация в плазме добровольцев хлорамфеникола после перорального назначения 4 образцов антибиотика (АБВГ) по 0,5
Применение равных (в пересчете на основание) количеств эритромицина и его эфира (пропионат эритромицина) одной и той же группе больных обеспечивает далеко не совпадающие уровни этого антибиотика в плазме крови. Так, если принять условно за 100 концентрацию антибиотика в плазме крови после назначения эритромицина основания, то в крови людей, получавших эритромицина-пропионат его концентрация будет равна 200-400.
Данная закономерность (вообще) характерна для лекарственных веществ, являющихся слабыми кислотами и их солями и в равной степени для слабоосновных соединении и их солей (фенобарбитал-натриевая соль фенобарбитала; сульфатиа-зол - натриевая соль сульфатиазола; ацетилсалициловая кислота - натриевая соль ацетилсалициловой кислоты и т.д.).
Различие в скорости и полноте наступления терапевтичес-кого эффекта объясняется различным влиянием на всасывание веществ атомных группировок, рН в месте введения, различной растворимостью в липидах клеточных оболочек или физиологи-ческих жидкостях, секретах желудка и кишечника, различным значением их рКа, различным коэффициентом межфазного распределения и т.д.
Биофармация уделяет изучению фактора ("Простой химической модификации") самое серьезное внимание, ибо учет его влияния на фармакокинетику препаратов позволяет значительно повысить эффективность лекарственного вмеша-тельства, уменьшить расход препаратов, резко повысить стабильность многих лекарственных веществ и их смесей.
2. Под физическим состоянием лекарственного вещества как фармацевтического фактора подразумевают степень измельчения вещества, аморфность или кристалличность его, огранку кристаллов, характер кристаллов и кристаллогидратов, растворимость в воде и липидах, электропроводность, темпера-туру плавления и т.д., иными словами, поверхностные свойст-ва лекарственного вещества.
При всей кажущейся простоте слагаемых данного фармацевтического фактора влияние его на фармакотерапев-тическую эффективность препаратов, стабильность их в процессе хранения и многие другие показатели являются весьма ощутимыми, а для многих препаратов решающим. Так, степень измельчения лекарственного вещества обеспечивает не только однородность смешения ингредиентов, но во многом определяет стабильность вещества, его реакционную способность и интенсивность всасывания.
Особенно существенно значение степени измельчения в процессах всасывания трудно растворимых соединений, всасывание которых возрастает по мере уменьшения размера частиц (сульфаниламидные препараты, тетрациклин и др. антибиотики этого ряда, производные кумарина, бутадион, ацетилсалициловая кислота и др.). Растворимость любого из этих веществ зависит от размера его частиц и его поверхности: чем меньше размер частицы и чем больше суммарная поверхность частиц, тем скорее вещество перейдет в раствор и будет доступным для всасывания. Так, если измельчить такое вещество, как ацетилсалициловую кислоту в 5-10 раз по сравнению с фармакопейным веществом, то резко увеличива-ется растворимость этого соединения и его всасывание, и в 2 раза повышается его терапевтическая эффективность. Уменьшение частиц гризеофульвина с размера 10 мкм до 2,6 мкм позволяет уменьшить общую дозу вещества, в 2 раза: с 0,5 г до 0,25г, обеспечивая равное содержание его в крови.
В настоящее время для большой группы веществ установлено, что как скорость всасывания, так и терапевтичес-кая активность их варьируют в значительной степени в зависимости от степени измельчения. Так, при назначении одинаковых доз сульфадимезина микронизированного и обычной степени измельчения найдено, что в крови людей максимальное содержание вещества в случае применения микронизата, с размерами частиц < 5 мкм, на 40% выше, чем в случае обычной. При этом и максимум концентрации сдвинулся по времени на 2 часа раньше.
Антикоагуляционное действие фениндиона в значительной степени также определяется размерами частиц: оптимальным считается размер частиц вещества от 10 до 30 мкм. Если таблетированию подвергнуть частицы размером более 30 мкм, то для достижения такого же лечебного эффекта приходится применять большие (двойные) дозы этого антикоагулянта.
Для кальциферола установлено, что всасывание его в организм и лечебное действие наступает только в случае измельчения веществ до частиц менее 10 мкм.
Однако, способствуя растворению и всасыванию лекарственных веществ, микронизирование может ускорить процессы их выведения из организма (эритромицин, левомице-тин) или усиливать побочные нежелательные эффекты препара-тов (дифенилгидантоин). Так, резорцин в мазях для накожного нанесения вводится в виде суспензии, а не раствора (молекуляр-ного состояния), т.к. иначе проявятся его токсические свойства.
С увеличением дисперсности резко снижается активность, пенициллина и эритромицина. А при назначении нитрофу-рантиона, в виде микронизата вещество быстро всасывается, создавая высокие концентрации в крови, при этом наблюдаются общие и местные токсические реакции, в т.ч. значительное раздражение слизистых пищеварительного тракта; назначением той же дозы нитрофурантиона в виде крупных кристаллов удается предотвратить указанные побочные реакции.
Поэтому, выбор степени измельчения лекарственных веществ должен осуществляться в обязательном порядке с учетом влияния данного фактора на их фармакокинетику.
Из других поверхностных свойств лекарственных веществ особого внимания с точки зрения влияния на фармакотерапев-тическую эффективность заслуживает полиморфизм. Как известно, многие вещества обладают способностью образовы-вать несколько кристаллических модификаций, различающихся показателями кристаллической структуры и, как следствие этого, характеризующиеся различными физическими свойства-ми.
Это явление носит название полиморфизм. Более 1/3 всех органических веществ существует в 2-х и более кристал-лических модификациях.
Распространенность явлений полиморфизма среди лекарственных веществ несомненна и весьма значительна. К ним следует отнести в первую очередь салицилаты, сульфаниламиды, препараты барбитуратов, антибиотиков, стероидов и многих других.
Способность вещества, склонного к полиморфизму, образовывать различные кристаллические модификации зависит от многих условий: способов получения, характера очистки и перекристаллизации, методов сушки и измельчения, наличия тех или иных сопутствующих веществ; хорошими условиями для аналогичных полиморфных превращений являются также: влажная грануляция и прессование при таблетировании, дражирование, получение пилюльной массы, расплавление основ и их охлаждение, суспендирование или растворение лекарственных веществ в гидрофильных или эмульсионных основах и т.д.
Обычно менее стабильные кристаллические модификации веществ характеризуются большей растворимостью и лучшей всасываемостью, а поэтому всегда являются наиболее эффектив-ными в терапевтическом отношении. Так, b-форма преднизо-лона растворяется в 14 раз быстрее a (стабильной)-формы этого вещества и обеспечивает в 1,7 раза более быстрое поступление в кровь стероидов.
Взвесь микрокристаллической модификации инсулина действует почти в 2 раза дольше, чем аморфная его модифика-ция.
Хлорамфеникол (левомицетин) существует в 3-х кристал-лических (А,В,С) и одном аморфном состояниях, из которых только форма В отличается высокой активностью.
Метастабильная форма рибофлавина растворяется в концентрации 1200 мг/л (0,12%), а стабильная - только 60 мг/л (0,006 %).
С биофармацевтической точки зрения изучение явления полиморфизма лекарственных и вспомогательных веществ, начатое сравнительно недавно в фармацевтическом аспекте, является обязательным и представляет собой исключительно плодотворную область современного лекарствоведения. Исследование полиморфизма лекарственных веществ и использование его с целью повышения эффективности лекарственной терапии является важнейшим разделом биофармации.
Вспомогательные вещества.
Биофармация впервые дала научное обоснование применению вспомогательных веществ в производстве лекарств.
В биофармацевтическом эксперименте установлено многообразное взаимодействие лекарственных и вспомогательных веществ. Обычно все типы связей между активными субстанциями и вспомогательными веществами классифицируют на следующие: водородные связи, соединения включения, cилы Ван-дер-Ваальса, ковалентные связи. В лекарственных формах, в каждом конкретном случае наличия тех или иных лекарственных и вспомогательных веществ, обычно наблюдается или доминируют различные типы связей, характеризующие тот или иной вид взаимодействий
В зависимости от характера взаимодействия вспомога-тельных и лекарственных веществ можно ожидать следующих явлений:
а) взаимодействие вспомогательных и лекарственных веществ практически не влияют на скорость и полноту всасывания лекарственных веществ;
б) изменяется качество всосавшегося вещества: одновре-менно образующиеся продукты деструкции лекарственных веществ могут обусловить, особенно при систематическом назначении, возникновение не характерных для основного вещества эффектов. Уровень лечебного действия пpeпарата будет соответствовать ожидаемому;
в) образующиеся комплексы, нестехиометрические соеди-нения и так далее, как результат взаимодействия лекарственных и вспомогательных веществ могут облегчить высвобождение вещества из лекарственной формы, повысить его растворимость, способствовать всасыванию или наоборот - вызовут ингибиро-вание вышеназванных процессов: замедлят высвобождение и всасывание лекарственных веществ.
Поэтому недопустимо применение какого бы то ни было вспомогательного вещества вместе с лекарственным веществом в виде определенной лекарственной формы без специального исследования возможных видов их взаимодействия и влияния взаимодействия лекарственного и вспомогательного вещества на фармакокинетику вещества в конкретной лекарственной форме.
Это - одна из главных задач биофармации, важность и масштабность которой позволяет иногда называть биофармацию учением о фармакокинетической функции вспомогательных веществ. И действительно, доказано, что в присутствии вспомогательных веществ очень часто меняется скорость и полнота всасывания многих лекарственных веществ.
Примеры:
Так, фенобарбитал (в форме суппозиториев, таблеток) в присутствии ПЭГ-400 образует прочный нерастворимый комплекс и поэтому не всасывается и не оказывает терапевтического действия (другие барбитураты не взаимодействуют с ПЭО).
В присутствии поливинилпирролидона (ПВП) резко уменьшается антимикробная активность левомицетина. В то же время ПВП повышает скорость всасывания и эффективность салициламида, преднизолона, гризеофульвина.
Таблица 2.1