Основные компоненты клеточной стенки растений
Химические компоненты клеточной стенки обычно разделяют на основные, инкрустирующие и откладывающиеся на ее поверхности (адкрустирующие). К основным химическим компонентам относятся целлюлоза, гемицеллюлоза, пектиновые вещества, белки. Компонентами, инкрустирующими клеточную стенку, являются лигнин и суберин. На поверхности клеточной стенки могут откладываться кутин, воск. Кроме того, клеточные стенки содержат силикаты и карбонаты кальция.
Самыми распространенными компонентами возобновляемого растительного сырья являются целлюлоза, лигнин и гемицеллюлозы (полиозы), которые составляют, соответственно, 40; 30 и 26% его общей массы. Целлюлоза является армирующим материалом клеточных стенок, образующим упорядоченные нитевидные структуры (фибриллы). Лигнин и гемицеллюлозы представляют аморфные биополимеры сетчатого или разветвленного строения и играют роль связующих (наполнителей).
Строение этих веществ, их межмолекулярное взаимодействие определяют свойства растительных субстратов в целом и особенности поведения их при переработке.
Целлюлоза
Целлюлоза является самым распространенным веществом на Земле, это скелет клеточной стенки растений. Лучше всего изучена структура целлюлозы хлопкового волокна и волокон, синтезируемых некоторыми бактериями, водорослями, а также моллюсками, так как в них целлюлоза встречается в наиболее чистой форме. В древесине она встречается только в виде композита с другими биополимерами, откуда ее сложно извлечь без частичного разрушения.
В химическом отношении целлюлоза представляет собой полисахарид, макромолекулы которого построены из остатков ß-D-глюкозы и представляют собой линейную цепь ангидроглюкопиранозных звеньев, соединенных 1,4-глюкозидными связями (рис.9).
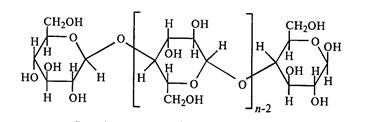
Рис.9. Химическое строение целлюлозы
Это стереорегулярный полимер, в цепи которого стереоповторяющимся звеном служит остаток целлобиозы. Суммарная формула целлюлозы имеет вид – (С6Н10О5)n или [С6Н7О2(ОН)3]n. В мономерном звене целлюлозы содержатся три спиртовых гидроксильных группы, из которых одна первичная – СН2ОН, а две у С2 и С3 вторичные – СНОН. Концевые звенья отличаются от остальных звеньев цепи. Одно концевое звено (у С4) имеет дополнительный, свободный вторичный спиртовый гидроксил. Концевое звено (у С1) содержит свободный гликозидный (полуацетальный) гидроксил и может существовать в двух таутомерных формах – циклической (полуацетальной) и открытой (альдегидной). Концевая альдегидная группа придает целлюлозе редуцирующую (восстанвливающую) способность. По способности целлюлозы к реакции восстановления можно охарактеризовать длину ее цепей, свойственную данному виду растений.
В глюкозном остатке принято выделять гидрофильную и гидрофобную плоскости, в зависимости от того, сколько ОН- и СН-групп ей соотвествуют. Это важно при изучении взаимодействия глюкозного остатка с остатками ароматических аминокислот при ферментативном расщеплении молекулы целлюлозы в активном центре фермента.
Благодаря тому, что гидроксильные группы у первого и четвертого атомов глюкозы отличаются расположением относительно плоскости кольца, соседние остатки глюкозы в полимерной цепи оказываются повернутыми по отношению друг к другу на 1800. Полимерные цепи стабилизируются за счет водородных связей, образующихся между остатками глюкозы при взаимодействии гидроксильных групп при 6,2,3 углеродных атомов и кислорода кольца. Линейные полимерные цепи соединяются между собой с помощью межмолекулярных водородных связей, которые возникают между атомами кислорода одной цепи и гидроксильными группами при С6 глюкозы другой цепи (рис. 10). В результате таких взаимодействий формируются прочные волокна. Гибкость молекулы целлюлозы определяется возможностью вращения ангидроглюкозных остатков в целлобиозном звене относительно гликозидной связи. Устойчивость линейной конформации целлюлозы определяется, в частности, минимальным отталкиванием С1-H и C4-H.
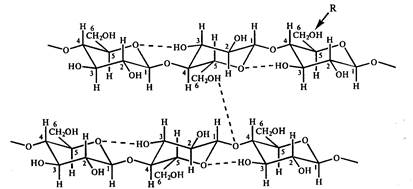
Рис. 10. Схематическое изображение системы водородных связей между остатками глюкозы в целлюлозе. R- центр возможной химической модификации целлюлозы. Так, в метилцеллюлозе, ацетилцеллюлозе и карбоксиметилцеллюлозе R= CH3, СОСН3, СН2СООNa соответственно
Молекула глюкозы представлена в конформации кресла, при которой атомы С2, С3, С5 и О5 лежат в одной плоскости, а атомы С1 и С4 - по разные стороны от нее. Остаток глюкозы может принимать также и энергетически менее выгодные конформации, которые по степени устойчивости располагаются в следующем порядке: скошенная конформация, конформация лодки (или ванны) и наименее выгодная конформация полукресла, при которой в одну плоскость попадают сразу 5 атомов 6-членного пиранозного цикла. Способность ангидроглюкозного звена принимать в молекуле целлюлозы помимо наиболее устойчивой менее устойчивые конформации (например, конформацию лодкиили конформациюполукресла) имеет важное значение при нарушении упорядоченной надмолекулярной структуры целлюлозы, а также при ферментативном гидролизе гликозидных связей в ее молекуле.
Элементарные волокна (мицеллы) целлюлозы состоят из 100-200 полимерных цепей, соединенных водородными мостиками. Эти волокна в клеточной стенке располагаются параллельно друг другу и группируются таким образом, что образуются пучки овальной формы –микрофибриллы. Около 10 мицелл образуют микрофибриллу диаметром 0,025 нм (рис.11).
Каждый пучок имеет центральную кристаллическую часть – ядро, в которой цепи упакованы настолько плотно, что в них с большим трудом проникают даже молекулы воды. Вокруг ядра располагается паракристаллический кортекс с менее упорядоченной структурой. Эти менее упорядоченные участки, называемые также аморфными,обычно составляют около 15% микроструктуры целлюлозы. Микрофибриллы могут объединяться в отдельные группы или слои – макрофибриллы – толщиной 0,4-0,5 мкм, видимые в световой микроскоп. Диаметр и степень кристалличности микрофибрилл довольно сильно варьируют в зависимости от вида растения и физиологического состояния клетки.

Рис.11. Модель строения микрофибриллы:а) поперечный разрез микрофибриллы с мицеллами и межмицелярными промежутками; б) схема расположения целлюлозы
Для древесной целлюлозы с индексом упорядоченности 50-70% поперечные размеры кристаллита не превышают 4х6 нм. По данным электронной микроскопии средние размеры в поперечнике могут составлять 1,5-2х2,5-3,5 нм. От 40 до 80% молекул при таких размерах расположено на поверхности кристаллита, где возможны их большая гидратация, нарушение дальнего порядка в структуре водородных связей, а также более сильное влияние химических воздействий.
Природная целлюлоза является полидисперсной, число глюкозных остатков в молекуле целлюлозы и, следовательно, длина самих молекул могут резко различаться в клеточных оболочках различных растений. Так, для целлюлозы волосков хлопчатника степень полимеризации первичной клеточной стенки равна 2-6 тысяч, вторичной – 13-14 тысяч, для целлюлозы Acetobacter xylinum- 2-6 тысяч, для древесины- 8-10 тысяч. Максимальная экспериментально установленная молекулярная масса целлюлозы льна составляет 6 000 000. В связи с тем, что степень полимеризации является усредненным показателем, наиболее точной характеристикой является кривая распределения молекул целлюлозы по длине (молекулярно-массовое распределение). Однако эту характеристику получить трудно и поэтому применяют усредненные характеристики: среднечисловую (DPn) и средневесовую (DPw) степени полимеризации. Среднечисловая степень полимеризации равна общему числу ангидроглюкозных остатков в образце целлюлозы, деленному на общее число молекул полимера. Для ее определения в образце полисахарида оттитровывают восстанавливающие концы. Средневесовую степень полимеризации целлюлозы определяют растворением образца целлюлозы в щелочном комплексе меди, цинка, кобальта или кадмия с этилендиамином, либо комплексе LiCl с N,N’-диметилацетамидом. Отношение DPw/DPn равно единице только у монодисперсных полимеров.
Для целлюлозы древесины ели, сосны, березы, и осины средневесовая степень полимеризации составляет 12000, при этом длина такой молекулы в вытянутом состоянии достигает почти 6 мкм, что в 6000 раз больше чем ее диаметр. Столь длинная и регулярно построенная молекула уложена определенным образом. Способ укладки определяет надмолекулярную структуру биополимера, основой которой являются внутри- и межмолекулярные водородные связи, образуемые целлобиозными звеньями. Исследование способа укладки и типов водородных связей в макромолекуле целлюлозы осуществляют с помощью конформационного анализа, дифракции (малоугловое рентгеновское рассеяние, рассеяние электронов), ИК-спектроскопии и ЯМР. Несмотря на значительные достижения в этой области вопрос о способах укладки молекул целлюлозы окончательно не решен.
Целлюлоза нерастворима в воде и органических растворителях, в химическом отношении инертна, механически очень прочна. Вода между близко расположенными, но не взаимодействующими непосредственно поверхностями кристаллитов, структурируется. Удаление гидратной воды, например в результате сушки способствует сближению изначально не контактировавших целлюлозных молекул и образованию между ними разнообразных типов водородных связей, которые не разрушаются при регидратации. Повышение степени кристалличности в процессе увлажнения исследователи связывают с проникновением воды из менее упорядоченных в более упорядоченные области. В результате наблюдается уменьшение абсолютных размеров кристаллитов и увеличение степени общей упорядоченности. Полагают, что вода при этом действует по принципу «молекулярной смазки», упрощая неупорядоченным фрагментам молекул достройку упорядоченной структуры путем кооперативного взаимодействия с кристаллической «затравкой». Замещение полярных групп целлюлозы, например, карбоксиметилом, ведет к нарушению молекулярной регулярности, способствует возникновению множества водородных связей с водой и делает целлюлозу растворимой.
Устойчивость целлюлозы к расщеплению, как в природных, так и в лабораторных условиях обусловлена не столько особенностями b-1,4- глюкозидной связи, сколько кристаллической структурой целлюлозы и особой «упаковкой» ее молекул в биологических структурах.
Во внутренние структуры фибрилл целлюлозы не могут проникать целлюлолитические ферменты. Они действуют на их поверхности. Число гликозидных связей, доступных действию ферментов, зависит в значительной мере от степени набухания целлюлозы. Увеличение степени набухания можно достичь за счет предобработки – пропаривания, размалывания, обработки ультразвуком и т.д. Набухание всего волокна увеличивают минеральные кислоты и щелочи в высоких концентрациях, так как они способны разрывать водородные связи и проникать в кристаллические участки. Сравнительно легко поддаются действию кислот и щелочей аморфные участки целлюлозы.
При действии на целлюлозу концентрированных растворов щелочи изменяются ее физико-химические и структурные свойства: отмечается интенсивное набухание, изменяется степень кристалличности. Высокомолекулярная фракция целлюлозы, нерастворимая в 17,5%- ной NaOH, называется a- целлюлозой. Хлопок состоит преимущественно из a- целлюлозы, а другие растения и древесина содержит преимущественно b- целлюлозы, растворимые в концентрированном растворе щелочи .
Микрофибриллы погружены в аморфный матрикс оболочки, который представляет собой сложную смесь полимеров, среди которых преобладают полисахариды различной молекулярной массы. Предполагается, что на поверхности всех микрофибрилл имеется слой молекул ксилоглюкана, сорбированный за счет водородных связей. Лигнин и гемицеллюлозы заполняют пространство между элементарными фибриллами целлюлозы. Таким образом, одревесневшее вещество является полимерной структурой, состоящей из целлюлозной арматуры, погруженной в лигноцеллюлозную матрицу.
Целлюлоза и гемицеллюлозы характеризуются различной кинетикой образования, что свидетельствует, по-видимому, о разных местах их синтеза. Синтез целлюлозы происходит, по-видимому, вне клетки на поверхности цитоплазматической мембраны при участии ГДФ или УДФ. Донорами гликозильных групп являются нуклеозиддифосфаты сахаров, которые образуются из глюкозы и сахарозы разными путями. Например, из нуклеозидтрифосфатов и сахар-1-фосфатов с участием пирофосфорилазы. Гликозильные остатки присоединяются к остаткам сахаров у невосстанавливающих концов растущей цепи. Между первым углеродом «добавляемого» остатка и гидроксильной группой четвертого углеродного атома концевого остатка при участии синтетазы возникает гликозидная связь.
 n(Нуклеозиддифосфатсахар) + (сахар)n синтетаза n (Нуклеозиддифосфат) + (сахар)n+1
n(Нуклеозиддифосфатсахар) + (сахар)n синтетаза n (Нуклеозиддифосфат) + (сахар)n+1
В клеточной стенке обнаружены ферменты синтеза целлюлозы и гранулы диаметром 8 нм, представляющие, по-видимому, мультиферментные комплексы, которые располагаются на наружной поверхности плазмалеммы и в матриксе стенки. Целлюлозосинтетаза (Е) в плазмалемме связана с активирующим белком Р, способным связывать ГТФ и переходить в активную форму с образованием комплекса Р-Е-ГТФ.
В процессе синтеза целлюлозы происходит образование не только одиночных цепей целлюлозы, но и формирование микрофибрилл целлюлозы. Такой синтез осуществляется, вероятно, при участии многих молекул целлюлозосинтетаз, сосредоточенных в отдельных местах плазмалеммы, причем целлюлозосинтетазы состоят из множества субъединиц, каждая из которых отвечает за синтез одиночной цепи глюкана. На внутренней стороне мембран были найдены «розетки» из шести белковых глобул. Розетки секретируются в плазмолемму с помощью эндомембранной системы везикул. На основании особенностей структурной связи розеток, терминальных комплексов и образующихся микрофибрилл целлюлозы возникло предположение о механизме формирования микрофибрилл в комплементарной трансмембранной структуре: розетки – терминальный комплекс – растущий конец микрофибриллы. С концом вновь синтезированной микрофибриллы связан терминальный комплекс, а розетки являются местом связывания предшественников целлюлозы и выведения «носителей» остатков глюкозы.
Одиночные розетки вместе с соответствующими, терминальными комплексами отвечают за синтез беспорядочно ориентированных микрофибрилл первичной клеточной стенки (рис.12), а ориентированная совокупность розеток до 175 штук на отдельных участках плазмалеммы определяет образование параллельно расположенных микрофибрилл вторичной клеточной стенки (рис.13).

Рис.12.Микрофибриллы целлюлозы в период образования
первичной клеточной стенки:1 — двойной слой липида; 2 — микрофибрилла; 3 — внешняя поверхность плазмалеммы; 4 — розетка
Каждая розетка формирует микрофибриллу диаметром 5 нм. Расстояние между рядами розеток в плазмалемме соответствует рас-стоянию между микрофибриллами в клеточной стенке. Тонкие микрофибриллы содержат около 50 полиглюкановых цепей. Эти микрофибриллы образуют фибриллы вторичной клеточной стенки, диаметр которых может достигать 28 нм. Целлюлоза в отличие от крахмала является труднометаболируемым соединением. Ее усвояемость определяется происхождением, содержанием в пищевом рационе, характером предварительной обработки и колеблется в среднем от 6 до 23%. Так, перевариваемость целлюлозы пшеничных отрубей порядка 15%.

Рис. 13.Микрофибриллы целлюлозы в период образования
вторичной клеточной стенки: 1 — розетка; 2 — двойной слой липида
В пищевых волокнах целлюлоза составляет примерно одну треть. Ее эффективное разложение происходит в результате симбиотического взаимодействия различных микроорганизмов толстого кишечника и их целлюлолитических ферментов. В пищеварительном тракте целлюлоза стимулирует деятельность кишечника, усиливая его перистальтику, нормализует деятельность кишечной микрофлоры, сорбирует стерины, препятствует их всасыванию и способствует выделению холестерина. Широкое применение в качестве добавки к пище нашла микрокристаллическая целлюлоза (МКЦ) – не волокнистая порошкообразная модификация природной целлюлозы. Она не только снижает калорийность пищи, но и является ее загустителем и диспергатором, улучшающим качество блюд.