Системы с открытой цепью сопряжения
π,π-Сопряжение.Простейшим представителем π,π-сопряженных систем с углеродной цепью служит бутадиен-1,3 (рис. 2.6, а). Атомы углерода и водорода и, следовательно, все σ-связи в его молекуле лежат в одной плоскости, образуя плоский σ-скелет. Атомы углерода находятся в состоянии sр2-гибридизации. Негибридизованные р-АО каждого атома углерода расположены перпендикулярно плоскости σ-скелета и параллельно друг другу, что является необходимым условием для их перекрывания. Перекрывание происходит не только между р-АО атомов С-1 и С-2, С-3 и С-4, но и между р-АО атомов С-2 и С-3, в результате чего образуется охватывающая четыре атома углерода единая π-система, т. е. возникает делокализованная ковалентная связь (см. рис. 2.6, б).
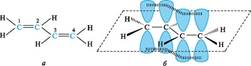
Рис. 2.6.Атомно-орбитальная модель молекулы бутадиена-1,3
Это отражается в изменении длин связей в молекуле. Длина связи С-1-С-2, а также С-3-С-4 в бутадиене-1,3 несколько увеличена, а расстояние между С-2 и С-3 укорочено по сравнению с обычными двойными и одинарными связями. Другими словами, процесс делокализации электронов приводит к выравниванию длин связей.
Углеводороды с большим числом сопряженных двойных связей распространены в растительном мире. К ним относятся, например, каротины, обусловливающие окраску моркови, томатов и т. п.
Открытая система сопряжения может включать и гетероатомы. Примером открытых π,π-сопряженных систем с гетероатомом в цепи могут служить α,β-ненасыщенные карбонильные соединения. Например, альдегидная группа в акролеине CH2=CH-CH=O явля- ется участником цепи сопряжения трех sр2-гибридизованных атомов углерода и атома кислорода. Каждый из этих атомов вносит в единую π-систему по одному р-электрону.
pn-Сопряжение.Этот вид сопряжения чаще всего проявляется в соединениях, содержащих структурный фрагмент -CH=CH-X, где X - гетероатом, имеющий неподеленную пару электронов (прежде всего O или N). К ним относятся, например, виниловые эфиры, в молекулах которых осуществляется сопряжение двойной связи с р-орбиталью атома кислорода. Делокализованная трехцен- тровая связь образуется путем перекрывания двух р-АО sр2-гиб- ридизованных атомов углерода и одной р-АО гетероатома с парой и-электронов.

Образование аналогичной делокализованной трехцентровой связи имеется в карбоксильной группе. Здесь в сопряжении участвуют π-электроны связи С=О и n-электроны атома кислорода группы ОН. К сопряженным системам с полностью выровненными связями и зарядами относятся отрицательно заряженные частицы, например ацетат-ион.

Направление смещения электронной плотности обозначается изогнутой стрелкой.
Существуют и другие графические способы отображения результатов сопряжения. Так, структура ацетат-иона (I) предполагает, что заряд равномерно распределен по обоим атомам кислорода (как показано на рис. 2.7, что соответствует действительности).

Структуры (II) и (III) применяются в теории резонанса. Согласно этой теории реальная молекула или частица описывается набором определенных так называемых резонансных структур, которые отличаются друг от друга только распределением электронов. В сопряженных системах основной вклад в резонансный гибрид вносят структуры с различным распределением π-электронной плотности (двусторонняя стрелка, связывающая эти структуры, является специальным символом теории резонанса).
Предельные (граничные) структуры в действительности не существуют. Однако они в той или иной степени «вносят вклад» в реальное распределение электронной плотности в молекуле (частице), которую представляют в виде резонансного гибрида, получающегося путем наложения (суперпозиции) предельных структур.
В ρ,π-сопряженных системах с уг- леродной цепью сопряжение может осуществляться при наличии рядом с π-связью атома углерода с негибридизованной р-орбиталью. Такими системами могут быть промежуточные частицы - карбанионы, карбокатионы, свободные радикалы, например, аллильной структуры. Свободнорадикальные аллильные фрагменты играют важную роль в процессах пероксидого окисления липидов.
В аллил-анионе CH2=CH-CH2 sр2-гибридизованный атом углерода С-3 поставляет в общую сопряженную систему два электрона, в аллильном радикале CH2=CH-CH2+ - один, а в аллильном карбокатионе CH2 =CH-CH2+ не поставляет ни одного. В результате при перекрывании p-АО трех sp2-гибридизованных атомов углерода образуется делокализованная трехцентровая связь, содержащая четыре (в карбанионе), три (в свободном радикале) и два (в карбокатионе) электрона соответственно.

Формально атом С-3 в аллил-катионе несет положительный заряд, в аллильном радикале - неспаренный электрон, а в аллил-анионе - отрицательный заряд. В действительности в таких сопряженных системах имеется делокализация (рассредоточение) электронной плотности, что приводит к выравниванию связей и зарядов. Атомы С-1 и С-3 в этих системах равноценны. Например, в аллил-катионе каждый из них несет положительный заряд +1/2 и связан «полуторной» связью с атомом С-2.
Таким образом, сопряжение приводит к существенному различию в распределении электронной плотности в реальных структурах по сравнению со структурами, изображаемыми обычными формулами строения.