Клиническая картина дизентерийной амёбы.
Дизентерийная, или гистологическая, амеба вызывает у человека заболевание амебную дизентерию, или амебиаз. В толстом кишечнике образуются множественные язвы. Заболевание бывает различной тяжести и начинается остро или постепенно. Беспокоят боли внизу живота, частый жидкий стул красно-бурого цвета из-за примеси крови и слизи (испражнения при этом нередко напоминают мясные помои). Температура тела обычно нормальная. Заболевание может тянуться с периодическими обострениями несколько лет. В тяжелых случаях развиваются анемия, истощение.
Тканевая форма амебы из кишечных язв может заноситься с кровью в печень, легкие, мозг и другие органы, вызывая там абсцессы. Эти осложнения без своевременного лечения могут закончиться летально.
Диагноз.
Для выявления дизентерийных амеб или их цист исследуют испражнения. С этой целью на предметных стеклах готовят нативные мазки испражнений в капле изотонического раствора хлорида натрия и капле раствора Люголя.
В нативном мазке (Х400) наблюдают подвижные вегетативные формы. В растворе Люголя хорошо видны цисты. В затруднительных случаях препараты окрашивают по Гейденгайну.
Для исследования нужно брать свежевыделенные испражнения, так как амебы быстро, в течение 10-20 мин, теряют подвижность, что делает невозможной достоверную диагностику. Цисты амеб можно обнаружить и в оформленном кале даже при хранении его до исследования в течение нескольких часов. Если выявлены только просветные формы или цисты, то ставить диагноз амебной дизентерии нельзя, так как они могут быть признаком только носительства. Поэтому при клинических показаниях, т. е. подозрении на возможность заболевания амебиазом, проводят многократные исследования, назначают солевое слабительное, ибо большие вегетативные или тканевые формы можно обнаружить только в жидких или полужидких фекалиях. При этом исследуют в первую очередь патологические примеси (комочки слизи).
Следует учитывать, что в острой стадии болезни с фекалиями чаще выделяются только тканевые, вернее, большие вегетативные формы, а в периоде выздоровления — просветные формы и цисты.
При невозможности немедленного исследования испражнений допускается их консервация. Консервированный материал можно изучить через несколько дней или направить на консультацию. Простейшие в консерванте окрашиваются и теряют подвижность, что в определенной степени затрудняет лабораторное исследование.
При подозрении на амебный абсцесс микроскопируют содержимое, полученное во время операции или пункции. Амебы при этом чаще обнаруживаются в материале, взятом на границе здоровой и пораженной тканей, на внутренней поверхности капсулы абсцесса, чем непосредственно в гное. Предшествовавшая антибиотико- или химиотерапия могут обусловить отрицательный результат такого исследования.Разработаны методы серологической диагностики амебиаза (РГА, РИФ, РЭМА).
Профилактика.
Распространение и механизм передачи амебной и бактериальной дизентерии имеют много общего, поэтому профилактические мероприятия также сходны. Больных госпитализируют. Выписка допускается после получения 3 отрицательных анализов кала, проведенных в течение 1нед. При неустойчивом стуле у реконвалесцентов, а также при необходимости выявления носителей среди здоровых лиц проводят не менее 6 анализов в течение 2 нед.
После выписки переболевшие подлежат наблюдению в кабинетах инфекционных заболеваний поликлиник не менее года с периодическим исследованием кала. Носителей санируют.
Фекалии, загрязненное белье обезвреживают 3% раствором лизола. Обычное хлорирование воды на цисты не действует. Быстрый эффект дает только кипячение.
Носительство дизентерийной амебы регистрируется повсеместно, однако заболевания наблюдаются чаще всего в Средней Азии, на Кавказе и Дальнем Востоке. Возможны завозные случаи.
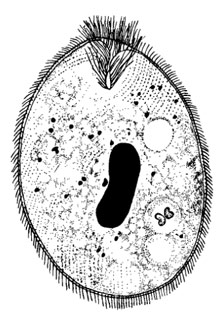 Балантидий
Балантидий
Балантидий (Balantidium coli). Слово балантидий происходит от греческого balantidium - мешок. Балантидий самый крупный представитель паразитических простейших человека.
Строение балантидия.
Вегетативная форма балантидия вытянута, чаще яйцеобразная. Длина балантидия 30 - 150 мкм, ширина 30 - 100 мкм. С помощью многочисленных ресничек балантидии активно двигаются, нередко вращаясь при этом вокруг своей оси. Питаются балантидии различными пищевыми частицами, включая бактерии, грибы, форменные элементы крови, для заглатывания которых служит цитостом (клеточный рот). Цитоплазма балантидия содержит пищеварительные и две пульсирующие выделительные вакуоли. Ядро балантидия (макронуклеус, или большое ядро, так как имеется еще и большое ядрышко, или микронуклеус) у живых представителей иногда видно и без окраски в виде светового пузырька бобовидной формы. При окраске по Гейденгайну оно имеет черный цвет. В фекалиях сохраняются в течение 3 часов.
Цисты балантидия округлой формы с толстой оболочкой размером 50 - 60 мкм. В растворе Люголя окраска равномерная, коричнево - желтая. Цитоплазма цисты балантидия однородная.
Жизненный цикл балантидия.
Балантидии обитают в кишечнике свиней, для которых малопатогенны. С испражнениями свиней цисты балантидия выделяются в окружающую среду, где могут сохраняться несколько недель. Попадая с загрязненной водой или пищей в рот цисты балантидия в толстом кишечнике человека дают начало вегетативной стадии с последующим их размножением. Человек, больной или носитель, только в редких случаях может быть источником распространения балантидиев, так как у человека цисты образуются редко и в незначительном количестве, а вегетативными стадиями заразиться почти невозможно.
Клиническая картина.
Балантидии могут внедряться в слизистую оболочку толстого кишечника и вызывать воспалительно - язвенный процесс. В результате развивается балантидиаз. У больного наблюдаются понос, боли в животе, интоксикация, рвота, головные боли, в испражнениях - слизь, кровь. Болезнь может протекать в субклинической, острой или хронической формах, в ряде случаев приводя к летальному исходу.
Диагноз.
Для обнаружения балантидиев каплю свежевыделенных испражнений помещают в изотонический раствор натрия хлорида на предметном стекле и исследуют под малым увеличение микроскопа. Балантидии хорошо видны благодаря крупным размерам и активному движению. Выделяются балантидии периодически, поэтому исследование при отрицательном результате необходимо повторять несколько раз. В некоторых случаях назначают солевое слабительное. У носителей обнаруживают только единичные цисты балантидиев.
Профилактика балантидиаза.
Соблюдение правил личной гигиены, особенно при уходе за свиньями. Охрана от загрязнения воды и пищи. Балантидиаз чаще регистрируется в южных районах, хотя спорадически он выявляется повсеместно, особенно там, где развито свиноводство.

Рис. 1.6. Балантидий.
а — вегетативная форма (с окраской по Гейденгайну); б — циста (Е. Н. Смирнова)
Виды лейшманий.
Для человека патогенны несколько видов лейшманий. Leishmania tropica (впервые обнаружены в 1897 г. русским врачом и ученым П. Ф. Боровским), вызывает антропонозный (городской) кожный лейшманиоз; Leishmania major — возбудитель зоонозного (пустынного) кожного лейшманиозa; Leishmania braziliensis — встречается в Южной Америке и вызывает кожно-слизистый (американский) лейшманиоз; Zeishmania donovani — вызывает висцеральный, или внутренний, лейшманиоз (индийский кала-азар), возбудителя этого вида впервые обнаружили в селезенке больных людей Лейшман и Донован (1900—1903), в честь которых он и получил название; Leishmania infantum — возбудитель висцерального (средиземноморского) лейшманиоза.
Строение лейшманий.
Лейшмании проходят две стадии развития: безжгутиковую и жгутиковую. Безжгутиковая форма овальная, длиной 2—6 мкм. Ядро округлое, занимает до 1/3 клетки. Рядом с ним находится кинетопласт, имеющий вид короткой палочки. При окраске по Романовскому цитоплазма голубая или голубовато-сиреневая, ядро - красно-фиолетовое, кинетопласт окрашивается более интенсивно, чем ядро.
Встречаются в теле позвоночного хозяина (человек, собака, грызуны), паразитируют внутриклеточно в макрофагах, клетках костного мозга, селезенки, печени. В одной пораженной клетке может содержаться до нескольких десятков лейшманий. Размножаются простым делением.
Жгутиковая форма подвижная, жгутик длиной 15—20 мкм. Тело удлиненное веретенообразное, длиной до 10-20 мкм. Деление продольное. Развиваются в теле безпозвоночного хозяина— переносчика (москита) и в культуре на питательных средах.
Жизненный цикл.

Лейшманиозы входят в группу трансмиссивных инфекций, переносчиками служат мелкие кровососущие насекомые — москиты. Москиты заражаются при кровососании на больных людях или животных. В первые же сутки заглоченные безжгутиковые паразиты превращаются в подвижные жгутиковые формы, начинают размножаться и спустя 6—8 дней скапливаются в глотке москита.
При укусе человека или животного зараженным москитом подвижные лейшмании из его глотки проникают в ранку и затем внедряются в клетки кожи или внутренних органов в зависимости от вида лейшманий. Здесь происходит их превращение в безжгутиковые формы.
Источники инфекции при лейшманиозах многообразны: при индийском висцеральном лейшманиозе (кала-азаре) — больные люди; при средиземноморском висцеральном лейшманиозе — шакалы, лисы, дикобразы, собаки (роль последних доказали советские ученые Н.И. Ходукин и М.С. Софиев).
У собаки, пораженной висцеральным лейшманиозом развиваются истощение, язвы на голове и коже тела, шелушение кожи, особенно вокруг глаз. У молодых собак заболевание может протекать остро и даже приводить к гибели, у взрослых животных течение болезни нередко более стертое или бессимптомное (носительство).
В СНГ висцеральный лейшманиоз встречается спорадически в Средней Азии, на юге Казахстана, в Закавказье и Крыму.
При кожном лейшманиозе источником инфекции являются или больные люди, или дикие грызуны — большая и краснохвостая песчанки, обитатели пустынь (при зоонозной форме, «пендинской язве», что в 1937- 1940 гг. доказал Н. И. Латышев).
Зоонозный кожный лейшманиоз встречается в Туркмении и Узбекистане, на юге Казахстана.
Клиническая картина.
Висцеральным (средиземноморским) лейшманиозом чаще заболевают дети. После инкубационного периода длительностью от нескольких недель до нескольких месяцев у заболевшего повышается температура тела, появляются вялость, адинамия, бледность, исчезает аппетит. Увеличиваются селезенка и печень, вследствие чего заметно выступает живот. Развиваются анемия и истощение больного.
Заболевание тянется несколько месяцев и при отсутствии специфического лечения обычно заканчивается смертью.
При кожном лейшманиозе после инкубационного периода (1—2 мес) в местах укусов москитов появляются небольшие бугорки буровато-красноватого цвета, средней плотности, обычно малоболезненные. Бугорки постепенно увеличиваются и затем изъязвляются через 3—6 нед при антропонозной форме и через 1—3 нед при зоонозной. Возникают язвы с отеком окружающей ткани, воспалением и увеличением лимфатических узлов.
Процесс тянется несколько месяцев, при антропонозной форме — больше года, заканчиваясь выздоровлением. На месте язв остаются рубцы. После перенесенного заболевания формируется стойкий иммунитет.
Диагноз.
Окончательный диагноз висцерального лейшманиоза ставят на основании обнаружения лейшманий при микроскопии мазков костного мозга, окрашенных по Романовскому, с иммерсионным объективом. Для получения костного мозга пункцию грудины, гребешка подвздошной кости или верхней части большеберцовой кости производит врач.
В препарате леишмании могут находиться группами или поодиночке, внутри или вне клеток.
При кожном лейшманиозе материал получают поскабливанием скальпелем нераспавшихся бугорков или инфильтрата по краю язв до появления серозно-кровянистой жидкости. Из соскоба готовят мазки, красят по Романовскому и исследуют с иммерсионным объективом.
Лейшмании легко обнаруживаются на начальных стадиях изъязвления. В гнойном отделяемом язвы могут быть обнаружены лишь деформированные и разрушающиеся лейшмании, что затрудняет постановку диагноза. На стадии заживления лейшмании обнаруживаются редко.
В ряде случаев применяют посев материала из кожных поражений или костного мозга на питательную среду которая готовится на агаре с добавлением дефибринированной крови кролика. В положительном случае на 2-10-й день в культуре появляются жгутиковые формы лейшманий.
Профилактика.
При висцеральном лейшманиозе — подворные обходы для раннего выявления больных, уничтожение безнадзорных собак и осмотры ветеринарными работниками собак ценных пород. При зоонозном кожном лейшманиозе — истребление диких грызунов в окрестностях поселков, профилактические прививки.
С целью предупреждения заболеваемости всеми видами лейшманиозов проводят уничтожение москитов, ликвидацию мест выплода, обработку мест пребывания ядохимикатами, а также принимают меры по предохранению людей от укусов москитов (пологи, репелленты).
Трипаносомы
Из рода трипаносом для человека патогенны три вида: Trypanosoma gambiense и Trypanosoma rhodesiense - эти 2 вида трипаносом вызывают африканский трипаносомоз - сонную болезнь и Trypanosoma cruzi — вызывает американский трипаносомоз - болезнь Шагаса.
Строение трипаносом. Тело трипаносом (от греч. trypanon бурав и soma — тело) продолговатое, узкое, имеет жгутики и ундулируюшую мембрану. На спаде паразитемии они становятся короткими, широкими с укороченным жгутом или даже без него. Длина тела трипаносом 17—28 мкм, в средней части находится овальное ядро.
Жизненный цикл трипаносом. Первая часть жизненного цикла проходит в пищеварительном канале мухи цеце, вторая — в организме хозяина. У позвоночных хозяек (человек, домашние и дикие животные) трипаносомы находятся в крови, откуда при укусах попадают в желудок переносчика. Переносчики возбудителей африканского трипаносомоза — кровососущие мухи рода Glossina или мухи цеце, американского трипаносомоза — триатомовые клопы.

Клиническая картина. Трипаносомы из места укуса проникают в кровь, лимфатические сосуды и узлы, в дальнейшем — в спинномозговую жидкость.
У больных повышается температура тела, на коже возникают высыпания.
Для гамбийского типа африканского трипаносомоза (встречается в Центральной и Западной Африке) характерны увеличение лимфатических узлов, особенно шейных, печени и селезенки, а также анемия и слабость. Болезнь длится несколько лет, приводя к поражению центральной нервной системы с характерной сонливостью (менингоэнцефалит). Обычно заканчивается смертью.
Родезийский тип трипаносомоза (встречается в Юго-Восточной Африке) отличается острым течением, длительными периодами лихорадки, быстрым прогрессированием симптомов поражения внутренних органов. Больные без лечения умирают в течение 3—9 месяцев от момента заражения еще до развития второго периода (сонливости).

Болезнь Шагаса - тяжелое заболевание, встречается в Южной и Центральной Африке. Поражает внутренние органы, сердечную мышцу, головной мозг. Повышается температура тела, увеличиваются печень и селезенка. Болезнь Шагаса может протекать в острой и хронической формах, приводя нередко к смерти.
Диагноз. При африканском трипаносомозе возбудителя можно обнаружить в начальном периоде заболевания на месте укуса зараженной мухой цеце, а также в периферической крови (родезийский тип) или пунктате шейных лимфатических узлов (гамбийский тип).
В период проявления симптомов поражения центральной нервной системы паразиты в крови и лимфатических узлах отсутствуют. На этой стадии болезни трипаносом находят в спинномозговой жидкости.
Для обнаружения подвижных трипаносом каплю крови, смешанную с цитратом натрия, пунктат лимфатического узла или спинномозговой жидкости помещают на предметное стекло, накрывают покровным стеклом и микроскопируют.
Исследуют под малым и большим увеличением. Более распространено исследование окрашенных по Романовскому мазков и толстых капель крови. Тело трипаносом окрашивается в голубоватый цвет, ядро и жгутики — в красный. На препарате можно видеть мембрану, соединяющую волнообразно извитой жгутик с краем тела.
При отрицательном результате микроскопии используют более сложный метод — заражения белых мышей исследуемым материалом подкожно или внутримышечно. При этом уже на 2—3-й день в крови появляются паразиты.
При американском трипаносомозе возбудителя обнаруживают в острой стадии болезни в периферической крови в свежих или окрашенных по Романовскому препаратах. Но из-за небольшого количества трипаносом в крови рекомендуется просматривать большое число препаратов. При отрицательном результате исследования применяют метод обогащения. Для этого в шприц с 1 мл 3,8 % раствора нитрата натрия набирают 9 мл крови из вены и смесь центрифугируют 10 мин при 150 об/мин. Жидкость отсасывают, из верхнего слоя осадка готовят нативные или окрашенные препараты и исследуют.
В хронической стадии заболевания трипаносомы в крови встречаются очень редко. В таких случаях заражают белых мышей или морских свинок и производят посевы на питательные среды, применяют серологические методы.
Трипаносома профилактика: личная — прием профилактических лекарственных препаратов. Общественная — уничтожение переносчиков и мест их выплода.
Лямблии
Лямблии (Lamblia intestinalis) впервые описал русский ученый Д. Ф. Лямбль (1859).
Строение лямблии. Существуют лямблии в виде вегетативной формы (трофозоит) и способны образовывать цисты. Вегетативная форма активная, подвижная, грушевидной формы. Передний конец тела закруглен, задний — заострен. Длина паразита 9—18 мкм.
В передней части тела лямблии находится присасывательный диск в виде углубления. Имеет 2 ядра, 4 пары жгутиков. Жгутики, проходя частично в цитоплазме, образуют два хорошо видимых при окраске продольных пучка.
Движение характерное, лямблии все время переворачиваются боком за счет вращательного движения вокруг продольной оси. В препарате при комнатной температуре лямблии быстро погибают. Пищу всасывают всей поверхностью тела. Размножаются лямблии путем продольного деления.
Цисты - неподвижные формы лямблии. Длина 10—14 мкм. Форма лямблии овальная. Оболочка сравнительно толстая, хорошо очерчена, часто в значительной своей части как бы отслоена от тела самой цисты. Этот признак помогает отличить цисту от других сходных образований. В растворе Люголя окрашиваются в желтовато-коричневый цвет. Окрашивание позволяет видеть в зрелой цисте 4 ядра.
Жизненный цикл лямблии. Лямблии обитают в верхнем отделе тонкого кишечника. С помощью присасывательного диска прикрепляются к ворсинкам. В желчном пузыре лямблии не живут, так как желчь на них действует губительно. Частое их обнаружение при дуоденальном зондировании объясняется тем, что лямблии попадают в содержимое со стенок двенадцатиперстной кишки.
Обычно вегетативные формы с испражениями не выделяются, однако при поносах их можно обнаружить в свежевыделенных жидких фекалиях. Лямблии, попадая в нижние отделы кишечника, где условия для них неблагоприятные, превращаются в цисты, которые и выделяются обычно с испражнениями.
Цисты лямблий хорошо сохраняются в окружающей среде, в зависимости от влажности и температуры воздуха — до месяца. При высушивании погибают очень быстро.
Заражение может произойти через загрязненные руки, игрушки, пищу и воду. Цисты лямблий, попадая в кишечник, превращаются там в вегетативные формы. Одна циста образует две вегетативные формы.
Клиническая картина лямблиоза. Лямблии распространены широко, часто встречаются у детей. При массированном заражении могут вызывать механическое раздражение слизистой оболочки кишечника, в определенной степени нарушать всасывание. Лямблии симптомы: могут возникать нерезкие боли в животе, вздутие и урчание, расстройство стула, снижение аппетита, тошнота, иногда боли в правом подреберье. Это заболевание называется лямблиоз. В некоторых случаях лямблии осложняют течение других заболеваний кишечника и желчных путей.
Диагностика лямблиоза. Обнаружить лямблии у зараженного человека обычно можно сравнительно легко. Так, если фекалии оформленные, то в нативном мазке при микроскопии (Х400) обнаруживаются цисты. Параллельно просматривают мазок, окрашенный раствором Люголя.
В свежевыделенных жидких фекалиях и материале, полученном при дуоденальном зондировании, можно обнаружить подвижные вегетативные формы лямблий. Для достоверного диагноза достаточно обнаружить цисты в фекалиях, в связи с чем отпадает необходимость срочного исследования обязательно свежевыделенных испражнений и дуоденального зондирования для нахождения вегетативных стадий лямблий. Однако в ряде случаев сочетание методов копроскопии и дуоденального зондирования повышает частоту выявления лямблиоза. При слабой инвазии применяют метод обогащения. Выделение цист лямблий может происходить нерегулярно, что требует многократных исследований.
Следует отметить, что широкое распространение носительства лямблий нередко вводит в заблуждение и вызывает гипердиагностику лямблиоза. Поэтому при наличии клинической картины поражения желудочно-кишечного тракта или желчных путей необходимо исключить другие возможные причины заболевания, например, провести бактериологические исследования.
ТРИХОМОНАДЫ
В организме человека обитает три вида трихомонад:
- Trichomonas hominis — кишечная трихомонада — в толстом кишечнике;
- Trichomonas tenax — ротовая трихомонада в полости рта;
- Trichomonas vaginalis — мочеполовая трихомонада (влагалищная) — в мочеполовых путях.
Кишечная трихомонада имеет грушевидное тело длиной 8 - 20 мкм. От переднего конца тела отходят обычно 5 жгутиков. С одной стороны тела по всей его длине расположена волнообразная перепонка (ундулирующая мембрана), по наружному краю которой проходит тонкая нить, выступающая свободным концом в виде жгутика. В цитоплазме при окраске видны ядро и осевая нить, или аксостиль.
Движение трихомонады активное, беспорядочное, «суетливое». Наряду с поступательным движением трихомонады вращаются вокруг продольной оси. Мембрану паразита удается заметить только при замедлении движения или при ее остановке в виде периодически пробегающих волн по одной из сторон тела.
Размножается трихомонада путем деления. Цист не образует. Обитает трихомонада в толстом кишечнике человека. В очень больших количествах обнаруживается в жидких испражнениях. В ряде случаев играет определенную роль в развитии или осложнении течения заболеваний толстого кишечника, особенно у детей раннего возраста.
Ротовая трихомонада по построению похожа на кишечную трихомонаду, ее длина 6 - 13 мкм, ундулируюшая мембрана не достигает конца тела. Цист трихомонада не образует.
Патогенное значение ротовой трихомонады не доказано, хотя имеются данные о значительно более частой встречаемости у лиц с различными заболеваниями полости рта и зубов (гингивит, парадонтоз, кариес зубов) и участии этих простейших в поддержании патологического процесса. Трихомонады обнаруживаются в мокроте больных легочными заболеваниями, а также в удаленных хирургическим путем бронхоэктазах и абсцессах легких. Все это указывает на необходимость более широкого применения лабораторных методов исследования с целью выявления ротовых трихомонад в стоматологических и терапевтических медицинских учреждениях.
Ротовых трихомонад обнаруживают при микроскопии нативиых или окрашенных мазков или соскоба ротовой полости (с зубов, десен, из очагов воспаления и нагноения), в бронхиальной слизи и мокроте. Выявляемость увеличивается при использовании метода посева на питательные среды.
Мочеполовая (влагалищная) трихомонада имеет грушевидное тело длиной 14—30 мкм. На переднем конце тела расположены 4 жгутика и ундулирующая мембрана, доходящая только до середины тела. Ближе к переднему концу тела влагалищной трихомонады находится ядро. Сквозь все тело проходит осевая нить (аксостиль), выступающая на заднем конце в виде шипика. Цитоплазма содержит вакуоли.
Цист влагалищная трихомонада не образует. В окружающей среде быстро погибает. Играет заметную роль в патологии мочеполовой системы, особенно у женщин. Наблюдается и длительное бессимптомное носительство трихомонад, чаще у мужчин. Основными симптомами заболевания, которое называется мочеполовой трихомоноз, являются зуд, боль, жжение, серозно-гнойные выделения (белки).
Трихомонады этого вида передаются половым путем. Они не могут переселиться во влагалище из кишечника, так как мочеполовая и кишечная трихомонады — разные виды с разными требованиями к условиям обитания.
Диагноз ставят при обнаружении трихомонад в нативных и окрашенных по Романовскому препаратах. Готовят их из выделений мочеполовых путей и осадка мочи (полученной катетером) после ее центрифугирования.
При отрицательных результатах микроскопии в ряде случаев (подозрение на носительство, контроль после лечения и т. п.) применяют метод посева на питательную среду, серологические методы.
МАЛЯРИЙНЫЕ ПЛАЗМОДИИ
Виды малярийных плазмодиев. Плазмодии, вызывающие у человека малярию, относятся к четырем вилам: Plasmodium vivax — возбудитель трехдневной малярии; Plasmodium malariae — возбудитель че-тырехдневной малярии; Plasmodium falciparum — возбудитель тропической малярии и Plasmodium ovale — возбудитель малярии, типа трехдневной (овале).
Возбудителя малярии человека впервые обнаружил французский ученый А. Лаверан (1880).
Жизненный цикл малярийных плазмодиев. Малярийные плазмодии проходят две стадии развития - бесполую (шизогонию, от греч. schizen — делиться) в организме человека и половую (спорогонию) в организме переносчика — самок малярийных комаров рода Anopheles.
При кровососании зараженный малярийный комар вместе со слюной вводит в ранку спорозоиты — веретенообразные, чуть изогнутые образования длиной 11—15 мкм. С кровью они попадают в клетки печени, где развиваются и делятся (тканевая, или экзоэритроцитарная, шизогония), Образовавшиеся в результате деления в клетках печени молодые паразиты (мерозоиты) поступают в кровь и проникают в эритроциты — наступает эритроцитарная шизогония.
С наступлением эритроцитарной шизогонии развитие P. falciparum и Р. mаlariae в печени прекращается. Однако у Р. vivax и P. ovale часть спорозоитов сохраняется в печени («дремлют») и в дальнейшем, активизируясь, вызывает отдаленные рецидивы болезни.
Мерозоиты, проникшие в эритроциты, превращаются в трофозоиты (растущие формы), а последние — в шизонты (делящиеся формы). Шизонты в процессе деления дают новое поколение мерозоитов, которые в свою очередь проникают в другие эритроциты. Указанный цикл развития в эритроцитах составляет 72 ч. для P. malariae или 48 ч. для остальных видов.
В некоторых эритроцитах развиваются мужские и женские половые формы — гамонты. Они завершают свое развитие, только попав в организм комара с кровью в течение 7—45 суток в зависимости от температуры окружающего воздуха. В результате в слюнных железах малярийного комара скапливаются спорозоиты, и такой комар становится способным вновь заражать людей.

Токсоплазма
 Токсоплазма (Toxoplasma gondii) по форме тела напоминает полумесяц или дольку апельсина (от греч. toxon — арка). Один конец заострен, другой — закруглен. Длина токсоплазмы 4—7 мкм. При окраске по Романовскому цитоплазма голубовато-серая, а расположенное в центре тела или ближе к закругленному концу ядро — красно-фиолетового цвета (смотрите рисунок токсоплазмы слева). Токсоплазма — внутриклеточный паразит.
Токсоплазма (Toxoplasma gondii) по форме тела напоминает полумесяц или дольку апельсина (от греч. toxon — арка). Один конец заострен, другой — закруглен. Длина токсоплазмы 4—7 мкм. При окраске по Романовскому цитоплазма голубовато-серая, а расположенное в центре тела или ближе к закругленному концу ядро — красно-фиолетового цвета (смотрите рисунок токсоплазмы слева). Токсоплазма — внутриклеточный паразит.
Токсоплазма была впервые обнаружена французскими учеными Николь и Мансо в 1908 году у африканских грызунов гонди. В СССР токсоплазма впервые была обнаружена у сусликов Д. Н. Засухиным и Н. А. Гайским в 1930 году.
Жизненный цикл токсоплазмы. Токсоплазмы поражают многих диких и домашних животных и птиц, а также человека, в организме которых проходят бесполый цикл развития и размножения (промежуточные хозяева).В клетках печени, легких, лимфоидной ткани и других органов образуются скопления токсоплазм (псевдоцисты). При их разрушении освобожденные паразиты проникают в другие клетки и цикл деления повторяется. Псевдоцисты характерны для острой стадии инфекции. При хроническом течении процесса во внутренних органах (головной мозг, глаза, мышцы и др.) токсоплазмы образуют округлые истинные цисты с плотной оболочкой. Размер их достигает 100 мкм. В одной цисте содержатся сотни паразитов, они лежат так плотно, что в препарате видны только ядра. Цисты токсоплазмы сохраняются много лет.
 Половой цикл размножения токсоплазм происходит в клетках слизистой оболочки кишечника кошек (основной хозяин). С испражнениями кошек выделяются ооцисты, округлые, с плотной бесцветной двухслойной оболочкой, диаметром 9—14 мкм. Ооцисты созревают и хорошо сохраняются в почве, при их заглатывании заражаются животные, в том числе грызуны.
Половой цикл размножения токсоплазм происходит в клетках слизистой оболочки кишечника кошек (основной хозяин). С испражнениями кошек выделяются ооцисты, округлые, с плотной бесцветной двухслойной оболочкой, диаметром 9—14 мкм. Ооцисты созревают и хорошо сохраняются в почве, при их заглатывании заражаются животные, в том числе грызуны.
Человек заражается токсоплазмами: I) через рот (алиментарный, или пищевой путь) при употреблении сырого или полусырого мяса, фарша, а чаше — через загрязненные ооцистами (от кошек) овощи, ягоды, предметы, руки; 2) иногда через кожу рук и слизистые оболочки, например при разделке мясных туш, лабораторных работах с заразным материалом; 3) внутриутробно (трансплацентарный путь).
Токсоплазмы - возбудители токсоплазмоза. При заражении беременной женщины возбудитель через плаценту проникает в плод. В результате плод погибает (выкидыш, мертворождение) или родится живым с симптомами острого врожденного токсоплазмоза (интоксикация, повышенная температура тела, желтушность, поражение печени, селезенки, лимфатических узлов, нервной системы). В ряде случаев у родившихся внешне здоровыми детей впоследствии выявляются умственная отсталость, нарушении зрении и т. д.
Приобретенный токсоплазмоз развивается в случае заражения после рождения. Симптомы токсоплазмоза разнообразны. У больного повышается температура тела, увеличиваются лимфатические узлы, поражаются различные внутренние органы, на коже появляется сыпь и т. д. Токсоплазмоз может протекать и бессимптомно.
При подозрении на токсоплазмоз исследуют кровь, спинномозговую жидкость, пунктаты лимфатических узлов, остатки плодных оболочек, плаценту, а также трупный или биопсийный материал. Обнаруживаются токсоплазмы в окрашенных по Романовскому мазках, гистологических срезах тканей и в ряде случаев — при биологической пробе на белых мышах.
В медицинских учреждениях наиболее доступна внутрикожная аллергическая проба с токсоплазмином. Обследуемому человеку вводят 0,1 мл токсоплазмина шприцем внутрикожно на ладонной поверхности предплечья. У лиц, чувствительных к токсоплазмину на месте введения аллергена формируются эритема и инфильтрат. Положительной считают реакцию, если через 24 ч после инъекции диаметр участка покраснения и инфильтрата имеет не менее 10 мм и через 48 ч от момента постановки пробы не уменьшается и не исчезает. Проба положительна примерно с 4-й недели болезни и может сохраняться в течение многих лет. Лица, положительно реагирующие на токсоплазмин, не считаются больными токсоплазмозом. Положительная аллергическая проба лишь свидетельство бывшего заражения и диктует необходимость дальнейшего тщательного клинического и лабораторного обследования.
С целью серологического обследования на токсоплазмоз применяют РСК, РИФ, РЭМА и другие.
Антитела в крови появляются на 2—3-й неделе заболевания токсоплазмозом. При стихании процесса титр антител снижается и через некоторое время они могут исчезать. Достоверный диагноз токсоплазмоза можно поставить только с учетом динамики, особенно при нарастании, титров. Поэтому обязательным является как минимум двукратное исследование сывороток.
Для профилактики врожденного токсоплазмоза обследуют беременных женщин с помощью пробы с токсоплазмином, и в случае ее положительного результата проводят серологические исследования. При положительных лабораторных данных и наличии клинических показаний беременные женщины подлежат специфическому лечению и наблюдению.
Для профилактики всех форм токсоплазмоза важно соблюдать правила содержания кошек. Особенно тщательно меры предосторожности необходимо выполнять беременным женщинам, а также медицинскому персоналу при работе с инфицированным материалом.