Острая ревматическая лихорадка и хроническая ревматическая болезнь сердца: диагностика, лечение, профилактика
Б.С.Белов
ГУ Институт ревматологии (дир. - член-корр. РАМН Е.Л.Насонов) РАМН, Москва
Острая ревматическая лихорадка (ОРЛ) - постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных b-гемолитическим стрептококком группы А (БГСА), в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией в сердечно-сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающегося у предрасположенных лиц, главным образом молодого возраста (7-15 лет), в связи с аутоиммунным ответом организма на антигены стрептококка и их перекрестной реактивностью со схожими аутоантигенами перечисленных поражаемых тканей человека (феномен молекулярной мимикрии).
Хроническая ревматическая болезнь сердца (ХРБС) - заболевание, характеризующееся стойким поражением сердечных клапанов в виде поствоспалительного краевого фиброза клапанных створок или сформированного порока сердца (недостаточность и/или стеноз) после перенесенной ОРЛ.
Эпидемиология
Первичная заболеваемость ОРЛ в России в начале ХХI века - 0,027/1000 населения. Частота впервые выявленной ХРБС - 0,097/1000, в том числе ревматических пороков сердца (РПС) - 0,076/1000. Распространенность ХРБС - 0,45/1000 детского и 2,6/1000 взрослого населения. Преимущественный возраст поражаемых 7-15 лет. Половой диморфизм четко не прослеживается.
Анализ данных госстатотчета Минздрава РФ свидетельствует о том, что в современной России в силу известных негативных общественно-социальных изменений существует опасность появления истинных вспышек ОРЛ. В частности, в 1994 г. по сравнению с предыдущим 1993 г. отмечен подъем первичной заболеваемости (выявляемости) ОРЛ с 0,06 до 0,16 % среди детей и с 0,08 до 0,17% у подростков. Этот рост произошел преимущественно в Северо-Кавказском регионе, особенно в республиках Ингушетия и Дагестан. Однако и в целом по стране должна быть постоянной настороженность врачей в отношении возможных вспышек ОРЛ в связи с неснижающимися показателями первичной заболеваемости (выявляемости) ХРБС. Подавляющее большинство в данной категории составляют пациенты с приобретенными РПС. К концу последнего десятилетия прошлого века в России ежегодно диагностировалось на 2,5 тыс. больных с ХРБС больше, чем в начале регистрации (1994 г.). При этом распространенность ХРБС наиболее значимо (с 1,4 до 2,3 на 1000) увеличилась за счет населения Северного Кавказа, т.е. там, где в 1994 г. была зарегистрирована вспышка ОРЛ. Следовательно, проблемы ОРЛ и ХРБС по-прежнему должны быть в центре внимания ученых-медиков, организаторов здравоохранения и практических врачей.
А-стрептококковая инфекция
Имеющиеся данные ВОЗ свидетельствуют о высокой (более 30%) распространенности БГСА-инфекций верхних дыхательных путей среди школьников. Таким образом, сохраняется потенциальная возможность развития ОРЛ у предрасположенных к ней индивидуумов, в основном молодого возраста. Помимо этого, больные ХРБС представляют собой "постоянно действующий" семейно-генетический фонд предрасположенности к ОРЛ.
В последние годы все больше накапливается данных, которые позволяют вести речь о существовании "ревматогенных" БГСА-штаммов, обладающих высокой контагиозностью, тропностью к носоглотке, индукцией типоспецифических антител и др. А главное - "ревматогенные" стрептококки содержат эпитопы, способные перекрестно реагировать с различными тканями макроорганизма-хозяина: миозином и сарколеммальной мембраной, синовией и мозгом, т.е. теми структурами, которые вовлекаются в патологический процесс при ОРЛ.
Указанные данные подкрепляют концепцию молекулярной мимикрии (перекрестной реактивности) как основного патогенетического механизма реализации стрептококковой инфекции в ОРЛ, при котором образующиеся в ответ на антигены стрептококка антитела способны реагировать с аутоантигенами перечисленных выше органов хозяина.
Диагностика
При распознавании ОРЛ используется синдромный принцип, сформулированный отечественным педиатром А.А.Киселем в 1940 г., который в качестве диагностических критериев выделил пять признаков болезни: мигрирующий полиартрит, кардит, хорею, кольцевидную эритему, ревматические узелки, обратив при этом внимание на значимость их сочетания. В 1944 г. американский кардиолог Т.Д.Джонс отнес указанную пентаду синдромов к "большим" диагностических критериям, выделив наряду с ними "малые" клинические и лабораторные параметры. Впоследствии схема Джонса была неоднократно модифицирована Американской кардиологической ассоциацией (АКА) и получила широкое распространение.
В табл. 1 представлена схема диагностических критериев Киселя-Джонса с учетом последнего пересмотра АКА (1992 г.) и модификаций, предложенных Ассоциацией ревматологов России (АРР) в 2003 г.
Кардит - ведущий синдром ОРЛ, выявляющийся в 90-95% случаев, который определяет тяжесть течения и исход заболевания. Основополагающим компонентом кардита считается вальвулит (преимущественно митрального, реже - аортального клапанов), проявляющийся органическим сердечным шумом, возможно, в сочетании с миоперикардитом. Симптомы ревматического вальвулита следующие: а) дующий, связанный с I тоном систолический шум на верхушке сердца (митральная регургитация); б) непостоянный низкочастотный мезодиастолический шум в митральной области; в) высокочастотный убывающий протодиастолический шум, выслушиваемый вдоль левого края грудины (аортальная регургитация). Поражение сердца по типу миоперикардита при отсутствии вальвулита повсеместно признается маловероятным при ОРЛ и является показанием для проведения тщательной дифференциальной диагностики с кардитами иной (в первую очередь вирусной) этиологии.
На фоне ярко выраженного артрита или малой хореи клиническая симптоматика кардита при ОРЛ может быть выражена слабо. В связи с этим возрастает диагностическая значимость эхокардиографического (ЭхоКГ) исследования с использованием допплеровской техники, позволяющего оценить анатомическую структуру сердца и состояние внутрисердечного кровотока, в том числе выявить митральную или аортальную регургитацию как ранний признак вальвулита. С учетом изложенного данные ЭхоКГ-исследования включены в состав "малых" модифицированных диагностических критериев ОРЛ.
Важнейшая особенность вальвулита при первой атаке ОРЛ - четкая положительная динамика под влиянием активной антиревматической терапии. В преобладающем большинстве случаев на фоне лечения происходит нормализация частоты сердечных сокращений, восстановление звучности тонов, уменьшение интенсивности систолического и диастолического шумов, сокращение границ сердца, исчезновение симптомов недостаточности кровообращения.
ОРЛ как проблема большой социальной значимости определяется приобретенными РПС, которые по мере прогрессирования приводят к стойкой нетрудоспособности и преждевременной смерти. Частота формирования РПС после первой атаки ОРЛ у детей составляет 20-25%. Преобладают изолированные пороки сердца, чаще митральная недостаточность. Реже формируются недостаточность аортального клапана, митральный стеноз и митрально-аортальный порок. Однако необходимо постоянно помнить, что примерно у 7-10% детей после перенесенного кардита формируется пролапс митрального клапана.
Среди подростков, перенесших первую атаку ОРЛ, пороки сердца диагностируются в 1/3 случаев. У взрослых пациентов данный показатель составляет 39-45%, причем максимальная частота возникновения РПС (>75%) наблюдается в течение первых трех лет от начала болезни. У больных, перенесших первую атаку ОРЛ в возрасте 23 лет и старше, сочетанные и комбинированные РПС формируются в 90% случаев.
Ревматический полиартрит (60-100% случаев) - мигрирующий полиартрит преимущественно крупных и средних суставов (коленных, голеностопных, реже - локтевых, плечевых, лучезапястных). Как правило, сочетается с кардитом и редко (10-15% случаев) протекает изолированно. Преобладающая форма поражения в последние годы - преходящий олигоартрит и - реже - моноартрит. Отличается быстрой регрессией воспалительных изменений в суставах под влиянием противовоспалительной терапии.
В отдельных случаях возможны атипичные проявления суставного синдрома - поражение мелких суставов кистей и стоп, асимптомные сакроилеиты I-II стадии по Dale, чаще у мужчин молодого возраста.
В 10-15% случаев выявляется только артралгия (мигрирующая боль в крупных суставах различной интенсивности), которая в отличие от артрита не сопровождается болезненностью при пальпации и другими симптомами воспаления. По сравнению с мигрирующим полиартритом она имеет меньшую специфичность для ОРЛ и поэтому относится к малым диагностическим критериям заболевания.
Ревматическая хорея (малая хорея, хорея Сиденгама) диагностируется у 6-30% больных детей и редко у подростков. Чаще поражаются девочки и девушки.
Основные клинические проявления ревматической хореи наблюдаются в различных сочетаниях и с вариабельной степенью выраженности:
• хореические гиперкинезы
• мышечная гипотония (вплоть до дряблости мышц с имитацией параличей)
• расстройства статики и координации
• сосудистая дистония
• психоэмоциональные нарушения (неустойчивость настроения, раздражительность, плаксивость и т.д.)
Малая хорея, как правило, сочетается с другими клиническими синдромами ОРЛ (кардит, полиартрит), однако у 5-7% больных она может быть единственным проявлением болезни. В этих ситуациях, т.е. при отсутствии иных критериев ОРЛ, диагноз ревматической хореи правомочен только после исключения прочих причин поражения нервной системы.
Кольцевидная (аннулярная) эритеманаблюдается у 4-17% больных детей на высоте атаки ОРЛ. Характеризуется бледно-розовыми кольцевидными высыпаниями диаметром от нескольких миллиметров до 5-10 см с преимущественной локализацией на туловище и проксимальных отделах конечностей (но не на лице!). Она имеет транзиторный мигрирующий характер, не возвышается над уровнем кожи, не сопровождается зудом или индурацией, бледнеет при надавливании, быстро исчезает без остаточных явлений (пигментаций, шелушения, атрофических изменений).
Подкожные ревматические узелки в последние годы наблюдаются очень редко (1-3%). Это округлые плотные малоподвижные безболезненные образования различных размеров на разгибательной поверхности суставов, в области лодыжек, ахилловых сухожилий, остистых отростков позвонков, затылочной области gallea aponeurotica с циклом обратного развития от 2 нед до 1 мес.
Несмотря на значительное снижение частоты кольцевидной эритемы и ревматических узелков у детского контингента больных и фактическое отсутствие таковых у подростков и взрослых пациентов, специфичность данных синдромов при ОРЛ остается очень высокой, в силу чего они сохраняют свою диагностическую критериальную значимость.
Поражение серозных оболочек в настоящее время встречается редко, только при тяжелом течении первой атаки и/или повторной ревматической лихорадке, и проявляется преимущественно абдоминальным синдромом разной интенсивности с быстрым обратным развитием на фоне противовоспалительной терапии.
Неспецифические клинические и лабораторные синдромы, причисляемые к "малым " диагностическим критериям Киселя-Джонса, рассматриваются как удовлетворяющие таковым только при условиях, что они выявляются впервые у конкретного больного и не имеют под собой других причин. ЭхоКГ-феномены клапанной регургитации должны быть подтверждены при повторном исследовании через 10-14 дней.
Диагноз ОРЛ обязательно должен быть подкреплен лабораторными исследованиями, подтверждающими активную БГСА-инфекцию, предшествовавшую развитию заболевания. В этом отношении наиболее надежны серологические исследования, позволяющие выявить повышенные или (что важнее) повышающиеся показатели (титры) противострептококковых антител - антистрептолизина-О (АСЛ-О) и антидезоксирибонуклеазы В (анти-ДНКаза В). Как правило, титры указанных противострептококковых антител начинают повышаться к концу 2-й недели после перенесенного БГСА-тонзиллита/фарингита, достигают максимума к 3-4-й неделе и сохраняются на этом уровне в течение 2-3 мес с последующим снижением до исходных значений. Следует заметить, что нормальные показатели данных тестов весьма варьируют в зависимости от возраста больного, географического положения местности и сезона. Поэтому согласно рекомендациям ВОЗ верхняя граница нормы для противострептококковых антител не должна превышать 20% уровень над популяционными данными, полученными от здоровых лиц определенной возрастной группы, проживающих в конкретном регионе с учетом времени года. Небходимо, чтобы для каждой серии новых исследований в качестве контроля использовались стандартные (reference) сыворотки c известным титром противострептококковых антител.
При отсутствии серологического ответа на стрептококковый антиген в сочетании с негативными данными микробиологического исследования диагноз ОРЛ представляется маловероятным. Однако необходимо заметить, что уровень противострептококковых антител может быть нормальным, если между началом ОРЛ и проведением исследования прошло более 2 мес. Чаще всего это наблюдается у больных с ревматической хореей. Подобная закономерность встречается и у пациентов с поздним кардитом.
Предположительный диагноз повторной ОРЛ (особенно на фоне уже сформированного порока сердца, когда диагностика кардита в значительной степени затруднена) может быть поставлен на основании одного "большого" или только "малых" критериев в сочетании с повышенными или повышающимися титрами противострептококковых антител. Окончательный диагноз возможен лишь после исключения интеркуррентного заболевания и осложнений, связанных с пороками сердца (в первую очередь инфекционного эндокардита).
Таким образом, рассмотренные критерии диагноза ОРЛ являются руководством в диагностике болезни, но они не заменяют клинического мышления. Любая система диагностических критериев требует определенной врачебной квалификации для их правильного распознавания и интерпретации и может рассматриваться лишь как "квалифицированный консультант". Решающая же роль в диагностике принадлежит опыту и суждениям клинициста.
Классификация
В наступившем ХХI веке назрела явная необходимость пересмотра классификации и номенклатуры рассматриваемой нозологической формы (табл. 2). Термин "острая ревматическая лихорадка" (а не ревматизм!) представляется наиболее оправданным, поскольку он привлекает внимание врача к выяснению связи с БГСА-инфекцией, а также необходимостью назначения антибиотиков для эрадикации этой инфекции в остром периоде (первичная профилактика) и предотвращения повторных атак (вторичная профилактика). Что касается термина "первичный ревмокардит (ревматизм)", то клинически опыт показал нередкое расширение этого понятия на любое, впервые диагностированное заболевание сердца, включая пролапс митрального клапана как проявление гипермобильного синдрома, при котором могут быть и артралгии из-за перегрузки крупных и средних суставов.
Следует подчеркнуть, что повторная ревматическая лихорадка рассматривается как новый эпизод ОРЛ (но не рецидив первого!), проявляется преимущественно кардитом, реже кардитом и полиартритом, редко - хореей.
В представленной классификации выделяется два варианта исходов заболевания.
При выздоровлении речь идет о полном обратном развитии клинической симптоматики ОРЛ с нормализацией лабораторных показателей и отсутствием каких-либо остаточных изменений.
Хроническая ревматическая болезнь сердца - см. выше.
Важно отметить, что при наличии впервые выявленного порока сердца необходимо, по возможности, уточнить его генез (перенесенный инфекционный эндокардит и др.).
Хроническая сердечная недостаточность (ХСН) оценивается в соответствии с классификациями Стражеско-Василенко (степень) и Нью-Йоркской ассоциации кардиологов (функциональный класс).
Примеры клинического диагноза, в соответствии с рубрикацией МКБ-10, представлены в приложении.
Таким образом, представленная классификация ОРЛ направлена на достоверное распознавание болезни, ее раннюю диагностику, а следовательно, и максимально раннее комплексное лечение антибиотиками и противовоспалительными препаратами с последующим проведением вторичной профилактики.
Лечение
Лечение ОРЛ - комплексное, складывающееся из этиотропной (антимикробной), патогенетической (противовоспалительной), симптоматической терапии и реабилитационных мероприятий.
Всем пациентам с ОРЛ показана госпитализация с соблюдением постельного режима в течение первых 2-3 нед болезни, включением в пищевой рацион достаточного количества полноценных белков (не менее 1 г на 1 кг массы тела) и ограничением поваренной соли.
Этиотропная (противомикробная) терапия, направленная на эрадикацию БГСА из глотки, осуществляется бензилпенициллином в суточной дозе 1,5-4 млн ЕД у подростков и взрослых и 400 000-600 000 ЕД у детей в течение 10 дней с последующим переходом на применение дюрантной формы препарата (бензатин бензилпенициллин). В случаях непереносимости препаратов пенициллина показано назначение одного из антибиотиков из групп макролидов или линкозамидов (см. раздел "Профилактика").
Патогенетическое (противовоспалительное) лечение ОРЛ заключается в применении глюкокортикоидов (ГК) и нестероидных противовоспалительных препаратов (НПВП). Преднизолон (метилпреднизолон) применяют преимущественно у детей, особенно при выраженном кардите и полисерозитах. Препарат назначают в суточной дозе 15-20 мг (реже 30 мг) до достижения терапевтического эффекта, как правило, в течение 2 нед. В дальнейшем дозу снижают (2,5 мг каждые 5-7 дней) вплоть до полной отмены с последующим назначением НПВП.
Таблица 1. Критерии Киселя-Джонса, применяемые для диагностики ОРЛ (в модификации АРР, 2003)
| "Большие" критерии | "Малые" критерии | Данные, подтверждающие предшествовавшую А-стрептококковую инфекцию |
| Кардит | Клинические | Позитивная А-стрептококковая культура, |
| Полиартрит | Артралгии | выделенная из зева, или положительный тест |
| Хорея | Лихорадка (>38°С) | быстрого определения А-стрептококкового антигена |
| Кольцевидная эритема | Лабораторные | Повышенные или повышающиеся титры |
| Подкожные ревматические узелки | Повышенные острофазовые параметры: СОЭ (>30 мм/ч) С-реактивный белок (³2 N)* Инструментальные Удлинение интервала PR (>0,2 с) на ЭКГ Признаки митральной и/или аортальной регургитации при допплер-ЭхоКГ | противострептококковых антител (АСЛ-О, анти-ДНКаза В) |
| Примечание. Наличие двух "больших" критериев или одного "большого" и двух "малых" в сочетании с данными, документированно подтверждающими предшествующую инфекцию стрептококками группы А, свидетельствует о высокой вероятности ОРЛ. Особые случаи: 1. Изолированная ("чистая") хорея - при исключении других причин. 2. Поздний кардит - растянутое во времени (>2 мес) развитие клинических и инструментальных симптомов вальвулита - при исключении других причин. 3. Повторная ОРЛ на фоне ХРБС (или без нее). *N - нормальное значение. |
Таблица 2. Классификация ревматической лихорадки (АРР, 2003)
| Клинические варианты | Клинические проявления | Исход | Стадия НК | ||
| основные | дополнительные | КСВ* | NYHA** | ||
| Острая ревматическая лихорадка | Кардит (вальвулит) | Лихорадка | Выздоровление | ||
| Артрит | Артралгии | Хроническая | I | I | |
| Повторная ревматическая лихорадка | Кольцевидная эритема | Абдоминальный синдром | ревматическая болезнь | IIА | II |
| Подкожные ревматические | Серозиты | сердца: | IIБ | III | |
| узелки | - без порока сердца*** - порок сердца**** | III | IV | ||
| Примечание. *По классификации Н.Д.Стражеско и В.Х.Василенко. **Функциональный класс по NYHA. ***Наличие поствоспалительного краевого фиброза клапанных створок без регургитации, которое уточняется с помощью ЭхоКГ. ****При наличии впервые выявленного порока сердца необходимо, по возможности, исключить другие причины его формирования (инфекционный эндокардит, первичный антифосфолипидный синдром, кальциноз клапанов дегенеративного генеза и др.). |
Таблица 3. Дозы и режим введения антибиотиков при остром БГСА-тонзиллите
| Антибиотики | Суточная доза | Длительность лечения, дни | |
| взрослые | дети | ||
| Препараты выбора | |||
| b-Лактамы | |||
| Пенициллины | 1,5 г в 3 приема | 0,375 г в 3 приема (<25 кг) | |
| Амоксициллин | 750 мг в 3 приема (>25 кг) | ||
| Феноксиметилпенициллин1 | 1,5 г в 3 приема | 0,375 г в 2 приема (<25 кг) | |
| 750 мг в 2 приема (>25 кг) | |||
| бензатин | 2,4 млн ЕД внутримышено | 600 тыс. ЕД в/м (<25 кг) | Однократно |
| бензилпенициллин2 | 1,2 млн ЕД в/м (>25 кг) | ||
| Цефалоспорины | |||
| цефадроксил | 1 г в 2 приема | 30 мг/кг в 1 прием | |
| При непереносимости b-лактамных антибиотиков | |||
| Макролиды | |||
| эритромицин3 | 1,5 г в 3 приема | 40 мг/кг в 3 приема | |
| азитромицин | 0,5 г - 1-й день, затем 0,25 г в 1 прием | 12 мг/кг в 1 прием | |
| спирамицин | 6 млн ЕД в 2 приема | 3 млн ЕД в 2 приема | |
| кларитромицин | 0,5 г в 2 приема | 15 мг/кг в 2 приема | |
| рокситромицин | 0,3 г в 2 приема | 5 мг/кг в 2 приема | |
| мидекамицин | 1,2 г в 3 приема | 50 мг/кг в 2 приема | |
| При непереносимости макролидов и b-лактамных антибиотиков | |||
| Линкозамины | |||
| линкомицин | 1,5 г в 3 приема | 30 мг/кг в 3 приема | |
| клиндамицин | 0,6 г в 4 приема | 20 мг/кг в 3 приема | |
| Примечание. 1Рекомендуется преимущественно для лечения детей, учитывая наличие лекарственной формы в виде суспензии. 2Целесообразно назначать при: а) сомнительной комплаентности (исполнительности) пациента в отношении перорального приема антибиотиков; б) наличии ОРЛ в анамнезе у больного или ближайших родственников; в) неблагоприятных социально-бытовых условиях; г) вспышках БСГА-инфекции в детских дошкольных учреждениях, школах, интернатах, училищах, воинских частях и т.п. 3Для эритромицина характерно наиболее частое, по сравнению с другими макролидами, развитие побочных реакций, особенно со стороны желудочно-кишечного тракта; в/м - внутримышечно. |
Таблица 4. Антибактериальная терапия рецидивирующего БГСА-тонзиллита
| Антибиотик | Суточная доза | Длительность лечения, дни | |
| взрослые | дети | ||
| Амоксициллин/клавуланат | 1,875 г в 3 приема | 40 мг/кг в 3 приема | |
| Цефуроксим-аксетил | 0,5 г в 2 приема | 20 мг/кг в 2 приема | |
| Клиндамицин | 0,6 г в 4 приема | 20 мг/кг в 3 приема | |
| Линкомицин | 1,5 г в 3 приема | 30 мг/кг в 3 приема |
При лечении ОРЛ с преимущественным мигрирующим полиартритом, а также повторной ревматической лихорадкой на фоне ХРБС назначают НПВП - диклофенак натрия в суточной дозе 75-150 мг (детям до 12 лет - 2-3 мг/кг) в течение 2 мес. Этот препарат также рассматривается в качестве средства выбора при лечении ревматической лихорадки у взрослых.
Принимая во внимание специфические особенности воздействия ГК на минеральный обмен, а также достаточно высокий уровень дистрофических процессов в миокарде, особенно у больных с повторной ОРЛ на фоне РПС, показано назначение следующих препаратов:
А) аспартат калия и магния - 3-6 таблеток в сутки в течение 1 мес;
Б) инозин 0,6-1,2 г/сут в 3 приема в течение 1 мес;
В) нандролон 1,0 мл внутримышечно еженедельно, 10 инъекций на курс.
Общепризнано, что при хорее, протекающей без других симптомов ОРЛ, применение ГК и НПВП практически не эффективно. В большей степени показано назначение психотропных препаратов - нейролептиков (аминазин 0,01 г/сут) или транквилизаторов из группы бензодиазепина (диазепам 0,006-0,01 г/сут). При выраженных гиперкинезах возможно сочетание указанных средств с противосудорожными препаратами (карбамазепин 0,6 г/сут).
Применение снотворных средств нерационально, поскольку независимо от выраженности хореи ее проявления исчезают во время сна. Важным элементом лечения является полный психический и физический покой. Во избежание травм пациента его кровать следует обложить мягкими подушками. При отсутствии других проявлений ОРЛ можно разрешить больному постепенно восстанавливать свою привычную физическую активность, как только появится тенденция к улучшению его состояния, а не ждать полного исчезновения хореиформных движений, так как для этого может потребоваться длительное время (иногда до 1 года).
Подходы к терапии ХСН у больных ОРЛ и ХРБС имеют ряд особенностей. В частности, в случаях развития сердечной декомпенсации как следствия острого вальвулита (что, как правило, встречается только в детском возрасте) применение кардиотонических препаратов нецелесообразно, поскольку в этих случаях явный терапевтический эффект может быть достигнут при использовании высоких доз преднизолона (40-60 мг в сутки). В то же время больным ХРБС и ХСН без явных признаков кардита назначение ГК совершенно не оправдано из-за усугубления прогрессирующей миокардиодистрофии. У пациентов с кардитом на фоне ХРБС при выборе лекарственных средств, применяемых в терапии ХСН, следует учитывать их возможное взаимодействие с противовоспалительными препаратами.
Основные группы препаратов, применяемых в лечении ХСН у больных ОРЛ и ХРБС:
1. Диуретики: петлевые - фуросемид; тиазидные и тиазидоподобные - гидрохлортиазид, индапамид; калийсберегающие - спиронолактон, триамтерен.
2. Блокаторы кальциевых каналов из группы дигидропиридинов длительного действия (амлодипин).
3. b-Адреноблокаторы (карведилол, метопролол, бисопролол).
4. Сердечные гликозиды (дигоксин).
Дозы и схемы применения вышеуказанных препаратов аналогичны таковым при лечении ХСН иной этиологии.
Применение нитратов в комплексном лечении ХСН у больных ХРБС в последнее время значительно снизилось из-за развития толерантности. Эти препараты также ухудшают прогноз заболевания у данной категории пациентов.
Вопрос о целесообразности применения ингибиторов АПФ больным с кардитом на фоне ХРБС требует дальнейшего изучения. Известно, что ряд эффектов ингибиторов АПФ при ХСН реализуется через активацию синтеза простагландинов и подавление разрушения брадикинина, также обладающего сосудорасширяющей активностью. В то же время основной механизм действия НПВП, в частности диклофенака, являющегося препаратом выбора при повторных атаках ОРЛ, связан с ингибицией синтеза простагландинов. Следовательно, совместное назначение НПВП и ингибиторов АПФ может привести к ослаблению вазодилатирующего эффекта последних.
Второй этап курации больного с ОРЛ предусматривает направление ребенка и подростка в специализированный ревматологический санаторий, а взрослого пациента - в кардиологический местный санаторий или в поликлинику для продолжения лечения, начатого в стационаре. На третьем этапе осуществляется диспансерное наблюдение и проводятся профилактические мероприятия.
Профилактика
Программа предупреждения ОРЛ и повторных атак заболевания включает первичную и вторичную профилактику.
Основные цели первичной профилактики заключаются в следующем.
1. Мероприятия, направленные на повышение уровня естественного иммунитета и адаптационных возможностей организма по отношению к неблагоприятным условиям внешней среды. К ним относятся:
• раннее закаливание
• полноценное витаминизированное питание
• максимальное использование свежего воздуха
• рациональная физкультура и спорт
• борьба со скученностью в жилищах, детских дошкольных учреждениях, школах, училищах, вузах, общественных учреждениях
• проведение комплекса санитарно-гигиенических мер, снижающих возможность стрептококкового инфицирования коллективов, особенно детских
2. Своевременное и эффективное лечение острой и хронической рецидивирующей БГСА-инфекции глотки: тонзиллита (ангины) и фарингита.
Несмотря на то что БГСА сохраняет практически полную чувствительность к b-лактамным антибиотикам, в последние годы отмечаются определенные проблемы в терапии тонзиллитов, вызванных этим микроорганизмом. По данным разных авторов, частота неудач пенициллинотерапии БГСА-тонзиллитов составляет 25-30%, достигая 38%. Одной из возможных причин этого может быть гидролиз пенициллина специфическими ферментами - b-лактамазами, которые продуцируются микроорганизмами - копатогенами (золотистый стафилококк, гемофильная палочка и др.), присутствующими в глубоких тканях миндалин, особенно при наличии хронических воспалительных процессов в последних.
Таким образом, препараты пенициллинового ряда остаются средствами выбора только при лечении острого БГСА-тонзиллита (табл. 3). На сегодняшний день оптимальным препаратом из группы оральных пенициллинов является амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50% соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 80% соответственно). При сомнительной комплаентности (исполнительности) больного, а также определенных клинико-эпидемиологических ситуациях показано назначение однократной инъекции бензатин пенициллина.
Применение феноксиметилпенициллина следует ограничить только младшим детским контингентом больных, учитывая наличие лекарственной формы в виде суспензии, а также несколько большую комплаентность, контролируемую со стороны родителей, чего нельзя сказать о подростках.
Наряду с пенициллинами заслуживает несомненного внимания цефадроксил - представитель оральных цефалоспоринов I поколения, высокая эффективность которого в терапии БГСА-тонзиллитов, а также хорошая переносимость подтверждены в многочисленных клинических исследованиях.
При непереносимости b-лактамных антибиотиков показано назначение макролидов (спирамицин, азитромицин, рокситромицин, кларитромицин, мидекамицин). Наряду с высокой противострептококковой активностью, преимуществами этих препаратов являются: способность создавать высокую тканевую концентрацию в очаге инфекции, более короткий (в частности, для азитромицина) курс лечения, хорошая переносимость. Применение эритромицина - первого представителя антибиотиков данного класса в настоящее время существенно снизилось, особенно в терапевтической практике, поскольку он наиболее часто, по сравнению с другими макролидами, вызывает нежелательные эффекты со стороны желудочно-кишечного тракта, обусловленные его стимулирующим действием на моторику желудка и кишечника.
Антибиотики-линкозамиды (линкомицин, клиндамицин) назначают при БГСА-тонзиллите только при непереносимости как b-лактамов, так и макролидов. Широкое применение этих препаратов при данной нозологической форме не рекомендуется. Известно, что при частом применении оральных пенициллинов чувствительность к ним со стороны зеленящих стрептококков, локализующихся в ротовой полости, существенно снижается. Поэтому у данной категории пациентов, среди которых достаточное число больных с РПС, линкозамиды рассматриваются как препараты первого ряда для профилактики инфекционного эндокардита при выполнении стоматологических манипуляций.
При наличии хронического рецидивирующего БГСА-тонзиллита вероятность колонизации очага инфекции микроорганизмами, продуцирующими b-лактамазы, достаточно высока. В этих случаях лечение проводят ингибиторзащищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим- аксетил), а при непереносимости b-лактамных антибиотиков - линкозамидами (табл. 4). Указанные антибиотики также являются препаратами второго ряда для случаев безуспешной пенициллинотерапии острого БГСА-тонзиллита (что чаще встречается при использовании феноксиметилпенициллина). Универсальной же схемы, обеспечивающей 100% элиминацию БГСА из носоглотки, в мировой клинической практике не имеется.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола (бисептола) и хлорамфеникола при БГСА-инфекции глотки в настоящее время не оправдано из-за высокой частоты резистентности и, следовательно, низких показателей эффективности терапии. Ранние фторхинолоны (ципрофлоксацин, пефлоксацин, офлоксацин, ломефлоксацин) также не должны назначаться при БГСА-инфекции глотки по причине их низкой природной противострептококковой активности.
Вторичная профилактика направлена на предупреждение повторных атак и прогрессирования заболевания у лиц, перенесших ОРЛ, и предусматривает регулярное круглогодичное введение пенициллина пролонгированного действия (бензатин бензилпенициллина). Препарат вводят глубоко внутримышечно детям с массой тела до 27 кг в дозе 600 000 ЕД 1 раз в 3 нед, детям с массой тела более 27 кг - 1 200 000 ЕД 1 раз в 3 нед, подросткам и взрослым - 2 400 000 ЕД 1 раз в 3 нед.
Длительность вторичной профилактики (которую следует начинать еще в стационаре) для каждого пациента устанавливается индивидуально и в соответствии с рекомендациями ВОЗ определяется наличием факторов риска повторных атак ОРЛ. К этим факторам относятся:
• Возраст больного
• Наличие ХРБС
• Время от момента первой атаки ОРЛ
• Число предыдущих атак
• Фактор скученности в семье
• Семейный анамнез, отягощенный по ОРЛ/ХРБС
• Социально-экономический и образовательный статус больного
• Риск стрептококковой инфекции в регионе
• Профессия и место работы больного (школьные учителя, врачи, лица, работающие в условиях скученности)
Как правило, длительность вторичной профилактики должна составлять:
а) для лиц, перенесших ОРЛ без кардита (артрит, хорея), - не менее 5 лет после последней атаки или до 18-летнего возраста (по принципу "что дольше");
б) в случаях излеченного кардита без формирования порока сердца - не менее 10 лет после последней атаки или до 25-летнего возраста (по принципу "что дольше");
в) для больных с пороком сердца (в том числе после оперативного лечения) - пожизненно.
Наиболее эффективной лекарственной формой бензатин бензилпенициллина является экстенциллин. Исследования, проведенные в Институте ревматологии РАМН и Государственном научном центре по антибиотикам, показали, что экстенциллин обладает явными фармакокинетическими преимуществами в сравнении с бициллином-5 по основному параметру - длительности поддержания адекватной противострептококковой концентрации бензилпенициллина в сыворотке крови пациентов. Из отечественных препаратов рекомендуется бициллин-1, который назначается в вышеуказанных дозах 1 раз в 7 дней.
В настоящее время препарат бициллин-5 (смесь 1,2 млн ЕД бензатин бензилпенициллина и 300 тыс. ЕД новокаиновой соли бензилпенициллина) рассматривается как не соответствующий фармакокинетическим требованиям, предъявляемым к превентивным препаратам, и не является приемлемым для проведения полноценной вторичной профилактики ОРЛ.
Широко практиковавшееся ранее ежедневное применение эритромицина у больных с ОРЛ в анамнезе и непереносимостью b-лактамных антибиотиков на сегодняшний день нуждается в пересмотре из-за повсеместного нарастания резистентности БГСА к макролидам. В качестве альтернативы у данной категории пациентов может рассматриваться своевременное курсовое лечение макролидами каждого случая БГСА-тонзиллита/фарингита.
Прогноз
Непосредственная угроза жизни в связи с ОРЛ практически отсутствует (за исключением чрезвычайно редких случаев панкардита в детском возрасте). В основном прогноз определяется состоянием сердца (наличие и тяжесть порока, степень застойной сердечной недостаточности). Весьма важны сроки начала терапии, так как при поздно начатом лечении (как и отсутствии такового) вероятность образования порока сердца резко увеличивается.
3.Ревматоидный артрит
Ревматоидный артрит
Ревматоидный артрит – хроническое аутоиммунное системное воспалительное заболевание соединительной ткани с преимущественным поражением суставов по типу эрозивно-деструктивного прогрессирующего полиартрита. Заболевание поражает 0.5-1% населения. Во всем мире ревматоидным артритом страдают около 58 млн. человек.
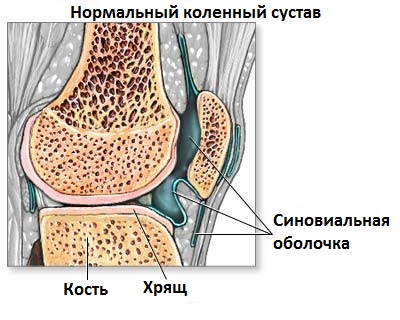
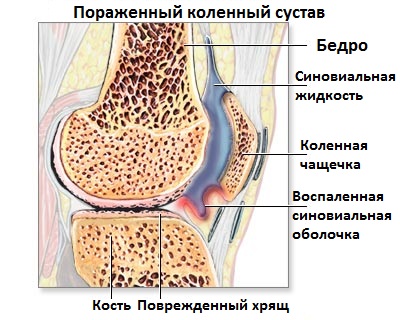
Точная причина развития ревматоидного артрита неизвестна. В основе патогенеза ревматоидного артрита лежат генетически детерминированные аутоиммунные процессы, возникновению которых способствует дефицит Т-супрессорной функции лимфоцитов. Неизвестный этиологический фактор вызывает развитие иммунной ответной реакции. Повреждение сустава начинается с воспаления синовиальной оболочки (синовита), приобретающего затем пролиферативный характер (паннус) с повреждением хряща и костей. Плазматические клетки синовии продуцируют измененный агрегированный IgG. В свою очередь, он распознается иммунной системой как чужеродный антиген, и плазматические клетки синовии, лимфоузлов, селезенки начинают вырабатывать к нему антитела – ревматоидные факторы (РФ). Важнейшим является РФ класса IgM, который обнаруживается у 70-80% больных ревматоидным артритом.
Вследствие аутоиммунного воспалительного процесса формируется паннус – грануляционная ткань, происходящая из воспаленной синовиальной оболочки, состоящая из активно пролиферирующих фибробластов, лимфоцитов, макрофагов и богатая сосудами. Паннус интенсивно растет, проникает из синовиальной ткани в хрящ и разрушает его посредством воздействия ферментов, индуцированных продукцией цитокинов внутри самого паннуса. Постепенно внутрисуставный хрящ исчезает, происходит замена его грануляционной тканью и развивается анкилоз. Хроническое воспаление околосуставных тканей, капсулы суставов, связок, сухожилий приводит к деформации суставов, подвывихам, контрактурам. В настоящее время существует точка зрения, что аутоиммунные процессы играют ведущую роль на ранних стадиях ревматоидного артрита, а на поздних стадиях большее значение имеют неиммунные механизмы (т.е. способность паннуса к росту, инвазии и разрушению суставного хряща).
Суставный синдром – ведущее клиническое проявление ревматоидного артрита. Типичным для ревматоидного артрита является двустороннее симметричное поражение суставов. Начало заболевания нередко связано с неблагоприятными метеоусловиями (весна, осень), периодами физиологической перестройки организма (пубертатный, послеродовый, климактерический периоды). Развитие ревматоидного артрита может быть спровоцировано перенесенной инфекцией, охлаждением, травмой, стрессовой ситуацией.
Наиболее характерно для ревматоидного артрита поражение суставов кистей, стоп, запястья, коленных, локтевых. Редко поражаются плечевые, тазобедренные и суставы позвоночника. Поражение суставов при ревматоидном артрите, как правило, носит симметричный характер, сопровождается ощущением утренней скованности, резким ограничением подвижности в суставах, что значительно ограничивает возможность самообслуживания (трудно одеться, умыться, причесаться, побриться и т. д.) и трудоспособность. Продолжительность утренней скованности тем больше, чем активнее воспалительный процесс в суставах.
Поражение почек в виде гломерулонефрита или амилоидоза – наиболее тяжелое висцеральное проявление ревматоидного артрита. Ревматоидный гломерулонефрит развивается обычно при высокой активности процесса и наиболее часто характеризуется изолированным мочевым синдромом (протеинурией, микрогематурией), исчезающим после купирования обострения ревматоидного артрита. Реже наблюдается диффузный гломерулонефрит со стойкой протеинурией, микрогематурией, повышением артериального давления, отеками, нарушением функции почек. В отдельных случаях возможен исход гломерулонефрита в нефросклероз.
Амилоидоз почек развивается обычно при длительном течении ревматоидного артрита (более 7-10 лет) и высокой активности процесса. Основные проявления: стойкая протеинурия (1-3 г/л), цилиндрурия, отеки, артериальная гипертензия, постепенное нарушение концентрационной (изогипостенурия в пробе по Зимницкому) и азотовыделительной функций почек. С развитием хронической почечной недостаточности появляется анемия. Амилоидоз почек может сопровождаться развитием нефротического синдрома, для которого характерны высокая протеинурия (концентрация белка в моче 6-8 г/л), гипопротеинемия, гипохолестеринемия, выраженные отеки, быстро развивающаяся почечная недостаточность, анемия.
Степени активности ревматоидного артрита:
I степень (минимальная активность). Небольшие боли в суставах, непродолжительная скованность по утрам (до 30 минут), незначительные экссудативные явления в суставах, температура кожи над суставами нормальная или несколько повышена. СОЭ повышена до 20 мм/ч, количество лейкоцитов в крови нормальное, уровень альфа-2-глобулинов повышен до 12%, С-реактивный протеин (СРП)+, показатели фибриногена, сиаловых кислот несколько повышены.
II степень (средняя активность). Боли в суставах не только при движениях, но и в покое, скованность продолжается до полудня, выраженное болевое ограничение подвижности в суставах, умеренные стабильные экссудативные явления. Гипертермия кожи над суставами умеренная. Поражение внутренних органов выражено нечетко, температура тела субфебрильная. СОЭ повышена – от 25 до 40 мм/ч, количество лейкоцитов в крови 8-10×109/л, содержание альфа-2-глобулинов увеличено до 15%. СРП ++, заметно повышены уровни сиаловых кислот, фибриногена.
III степень (высокая активность). Сильные боли в покое, выраженные экссудативные явления в суставах (значительная припухлость, гиперемия и повышение температуры кожи), скованность в течение всего дня, выраженное ограничение подвижности.
Признаки активного воспалительного процесса во внутренних органах (плеврит, перикардит, кардит, нефрит и др.): температура тела высокая. СОЭ превышает 40 мм/ч, количество лейкоцитов в крови 15-20×109/л, агглобулинов больше 15%, СРП+++, резко увеличено содержание фибриногена, сиаловых кислот.
Функциональные нарушения (ФН) опорно-двигательного аппарата:
ФН I - незначительное ограничение движений в суставах, ощущение небольшой скованности по утрам; профессиональная пригодность обычно сохранена, но несколько ограничена (противопоказана тяжелая работа).
ФН II – ограничение движений в суставах, стойкие контрактуры, затрудняется самообслуживание, профессиональная пригодность обычно потеряна.
ФН III – тугоподвижность либо полное отсутствие движений в суставах, потеряна способность самообслуживания, больной нуждается в постоянном уходе.
Лечение РА симптоматическое, направлено на уменьшение степени тяжести воспалительного процесса в суставах: глюкокортикостероиды, нестероидные противоспалительные препараты, местная обезболивающая и противоспалительная терапия, физиотерапия.
Причины
Точная причина Ревматоидного Артрита неизвестна. В норме иммунная система организма борется с различными чужеродными агентами, такими как вирусы, бактерии и т.д. При аутоиммунном заболевании иммунная система путает здоровые ткани с чужеродными агентами. И, как результат, борется с собственным организмом.
Ревматоидный Артрит может проявляться в любом возрасте. Женщины страдают чаще мужчин.
Ревматоидный Артрит обычно симметрично поражает суставы. Кисти, пальцы, колени, стопы, локти – наиболее частые локализации Ревматоидного Артрита.
Первичные симптомы
· Усталость
· Потеря аппетита
· Незначительное повышение температуры
· Воспаление слюнных желез
· Слабость
В последующем появляются боли в области суставов:
· Утренняя скованность более 1 часа. Суставы могут быть горячими, болезненными. Скованность может появляться даже при незначительном отдыхе
· Боль в области суставов чаще симметричная
· Наиболее часто поражаются пальцы, кисти, локти, плечи, тазобедренные суставы, колени, лодыжки, пальцы ног, суставы нижней челюсти и шейного отдела позвоночника
· Суставы часто отечные, теплые и мягкие (губчатые) на ощупь
· Со временем появляются ограничение движений в суставах, они деформируются
Другие симптомы
· Боль в груди во время дыхания (плеврит)
· Жжение и зуд в глазах
· Узелки под кожей
· Онемение, покалывание или жжение в руках и ногах
Поражение суставов может проявляться через 1-2 года после появления первичных симптомов заболевания.
Обследование и анализы
Наиболее специфическое исследования крови для подтверждения Ревматоидного Артрита - анти-ЦЦП (Антитела к циклическому цитрулинированному пептиду/Anti-ССР).
Другие исследования включают:
· Общий анализ крови
· С-реактивный белок
· Скорость (реакция) оседания эритроцитов (СОЭ)
· УЗИ и МРТ суставов
· Рентгенография суставов
· Ревматоидный фактор (позитивный у 75% людей с симптомами Ревматоидного Артрита)
· Анализ синовиальной жидкости
Исследование крови и мочи в динамике показывает эффективность получаемого пациентом лечения и тяжесть побочных эффектов вызванных получаемым лечением.
Лечение
Ревматоидный Артрит обычно требует пожизненного лечения, которое включает: медикаменты, физиотерапию, лечебную физкультуру и возможно хирургическое лечение. Раннее активное лечение Ревматоидного Артрита может на длительный срок отсрочить деструкцию суставов.
Медикаменты
Иммуносупрессивные препараты. В комбинации с лечебной физкультурой и нестероидными противовоспалительными средствами данная группа препаратов являются базисными в лечении Ревматоидного Артрита. К ним относятся:
Метотрексат, Азотиоприн, Инфликсимаб, Левамизол, Лефлуномид, Меркаптопурин и т.д. При приеме этих препаратов возможны значительные побочные эффекты, поэтому при их длительном приеме пациенты нуждаются в систематической сдачи анализов крови и мочи.
Нестероидные противовоспалительные препараты (НПВП): диклофенак натрия, ибупрофен, мелоксикам и др.
Несмотря на значительный эффект при длительном приеме НПВП возможны различные осложнения со стороны желудочно-кишечного тракта (гастрит, язва, кровотечение) и сердечно-сосудистой системы.
Противомалярийные средства. Данная группа препаратов включает гидроксихлорохин (плаквенил) и сульфасалазин, и часто используется в комплексе с метотрексатом. Эффект от этой комбинации обычно наступает через несколько недель (месяцев).
Кортикостероиды. Данные препараты очень быстро уменьшают отек и воспаление суставов. Однако из-за большого числа серьезных побочных эффектов прием кортикостероидов необходимо по возможности ограничивать малыми дозами и кратковременным приемом.
Биологическая терапия
Биологические препараты оказывают прицельное влияние на те звенья иммунитета, которые принимают участие в патогенезе Ревматоидного Артрита. Они могут быть назначены врачом как первично, так и при неэффективности предыдущего лечения. Большинство из них вводятся инъекционно: внутривенно или подкожно.
Существует 3 группы препаратов применяемых как биологическая терапия при Ревматоидного Артрита:
· Модуляторы белых клетки крови (лимфоцитов): абатацепт (Orencia) и ритуксимаб (Ритуксан)
· Ингибитор фактора некроза опухоли (ФНО) включают: адалимумаб (Humira), инфликсимаб (Ремикейд) и др.
· Ингибиторы Интерлейкина-6 (ИЛ-6): тоцилизумаб (Актемра).
Биологические препараты крайне эффективны в лечении Ревматоидного Артрита, однако, люди принимающие их находятся в зоне риска по следующим заболеваниям:
· Инфекции вызванные бактериями, вирусами, грибками
· Лейкемия
· Возможны обострения псориаза
Хирургическое лечение
При серьезных поражениях суставов для уменьшения болей и коррекции их деформаций требуется хирургическое лечение. Первичным хирургическим вмешательством при Ревматоидного Артрита обычно является синовэктомия (удаление капсулы сустава). В некоторых случаях требуется тотальное протезирование сустава (коленного, тазобедренного, локтевого, плечевого и других).