Далее серин может превратиться в ПВК.
Превращения АК в соответствующие a-оксокислоты происходит также путем окислительного дезаминирования. Этот процесс катализируется либо НАД-зависимостью ДГ, либо флавинзависимой оксидазой.
Общий вид:
R R R
| | |
CH – NH2 C=NH C=O
| -H2 | +H2O; - NH3 |
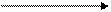
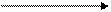 COOH COOH COOH
COOH COOH COOH
Аминокислота иминокислота альфа – кетокислота
Наиболее важной и широко распространенной ДГ является глутамат ДГ.
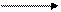 COOH НАД НАДН COOH
COOH НАД НАДН COOH
| +H2O |
 CH2 - NH3 CH2
CH2 - NH3 CH2
| глютамат ДГ |
CH2 CH2
| |
CH – NH2 C=O
| |
COOH COOH
Глутамат альфа-кетоглютомат
Так как глютамат может образовываться из альфа-кетоглютарата, то такой вид дезамирования называется непрямым.
 НАД НАДН
НАД НАДН
 (НАДФ) (НАДФН2)
(НАДФ) (НАДФН2)

 Глутамат альфа-оксоглютарат + аммиак.
Глутамат альфа-оксоглютарат + аммиак.
Хотя эта реакция легко обратима, ее основная роль, видимо, сводится к дезаминированию. Выделившийся аммиак может использоваться в других реакциях, например, при амидировании глутамата или аспартата до образования, соответственно, глютамина и аспарагина, но большая его часть выводится из организма в виде аммиака или мочевины. интересное свойство этого фермента заключается в том, что хотя глутамат является идеальным субстратом, фермент способен в качестве ко-фермента использовать как НАД, так и НАДФ. Следовательно, помимо роли, которую он играет в метаболизме азота, фермент может служить также внутриклеточным источником НАДФН, необходимого для процессов анаболизма (например, при синтезе жирных кислот, холестерина и т.д.). Существует два разных типа флавинзависимых оксидаз аминокислот. Один из них использует в качестве акцептора электронов ФАД (действует на Д-АК), второй – ФМН (действует на L-АК). В обоих случаях и ФАДН2 и ФМНН2 могут реагировать с кислородом с образованием перекиси воорода. Каталаза играет роль предохранительного клапана, расщепляя перекись водорода до воды и кислорода. Есть и неокислительные дезаминирования. Как правило, этот процесс происходит в результате перегруппировки атомов (это характерно для серина, треонина, цистеина, гистидина). Общий вид:
R R
 | - NH3 |
| - NH3 |
CH – NH2 COOH
|
COOH
Для гистидина:










 N CH2 – CH – COOH N CH = CH – COOH
N CH2 – CH – COOH N CH = CH – COOH





 | -NH3
| -NH3
NH NH2 NH уроканиновая кислота
 2АТФ 2АДФ + ФК
2АТФ 2АДФ + ФК
 NH3 + CO2 NH2
NH3 + CO2 NH2
Карбомоилфосфатсинтетаза |
CO
|
O – PO3H2
Карбомоилфосфат
Особенности обмена глицина и серина.
Глицин используется для синтеза ряда важных соединений (гем, пуриновые нуклеотиды, парные желчные кислоты, глютатион, креатин, муравьиная кислота, гиппуровая кислота). При распаде глицин превращается в глиоксалевую кислоту, которая переходит в муравьиную кислоту, в свою очередь используемую для образования из глицина
(NH2 – CH2 - COOH) серина (OH – CH2 – CH2(NH2) - COOH). Синтезироваться глицин может из треонина, серина, глиоксалата. Глицин может превращаться в серин, при этом донором одноуглеродного радикала является тетрагидрооронат.
 метилен-ТГФК ТГФК
метилен-ТГФК ТГФК

 СН2 – СООН СН2 – СН – СООН
СН2 – СООН СН2 – СН – СООН
| серингидроксиметилтрансфераза | |
NH2 OH NH2
Глицин серин
Далее серин может превратиться в ПВК.
Главный путь катаболизма глицина – это катализируемое глицинсинтазным комплексом (очень похож на ПДК) превращение, в результате которого образуется NH3, СО2, а метиленовая группа переносится на ТГФК тетрагидрофоливую кислоту с образованием метилентетрагидрофолата. Это происходит в митохондриях:
 ТГФК метиленТГФК
ТГФК метиленТГФК

 NH2 – CH2 – COOH NH3 + CO2
NH2 – CH2 – COOH NH3 + CO2