Править] Микробиологический синтез
Править] История биотехнологии
Впервые термин «биотехнология» применил венгерский инженер Карл Эреки в 1917 году.
Отдельные элементы биотехнологии появились достаточно давно. По сути, это были попытки использовать в промышленном производстве отдельные клетки (микроорганизмы) и некоторые ферменты, способствующие протеканию ряда химических процессов.
Так, в 1814 году петербургский академик К. С. Кирхгоф открыл явление биологического катализа и пытался биокаталитическим путём получить сахар из доступного отечественного сырья (до середины XIX века сахар получали только из сахарного тростника). В 1891 году в США японский биохимик Дз. Такамине получил первый патент на использование ферментных препаратов в промышленных целях: учёный предложил применить диастазу для осахаривания растительных отходов.
В начале XX века активно развивалась бродильная и микробиологическая промышленность. В эти же годы были предприняты первые попытки использовать ферменты в текстильной промышленности.
В 1916—1917 годах русский биохимик А. М. Коленев пытался разработать способ, который позволил бы управлять действием ферментов в природном сырье при производстве табака.
Огромный вклад в дело практического использования достижений биохимии внёс академик А. Н. Бах, создавший важное прикладное направление биохимии — техническую биохимию. А. Н. Бах и его ученики разработали множество рекомендаций по улучшению технологий обработки самого различного биохимического сырья, совершенствованию технологий хлебопечения, пивоварения, виноделия, производства чая и табака и т. п., а также рекомендации по повышению урожая культурных растений путём управления протекающими в них биохимическими процессами.
Все эти исследования, а также прогресс химической и микробиологической промышленности и создание новых промышленных биохимических производств (чая, табака и т. п.) были важнейшими предпосылками возникновения современной биотехнологии.
В производственном отношении основой биотехнологии в процессе её формирования стала микробиологическая промышленность. За послевоенные годы микробиологическая промышленность приобрела принципиально новые черты: микроорганизмы стали использовать не только как средство повышения интенсивности биохимических процессов, но и как миниатюрные синтетические фабрики, способные синтезировать внутри своих клеток ценнейшие и сложнейшие химические соединения. Перелом был связан с открытием и началом производства антибиотиков.
Первый антибиотик — пенициллин — был выделен в 1940 году. Вслед за пенициллином были открыты и другие антибиотики (эта работа продолжается и поныне). С открытием антибиотиков сразу же появились новые задачи: налаживание производства лекарственных веществ, продуцируемых микроорганизмами, работа над удешевлением и повышением уровня доступности новых лекарств, получением их в очень больших количествах, необходимых медицине.
Синтезировать антибиотики химически было очень дорого или вообще невероятно трудно, почти невозможно (недаром химический синтез тетрациклина советским учёным академиком М. М. Шемякиным считается одним из крупнейших достижений органического синтеза). И тогда решили для промышленного производства лекарственных препаратов использовать микроорганизмы, синтезирующие пенициллин и другие антибиотики. Так возникло важнейшее направление биотехнологии, основанное на использовании процессов микробиологического синтеза.
Править] Направления биотехнологии
править] Микробиологический синтез
Развитие микробиологической промышленности, выпускающей ценные продукты биосинтеза, позволило накопить очень важный опыт конструирования, производства и эксплуатации принципиально нового промышленного оборудования. Современное микробиологическое производство — производство очень высокой культуры. Технология его очень сложна и специфична, обслуживание аппаратуры требует овладения специальными навыками, ведь всё производство работает только в условиях строжайшей стерильности: стоит попасть в ферментатор лишь одной клетке микроорганизма другого вида, как всё производство может остановиться — «чужак» размножится и начнёт синтезировать совсем не то, что нужно человеку.
В настоящее время с помощью микробиологического синтеза производят антибиотики, ферменты, аминокислоты, полупродукты для дальнейшего синтеза разнообразных веществ, феромоны (вещества, с помощью которых можно управлять поведением насекомых), органические кислоты, кормовые белки и другие. Технология производства этих веществ хорошо отработана, получение их микробиологическим путём экономически выгодно.
В то же время идут поиски видов микроорганизмов, которые обладают способностью синтезировать в наибольших количествах другие необходимые вещества. В частности, учёные работают над тем, чтобы сделать выгодным производство с помощью микроорганизмов обычных химических продуктов: ацетона, различных спиртов, простых органических кислот, окиси пропилена и т. п. На микробиологической основе пытаются производить горючее: метан и спирт. Уже сейчас спирт, полученный микробиологическим путём, конкурирует с бензином по своим «рабочим» качествам, а также по показателям, очень важным с точки зрения охраны природы: продукты сгорания спирта не загрязняют окружающую среду.
Эти работы учёных важны ещё и по другой причине. Сейчас химическая промышленность для производства горючего, ацетона и других подобных веществ использует как исходное сырьё нефть, газ и уголь. Но их запасы не безграничны. А в микробиологической промышленности для производства химических продуктов могут использоваться (и уже частично используются) неограниченные, постоянно возобновляющиеся массы органического сырья, отходов, образующихся в сельском хозяйстве, лесной и деревообрабатывающей промышленности, очистных сооружениях городов и т. п. Разработка и внедрение эффективных технологий такого производства — задача, имеющая большое значение для экономики народного хозяйства.
Важным направлением биотехнологии является производство и использование так называемых иммобилизованных ферментов.
Использование ферментов — биологических катализаторов — очень заманчивая вещь. Ведь они по многим своим свойствам, прежде всего активности и избирательности действия (специфичности), намного превосходят катализаторы химические. Ферменты обеспечивают осуществление химических реакций без высоких температур и давлений, а ускоряют их в миллионы и миллиарды раз. При этом каждый фермент катализирует только одну определённую реакцию.
В пищевой и кондитерской промышленности ферменты применяются уже давно: многие из первых патентов ещё начала века касались производства ферментов именно для этих целей. Однако требования к этим препаратам тогда были не очень высокие — по существу, в производстве использовались не чистые ферменты, а различные вытяжки или полуразрушенные и высушенные клетки дрожжей или низших грибов. Ферменты (вернее, содержащие их препараты) использовали и в текстильной промышленности для отбеливания и обработки пряжи и хлопковых нитей.
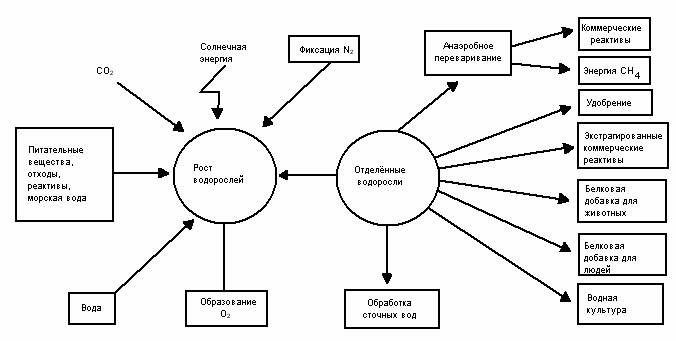
Возможные способы применения массовой культуры водорослей.
Биологические катализаторы можно использовать также не извлекая их из живых организмов, прямо в бактериальных клетках, например. Этот способ, собственно, есть основа всякого микробиологического производства, и применяется он издавна.
Гораздо заманчивее использовать чистые препараты ферментов и избавиться таким образом от побочных, сопутствующих жизнедеятельности микроорганизмов реакций. Создание производства, в котором используется биологический катализатор в чистом виде как реактив, сулит очень большие выгоды — повышается технологичность, возрастают во много тысяч раз производительность и чистота процессов. Но здесь возникает принципиальное затруднение: многие ферменты после их извлечения из клетки очень быстро инактивируются, разрушаются. Ни о каком многократном их использовании не может быть и речи.
Учёные нашли решение проблемы. Для того чтобы стабилизировать, или, как говорят, иммобилизовать, ферменты, сделать их устойчивыми, пригодными для многократного, длительного промышленного использования, ферменты присоединяют с помощью прочных химических связей к нерастворимым или растворимым носителям — ионообменным полимерам, полиорганосилоксанам, пористому стеклу, полисахаридам и т. п. В результате ферменты становятся устойчивыми и могут быть использованы многократно. (Эта идея была затем перенесена в микробиологию — возникла мысль иммобилизовать живые клетки. Иногда очень нужно, чтобы они в процессе микробиологического синтеза не загрязняли среду, не смешивались с синтезируемыми ими продуктами и вообще были бы больше похожи на химические реактивы. И такие иммобилизованные клетки были созданы; они успешно применяются, например, при синтезе стероидных гормонов — ценных лекарственных препаратов).
Разработка способа повышения устойчивости ферментов значительно расширяет возможности их использования. С помощью ферментов можно, например, получать сахар из растительных отходов, и этот процесс будет экономически рентабельным. Уже создана опытная установка для непрерывного производства сахара из клетчатки.
Иммобилизованные ферменты находят применение и в медицине. Так, в нашей стране для лечения сердечно-сосудистых заболеваний разработан препарат иммобилизованной стрептокиназы (препарат получил название «стрептодеказа»). Этот препарат можно вводить в сосуды для растворения образовавшихся в них тромбов. Растворимая в воде полисахаридная матрица (к классу полисахаридов относятся, как известно, крахмал и целлюлоза, близким к ним по строению был и подобранный полимерный носитель), к которой химически «привязана» стрептокиназа, значительно повышает устойчивость фермента, снижает его токсичность и аллергическое действие и не влияет на активность, способность фермента растворять тромбы.

Субстраты для получения белка одноклеточных для разных классов микроорганизмов.
Создание иммобилизованных ферментов, так называемая инженерная энзимология, — одно из новых направлений биотехнологий. Достигнуты лишь первые успехи. Но они существенно преобразили прикладную микробиологию, техническую биохимию и ферментную промышленность. Во-первых, в микробиологической промышленности сейчас актуальными стали разработки производства ферментов самой различной природы и свойства. Во-вторых, возникли новые области производства, связанные с получением именно иммобилизованных ферментов. В-третьих, создание новых ферментных препаратов открыло возможность организации ряда новых производств для получения нужных веществ с помощью биологические катализаторов.
Править] Плазмиды
Наибольшие успехи были достигнуты в области изменения генетического аппарата бактерий. Вводить новые гены в геном бактерии научились с помощью небольших кольцеобразных молекул ДНК — плазмид, присутствующих в бактериальных клетках. В плазмиды «вклеивают» необходимые гены, а затем такие гибридные плазмиды добавляют к культуре бактерий, например кишечной палочки. Некоторые из этих бактерий поглощают такие плазмиды целиком. После этого плазмида начинает реплицироваться в клетке, воспроизводя в клетке кишечной палочки десятки своих копий, которые обеспечивают синтез новых белков.
Править] Генная инженерия
Сейчас созданы и создаются ещё более остроумные методы введения генов в клетку прокариотов (организмов, не имеющих оформленного ядра и хромосомного аппарата). На очереди разработка методов введения новых генов в клетки эукариотов, прежде всего высших растений и животных организмов.
Но и то, что уже достигнуто, позволяет сделать очень многое в практике народного хозяйства. Возможности микробиологического производства значительно расширились. Благодаря генетической инженерии область микробиологического синтеза различных биологически активных соединений, полупродуктов для синтеза, кормовых белков и добавок и других веществ стала одной из наиболее окупаемых наук: вложение средств в перспективные биотехнологические исследования обещает получение высокого экономического эффекта.
Для селекционной работы, независимо от того, проводится она методами мутагенеза или «индустрии ДНК», учёные должны располагать многочисленными коллекциями микроорганизмов. Но сейчас даже выделение нового штамма природных микроорганизмов, ранее неизвестных науке, обходится на мировом «рынке бактериальных культур» приблизительно в 100 долларов. А для того, чтобы получить хороший промышленный штамм обычными селекционными методами, надо иногда затратить миллионы.
Сейчас уже существуют способы ускорить и удешивить эти процессы. Например, во Всесоюзном научно-исследовательском институте генетики и селекции микроорганизмов Главмикробиопрома был получен промышленный штамм-сверхпродуцент микроорганизма, синтезирующего треонин — незаменимую аминокислоту, которая в кормах сельскохозяйственных животных содержится в недостаточном количестве. Добавка треонина в корм повышает привесы животных на килограммы, что в масштабах страны оборачивается миллионами рублей прибыли, а самое главное — приростом мясной продукции животноводства.
Коллектив учёных института под руководством директора В. Г. Дебабова за основу для получения промышленного штамма взял обыкновенную кишечную палочку — повсеместно распространённый микроорганизм. Сначала были получены мутантные клетки, способные накапливать в среде избыток треонина. Затем в клетке были вызваны генетические изменения, которые привели к усилению биосинтеза аминокислот. Таким путём удалось получить штамм, который производил треонин, но в 10 раз меньше того количества, которое требовалось по соображениям рентабельности производства. Тогда в дело были выпущены методы генетической инженерии. С их помощью была увеличена «доза треонинового гена» в молекуле бактериальной ДНК. Причём количество генов, обусловливающих синтез треонина, было в молекуле ДНК клетки увеличено в несколько раз: одинаковые гены оказались как бы нанизанными один за другим в молекуле ДНК. Естественно, биосинтез треонина пропорционально увеличился и достиг уровня, достаточного для промышленного производства.
Правда, после этого штамм пришлось ещё улучшать, причём снова генетически. Сначала для того, чтобы культуру бактерий очистить от клеток, в которых плазмиды с «треониновым геном» исчезали в процессе размножения культуры. Для этого в клетки был «вшит» ген, содержащий закодированный сигнал к «самоубийству» клеток, в которых плазмид с «треониновым геном» после деления не оказывалось. Таким путём культура клеток самоочищалась от балластных микроорганизмов. Затем в клетки был введён ген, благодаря которому она могла развиваться на сахарозе (а не дорогих глюкозе и фруктозе, как раньше) и производить рекордные количества треонина.
По существу, полученный микроорганизм уже не был кишечной палочкой: манипуляции с его генетическим аппаратом привели к появлению принципиально нового организма, сконструированного вполне сознательно и целенаправленно. И эта сложнейшая многоступенчатая работа, имеющая огромное практическое значение, была проведена с помощью новых оригинальных методов генетической инженерии за очень короткий срок — всего за три года.
К 1981 г. в ряде институтов страны, и прежде всего в Институте биоорганической химии им. М. М. Шемякина АН СССР под руководством академика Ю. А. Овчиникова, были выполнены ещё более впечатляющие работы. Эти исследования приобрели сейчас форму чётких долгосрочных программ, по которым их развивают дальше ряд академических и отраслевых институтов. Эти исследования были направлены на то, чтобы осуществить поистине чудо — ввести в бактериальную клетку ген, выделенный из человеческого организма.
Работа велась сразу с несколькими генами: геном ответственным за синтез гормона инсулина, геном, обеспечивающим образование интерферона, и геном, контролирующим синтез гормона роста.
Прежде всего учёные поставили перед собой задачу «обучения» бактерии синтезу ценнейшего медицинского препарата — гормона инсулина. Инсулин необходим для лечения сахарного диабета. Этот гормон надо вводить больным постоянно, а производство его традиционным способом (из поджелудочных желез убойного скота) сложно и дорого. К тому же молекулы инсулина свиньи или крупного рогатого скота отличаются от молекул инсулина человека, и естественно, что активность их в организме человека ниже, чем активность человеческого инсулина. Кроме того, инсулин — хотя и небольшой по размерам, но всё же белок, и в организме человека со временем накапливаются антитела к нему: организм борется против чужеродных белков, отторгает их. Поэтому введённый бычий или свиной инсулин может начать необратимо инактивироваться, нейтрализовываться этими антителами и в результате может исчезнуть прежде, чем успеет оказать лечебное действие. Чтобы этого не произошло, необходимо вводить в организм вещества, предотвращающие этот процесс, но они сами по себе не безразличны для организма.
Человеческий инсулин можно было бы получать с помощью химического синтеза. Но этот синтез настолько сложен и дорог, что его проводили только в экспериментальных целях, а полученные количества инсулина были недостаточны даже для одной инъекции. Это был, скорее, символической синтез, доказательство того, что химики могут синтезировать в пробирке настоящий белок.
Учитывая всё это, учёные и поставили перед собой такую сложную и очень важную задачу — наладить биохимическое производство человеческого инсулина. Был получен ген, обеспечивающий синтез инсулина. С помощью методов генетической инженерии этот ген был введён в бактериальную клетку, которая в результате приобрела способность синтезировать гормон человека.
Столь же большой интерес и не меньшее (а может быть, и большее) значение имела работа, выполненная в том же институте, по введению методами генетической инженерии в бактериальную клетку гена, ответственного за синтез интерферона человека. (Интерферон — это белок, играющий исключительно важную роль в борьбе организма против вирусных инфекций.) Ген интерферона также был введён в клетку кишечной палочки. Созданные штаммы отличались высоким выходом интерферона, обладающего мощным противовирусным действием. Сейчас уже получены первые промышленные партии человеческого интерферона. Осуществление промышленного производства интерферона — очень важное достижение, так как предполагают, что интерферон обладает также и противоопухолевой активностью.
В институте АН СССР были проведены работы по созданию бактериальных клеток, продуцирующих соматотропин — гормон роста человека. Ген этого гормона был выделен из гипофиза и методами генетической инженерии встроен в более сложную молекулу ДНК, которую затем ввели в генетический аппарат бактерии. В результате бактерия приобрела способность синтезировать человеческий гормон. Эта бактериальная культура, так же как и культура бактерий с введённым геном инсулина, апробируется для промышленного получения человеческих гормонов в микробиологическом производстве.
Это лишь отдельные примеры работ по введению генов высших организмов в клетки бактерий. Есть ещё немало подобных интересных и перспективных работ.
Вот ещё один пример. Английские биохимики из плодов одного африканского кустарника выделили довольно крупный белок (около 200 аминокислотных остатков) — тауматин. Этот белок оказался в 100 тыс. раз слаще сахарозы. Сейчас во всём мире думают над созданием заменителей сахара, который при большом потреблении далеко не безвреден для организма. Поэтому тауматин — природный продукт, не требующий специальных токсикологических испытаний, — привлёк пристальное внимание: ведь ничтожные его добавки в кондитерские изделия позволяют просто исключить использование сахара. Учёные решили, что получать тауматин проще и выгоднее не из естественного источника, а микробиологическим синтезом с помощью бактерий, в которые введён ген тауматина. И эту работу выполнили, введя этот ген во всё ту же кишечную палочку. Сейчас пока заменитель сахара тауматин (под названием «талин») производят из природного источника, но не за горами и его микробиологическое производство.
Пока речь шла о введении генов в клетки бактерий. Но это не означает, что не ведётся работа и по введению искусственных генов в высшие организмы — растения и животных. Здесь не меньше, а гораздо больше привлекательных идей. Практическое воплощение некоторых из них будет иметь для человечества исключительно важное значение. Так, известно, что высшие растения не могут усваивать азот атмосферы: они получают его из почвы в виде неорганических солей или в результате симбиоза с клубеньковыми бактериями. Осуществление идеи — ввести гены этих бактерий в растения — может привести к коренным революционным изменениям в сельском хозяйстве.
Как же обстоят дела с введением генов в генетический аппарат эукариотов? Основная трудность здесь заключается в том, что изменить генотип всех клеток многоклеточного организма невозможно. Поэтому надежды связывают с созданием методов генетической инженерии, предназначенных для работы с культурами клеток растений и с одноклеточными растениями.
Введение синтетических генов в искусственно культивируемые клетки может привести к получению модифицированного растения: при определённых условиях изолированные клетки могут превращаться в целые растения. И в таком растении должны действовать и передаваться по наследству искусственно введённые в исходную клетку гены.
Здесь помимо перспектив успешного использования методов генетической инженерии вырисовывается ещё одно преимущество биотехнологии — методом клеточной биотехнологии из одного растения можно получить миллионы одинаковых растений, а не десятки, как при использовании семян. Клеточная технология не требует больших площадей, не зависит от погодных условий и отличается огромной производительностью.
Советские учёные сейчас исследуют ещё один путь введения генов в клетки растений — создают симбиотическое сообщество, где в протопласты растений (они лишены целлюлозной оболочки) пытаются внедрить цианобактерии, которые способны и к фотосинтезу, и к азотфиксации.
Определённые перспективы имеются и в области использования методов генетической инженерии в работе с животными, во всяком случае существует принципиальная возможность переноса генетического материала в клетки животных. Особенно убедительно это показано на гибридомах. Гибридома — это клетка, образованная из лимфоцита, вырабатывающего антитела, и опухолевой клетки, способной к неограниченному размножению, и сочетающая оба эти свойства. С помощь гибридом можно получать высокоспецифичные антитела. Метод гибридом — это ещё один биотехнологический приём получения ценных белков.
Космическая биотехнология При реализации программ пилотируемых полетов в бывшем СССР сложился научно-технический потенциал в области космической биотехнологии с участием головных организаций Росавиакосмоса, Минмедпрома, РАН и РАМН, которые создали аппаратурно-методическую базу, необходимую для осуществления биотехнологических экспериментов в условиях орбитального полета. За 15 летний период выполнен ряд программ биотехнологических экспериментов, их результаты внедрены в технологии по производству различных биологически активных веществ (антибиотиков, иммунностимуляторов и др.). С использованием методов космической биотехнологии создан целый ряд новейших лечебных и диагностических препаратов. Накопленный опыт позволил определить наиболее перспективные направления развития космической биотехнологии:· получение высококачественных кристаллов биологически значимых веществ в целях определения их пространственной структуры и создания новых препаратов для медицины, фармакологии, ветеринарии, других отраслей народного хозяйства и различных областей науки;· получение и отбор в условиях микрогравитации улучшенных, а также рекомбинантных промышленных штаммов микроорганизмов, продуцентов биологически активных веществ для медицины, фармакологии, сельского хозяйства и экологии; электрофоретическое разделение биологических субстанций, в частности, тонкая высокопроизводительная очистка генно-инженерных и вирусных белков, преимущественно медицинского назначения, а также выделение специфических клеток, характеризующихся требуемыми секреторными функциями;· исследование влияния факторов космического полета на биологические объекты и физико-химические характеристики биотехнологических процессов с целью расширения фундаментальных знаний в области биологии и биотехнологии. В 1989 году РКК «Энергия» им. С. П. Королёва и РАО «Биопрепарат», объединив усилия в исследованиях по одной из перспективных областей космической деятельности, создали лаборатории космической биотехнологии. Научное руководство работами в области биотехнологии в рамках российской национальной программы на орбитальной станции «Мир» и российском сегменте международной космической станции осуществляет председатель секции «Космическая биотехнология» КНТС Росавиакосмоса и РАН, Заслуженный деятель науки Российской Федерации, профессор Юрий Тихонович Калинин. Координация работ, обеспечение создания и предполетной подготовки бортовой научной аппаратуры, биологических материалов при реализации биотехнологических проектов, а также обработка и анализ полученных результатов осуществляются специализированными лабораториями космической биотехнологии в РАО «Биопрепарат» (на базе АООТ «Биохиммаш») и в РКК «Энергия» им. С. П. Королёва. Для непосредственной реализации экспериментов на борту орбитальных станций разработан комплекс мероприятий по их организации, обеспечению и сопровождению на всех стадиях проведения:· подготовка научных экспериментов и аппаратуры, тренировка экипажей совместно с Российским государственным научно-исследовательским и испытательным центром подготовки космонавтов им. Ю. А. Гагарина;· доставка научной аппаратуры на орбитальный комплекс; материально-техническое обеспечение экспериментов на борту орбитального комплекса; планирование, подготовка и сопровождение экспериментов в Центре Управления Полетами;· возвращение результатов экспериментов с орбиты и их доставка с места посадки спускаемого аппаратам лабораторию. Вышеупомянутыми лабораториями космической биотехнологии разработаны пакеты документов, необходимых для реализации космических экспериментов, в том числе методики предполетной подготовки, паспорта и сертификаты и др. разрешительная документация. Мы готовы, по выбору заказчика, дать необходимые научные консультации в данной области, а также подготовить и провести космические эксперименты с любыми биологическими объектами. Очевидна неоднократно подтвержденная нами в коммерческих проектах с зарубежными фирмами перспективность получения в условиях микрогравитации высококачественных кристаллов биологических веществ. Они позволили с высокой точностью изучить пространственную структуру различных биополимеров и использовать результаты для создания качественно новых лечебных, профилактических и диагностических препаратов. Наш опыт работы с микробиологическими культурами биодеградантов нефти и нефтепродуктов, а также со штаммами, используемыми для препаратов средств защиты растений, культурами клеток высших растений, позволил получить варианты культур после их экспозиции в космосе, значительно превышающие по активности исходные штаммы. Эксперименты по рекомбинации микроорганизмов в условиях орбитального полета показали реальную возможность 100 % передачи генетического материала между отдаленными видами, что позволяет получать уникальные гибриды с новыми заданными свойствами. Многочисленные результаты экспериментов, проведенных в условиях микрогравитации по электрофоретической очистке и разделению белковых и клеточных биообъектов, подтвердили возможность и эффективность использования электрофоретических методов в целях наработки опытных и опытно-промышленных партий особо чистых и высокооднородных хозяйственно-ценных биологически-активных веществ. Мы готовы по Вашим заказам на нашем или ином оборудовании обеспечить проведение исследований по кристаллизации биологических объектов в космосе, получению улучшенных или рекомбинантных штаммов, а также электрофорезу и другим направлениям исследований, как по Вашему заказу, так и в кооперации. По нашему мнению весьма перспективным направлением, как в научном так и в коммерческом плане может служить проект по созданию универсальной установки по выращиванию и получению кристаллических белков в условиях космического полета. Описание проекта прилагается. Мы рассмотрим также любые предложения от заинтересованных лиц по подготовке и проведению космических биотехнологических экспериментов, выполним экспертизу их реализуемости и обеспечим осуществление предложенных проектов на коммерческой основе. ЦЕЛИ И ЗАДАЧИ ПРОЕКТАПроект осуществляется усилиями РАО «Биопрепарат» и потенциальными участниками, заинтересованными в разработке перспективной биотехнологической научной аппаратуры и получении в условиях космического полета конкурентоспособной биопродукции. Основной целью проекта по кристаллизации биопрепаратов в условиях орбитального полета является создание и эксплуатация на международной космической станции (МКС) биокристаллизационной аппаратуры нового поколения, способной обеспечить получение крупных однородных кристаллов большого спектра биообъектов, а также оперативное получение на Земле видео и телеметрической информации об основных параметрах процесса и получаемых результатах. При организации работ в рамках проекта ставятся следующие задачи:· отработка механизмов взаимодействия между сторонами участниками проекта по организационно-методическим, техническим, научным и экономическим вопросам;· на базе российских биокристаллизаторов и зарубежной электронной и видео аппаратуры изготовить макетные и летные образцы биокристаллизационной аппаратуры с характеристиками, превышающими известные мировые аналоги по эффективности и надежности;· осуществлять на МКС эксплуатацию созданной аппаратуры; как по индивидуальным национальным программам сторон участников, так и по совместным научным или коммерческим проектам;· поиск путей и способов реализации научных результатов, полученных в ходе полетных экспериментов на основе взаимных интересов сторон участников проекта. КРАТКИЕ ТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ АППАРАТУРЫНиже представлены краткие технические характеристики аппаратуры для кристаллизации биообъектов, создаваемой на базе российских разработок. Универсальный биокристаллизаторФункционально аппаратура представляет собой комплект универсальных кристаллизационных кассет, позволяющих реализовать кристаллизацию белков (или др. биообъектов) различными методами. Аппаратура обеспечивает:· многоуровневую и высоконадежную герметизацию камер с рабочими растворами;· быстрое выполнение операций по раздельной заправке камер кристаллизационных кассет растворами белка (или другого биополимера) и осадителя;· реализацию нескольких методов кристаллизации в одной кассете;· высокую воспроизводимость характеристик процесса в различных кристаллизационных ячейках универсальной кассеты;· высокую степень взаимозаменяемости основных функциональных элементов биокристаллизатора; · удобное и быстрое выполнение операций стерилизации, сборки, проверки герметичности и заправки рабочими растворами;· удобное и неразрушающее извлечение полученных кристаллов;· высокую надежность и ремонтопригодность;· ручную и автоматическую активацию/деактивацию процесса кристаллизации;· измерение и регистрацию температуры кристаллизационных кассет на всех этапах транспортировки и эксплуатации;· высокий коэффициент использования массы полезного груза на этапах выведения на орбиту и возвращения на Землю;· низкая требовательность к средствам доставки и возвращения;· гибкость построения и использования научной программы при минимальных используемых ресурсах МКС;· возможность модульного наращивания кристаллизационных ячеек в зависимости от требований заказчиков. Доставка на борт МКС и возвращение на Землю кассет универсального биокристаллизатора осуществляется в термоизолирующем возвращаемом контейнере (ТВК) с автономным регистратором температуры. СОСТАВ АППАРАТУРЫПолная конфигурация аппаратуры имеет следующий состав:· комплект кассет универсального биокристаллизатора — 12 шт. (конфигурация кассет определяется постановщиком эксперимента);· термоизолирующий возвращаемый контейнер (ТВК) с автономным регистратором температуры;· ручной привод кассет;· термостат биотехнологический универсальный (ТБУ) для активного термостатирования кассет в полуавтоматическом режиме;· блок электропривода активации/деактивации кассет в ТБУ;· блок управления электроприводом;· система видеоконтроля кристаллизационных ячеек в ТБУ;· блок наблюдения и управления системой видеоконтроля и интерфейса (СВИ) с TV-системой МКС;· комплект соединительных кабелей. Каждая из универсальных кристаллизационных кассет конструктивно выполнена моноблочно. Кассета включает в себя 4 автономные кристаллизационные ячейки. Каждая кристаллизационная ячейка, в свою очередь, имеет от одной до трех кристаллизационных (белковых) камер и одну или несколько камер для раствора осадителя.