Биохимические показатели биологических жидкостей человека 2 страница
Живой организм – сложная, упорядоченная иерархическая структурная организация. Уровень организации живой материи повышается в ходе эволюции. Формирование каждой следующей ступени иерархии уровней происходит на основе предыдущей, которая структурно в неё входит. Существует множество теорий о структурной организации живой материи. Наиболее известная из них оценивает иерархию по критерию масштабности. Согласно ей, жизнь имеет следующие уровни организации:
1. Молекулярный уровень - отражает особенности химизма живого вещества, а также механизмы и процессы передачи генной информации
2. Клеточный и субклеточный уровни - отражают особенности специализации клеток, а также внутриклеточные структуры. На этом уровне происходят процессы жизнедеятельности (обмен веществ, питание, дыхание, раздражимость и т. д.)
3. Организменный и органно-тканевый уровни - отражают признаки отдельных особей, их строение, физиологию, поведение, а также строение и функции органов и тканей живых существ
4. Популяционно-видовой уровень - образуется свободно скрещивающимися между собой особями одного и того же вида, совокупность особей одного вида
5. Уровень биогеоценозов - структуры, состоящие из участков Земли с определенным составом живых и неживых компонентов, представляющих единый природный комплекс – экосистему
6. Биосферный - вся совокупность живых организмов Земли вместе с окружающей их природной средой
Еще одним качеством, благодаря которому возможна жизнь - это свойство живых организмов к самовоспроизведению. Самовоспроизведение свойственно целым организмам, отдельным их органам, тканям, клеткам, клеточным включениям и многим органеллам. Самовоспроизведение осуществляется посредством вегетативного, полового и бесполого размножений, у животных - путем деления, живорождения, яйцерождения и яйцеживорождения. В основе самовоспроизведения лежит образование новых молекул и структур, которое обусловлено информацией, заложенной в нуклеиновой кислоте ДНК,. Самовоспроизведение тесно связано с явлением наследственности: любое живое существо рождает себе подобных, путем реализации механизма матричного синтеза ДНК.
2. Гетеротрофные и аутотрофные организмы: различия по питанию и источникам энергии. Катаболизм и анаболизм.
Живые клетки постоянно нуждаются в органических и неорганических веществах, а также в химической энергии, которую они получают преимущественно из АТФ (АТР). По способу удовлетворении этих потребностей организмы подразделяются на автотрофные и гетеротрофные. Автотрофные организмы, к которым принадлежат растения и многие микроорганизмы, могут синтезировать органические молекулы из неорганических предшественников в процессах хемо- и фотосинтеза . Автотрофы обеспечивают существование все других организмов на планете.
Гетеротрофы, например животные и грибы, зависят от получения органических веществ с пищей. Так как большая часть этих питательных веществ (белки, углеводы, нуклеиновые кислоты и липиды) не могут утилизироваться непосредственно, они сначала разрушаются до более мелких фрагментов катаболическим путем . Возникающие метаболиты (в совокупности их называют иногда «пулом метаболитов») затем катаболизируются с высвобождением свободной энергии или используются в анаболических путях для синтеза более сложных молекул.
Процесс обмена веществ определяется двумя сопряженными процессами: анаболизма и катаболизма.
Анаболизм - совокупность химических процессов синтеза собственных органических соединений из полученных питательных веществ, идущий с потреблением энергии. В результате такого обмена из питательных веществ, поступающих в организм, строятся свойственные организму структурные молекулы, которые, в свою очередь, идут уже на создание новых функциональных единиц живого организма, что является основой ассимиляции.
Катаболизм - процесс метаболического распада, разложения на более простые вещества или окисления какого-либо вещества, обычно протекающий с высвобождением энергии в виде тепла и в виде АТФ. Катаболические реакции лежат в основе диссимиляции: утраты сложными веществами своей специфичности для данного организма в результате распада до более простых.
3. Многомолекулярные системы (метаболические цепи, мембранные процессы, системы синтеза биополимеров, молекулярные регуляторные системы) как основные объекты биохимического исследования.
Как известно, биохимия - это наука изучающая химическую основу жизни как таковой. В её рамках изучаются все основные молекулярные процессы жизнедеятельности организма.
1. Метаболические цепи - процессы последовательных превращений исходного вещества, приводящие к образованию некоторого продукта. Все метаболические пути можно подразделить на анаболические и катаболические. Метаболическая цепь, состоящая из реакций, протекающих внутри одной системы, называется внутренней. Метаболическая цепь, реакции которой протекают в разных системах, называется межсистемной. Одно и то же вещество может участвовать в различных превращениях. В подобных случаях наблюдается пересечение различных метаболических цепей. Следствием такого пересечения является возникновение метаболической сети биологической системы. Понимание функционирования одного звена цепи позволяет проводить корректировку нарушений протекания определенного биохимического процесса в организме.
2. Мембранные процессы – это физико-химические процессы, происходящие на поверхности клеточных мембран. К ним относят: процессы активного транспорта веществ, проведение и передача биопотенциалов, рецепция и др. Изучение природы мембранных процессов позволяет на клеточном уровне понимать характер протекающих процессов жизнедеятельности и их патологию.
3. Система синтеза биополимеров – совокупность ферментативных механизмов, которые обеспечивают воспроизведение специфических для данного организма видов высокомолекулярных соединений. Биополимеры играют важнейшую роль во всех процессах жизнедеятельности организма. Поэтому особенно важно понимать суть процессов их воспроизведения.
4. Молекулярные регуляторные системы- системы, направленные на поддержание гомеостаза. Данная системы включают в себя ряд биохимических процессов. Нарушение хотя бы одного звена в системе поддержания гомеостаза, способно вызвать необратимые изменения, которые могут привести к гибели организма.
4. Уровни структурной организации живого. Биохимия как молекулярный уровень изучения явлений жизни. Биохимия и медицина (медицинская биохимия).
Жизнь имеет следующие уровни организации:
1. Молекулярный уровень - отражает особенности химизма живого вещества, а также механизмы и процессы передачи генной информации
2. Клеточный и субклеточный уровни - отражают особенности специализации клеток, а также внутриклеточные структуры. На этом уровне происходят процессы жизнедеятельности (обмен веществ, питание, дыхание, раздражимость и т. д.)
3. Организменный и органно-тканевый уровни - отражают признаки отдельных особей, их строение, физиологию, поведение, а также строение и функции органов и тканей живых существ
4. Популяционно-видовой уровень - образуется свободно скрещивающимися между собой особями одного и того же вида, совокупность особей одного вида
5. Уровень биогеоценозов - структуры, состоящие из участков Земли с определенным составом живых и неживых компонентов, представляющих единый природный комплекс – экосистему
6. Биосферный - вся совокупность живых организмов Земли вместе с окружающей их природной средой
Молекулярный уровень выступает основой для всей жизнедеятельности любого организма на планете, это уровень функционирования биологических макромолекул - биополимеров: нуклеиновых кислот, белков, полисахаридов, липидов, стероидов. На молекулярном уровне происходят различные процессы жизнедеятельности живых организмов: обмен веществ, превращение энергии, формирование биопотенциалов клетки. С помощью молекулярного уровня осуществляется передача наследственной информации, образуются отдельные органоиды, происходят ферментативные процессы. Понимание химических процессов, происходящих в организме – является одной из ключевых задач биологической химии, поэтому она выступает на молекулярном уровне организации живого.
Биохимия оказывает все более глубокое воздействие на медицину. Так, например, определение активности ферментов играет в настоящее время важную роль в клинической диагностике. Содержание определенных ферментов в сыворотке крови может служить ценным критерием при диагностике недавно перенесенного инфаркта миокарда. Кроме того, биохимия постепенно создает основу для рационального назначения лекарственных препаратов. Исключительную важность представляет выяснение молекулярных механизмов некоторых заболеваний, например серповидно-клеточной анемии или большого числа врожденных нарушений метаболизма, исследованных к настоящему времени. Быстрое развитие биохимии в последние годы позволило исследователям приступить к изучению самых острых, коренных проблем биологии и медицины.
5. Основные разделы и направления в биохимии: биоорганическая химия, динамическая и функциональная биохимия, молекулярная биология.
Биохимия включает в себя:
1) Биоорганическая химия - изучает вещества, лежащие в основе процессов жизнедеятельности, в непосредственной связи с познанием их биологической функции. Основные объекты БОХ — биополимеры, превращения которых составляют химическую сущность биологических процессов, и биорегуляторы, которые химически регулируют обмен веществ. БОХ занимается получением этих веществ в химически чистом состоянии, установлением строения, синтезом, выяснением зависимостей между строением и биологическими свойствами, изучением химических аспектов механизма биологического действия биополимеров, а также природных и синтетических биорегуляторов. Характерная особенность БОХ. — использование всего комплекса химических и физических методов индивидуализации веществ и выяснение их строения.
2) Динамическая биохимия - раздел биохимии, изучающий обмен веществ в организме от момента поступления в него питательных веществ до образования конечных продуктов обмена, механизмы нейтрализации токсических продуктов, выведения их из организма и регуляции скорости соответствующих превращений.
3) Функциональная биохимия - раздел биохимии, изучающий химические превращения, лежащие в основе функций органов, тканей и организма в целом.
4) Молекулярная биология - наука, ставящая своей задачей познание природы явлений жизнедеятельности путём изучения биологических объектов и систем на уровне, приближающемся к молекулярному, а в ряде случаев и достигающем этого предела. Конечной целью при этом является выяснение того, каким образом и в какой мере характерные проявления жизни, такие, как наследственность, воспроизведение себе подобного, биосинтез белков, возбудимость, рост и развитие, хранение и передача информации, превращения энергии, подвижность и т. д., обусловлены структурой, свойствами и взаимодействием молекул биологически важных веществ, в первую очередь двух главных классов высокомолекулярных биополимеров.
6. История изучения белков. Представление о белках как важнейшем классе органических веществ и структурно-функциональном компоненте организма человека.
Белки были выделены в отдельный класс биологических молекул в XVIII веке в результате работ французского химика Антуана Фуркруа и других учёных, в которых было отмечено свойство белков коагулировать (денатурировать) под воздействием нагревания или кислот. В то время были исследованы такие белки, как альбумин («яичный белок»), фибрин (белок из крови) и глютен из зерна пшеницы.
Голландский химик Геррит Мульдер провёл анализ состава белков и выдвинул гипотезу, что практически все белки имеют сходную эмпирическую формулу.
Термин «протеин» для обозначения подобных молекул был предложен в 1838 году шведским химиком Якобом Берцелиусом . Мульдер также определил продукты разрушения белков — аминокислоты и для одной из них (лейцина) с малой долей погрешности определил молекулярную массу — 131 дальтон.
В 1836 Мульдер предложил первую модель химического строения белков. Основываясь на теории радикалов он сформулировал понятие о минимальной структурной единице состава белка, C16H24N4O5, которая была названа «протеин», а теория — «теорией протеина» . По мере накопления новых данных о белках теория стала неоднократно подвергаться критике, но до конца 1850-х несмотря на критику ещё считалась общепризнанной.
К концу XIX века было исследовано большинство аминокислот, которые входят в состав белков. В 1894 году немецкий физиолог Альбрехт Коссель выдвинул теорию, согласно которой именно аминокислоты являются основными структурными элементами белков.
В начале XX века немецкий химик Эмиль Фишер экспериментально доказал, что белки состоят из аминокислотных остатков, соединённых пептидными связями. Он же осуществил первый анализ аминокислотной последовательности белка и объяснил явление протеолиза. Сложность выделения чистых белков затрудняла их изучение. Поэтому первые исследования проводились с использованием тех полипептидов, которые могли быть очищены в большом количестве, то есть белков крови, куриных яиц, различных токсинов, а также пищеварительных/метаболических ферментов, выделяемых после забоя скота.
Идея о том, что вторичная структура белков — результат образования водородных связей между аминокислотами, была высказана Уильямом Астбери в 1933 году, но Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру белков. Позднее Уолтер Каузман, опираясь на работы Кая Линдерстрём-Ланга, внёс весомый вклад в понимание законов образования третичной структуры белков и роли в этом процессе гидрофобных взаимодействий.
В 1949 году Фред Сенгер определил аминокислотную последовательность инсулина, продемонстрировав таким способом, что белки — это линейные полимеры аминокислот, а не их разветвлённые (как у некоторых сахаров) цепи, коллоиды или циклолы.
Первые структуры белков, основанные на дифракции рентгеновских лучей на уровне отдельных атомов были получены в 1960-х годах и с помощью ЯМР в 1980-х годах.
В XXI веке исследование белков перешло на качественно новый уровень, когда исследуются не только индивидуальные очищенные белки, но и одновременное изменение количества и посттрансляционных модификаций большого числа белков отдельных клеток, тканей или организмов.
Белки (протеины, полипептиды]) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью -аминокислот. Для живых организмов характерны широкое разнообразие белковых структур и их высокая упорядоченность; последняя существует во времени и пространстве. Удивительная способность живых организмов к воспроизведению себе подобных также связана с белками. Сократимость, движение – непременные атрибуты живых систем – имеют прямое отношение к белковым структурам мышечного аппарата. Наконец, жизнь немыслима без обмена веществ, постоянного обновления составных частей живого организма, т.е. без процессов анаболизма и катаболизма (этого удивительного единства противоположностей живого), в основе которых лежит деятельность каталитически активных белков – ферментов.
Таким образом, белки (белковые вещества) составляют основу и структуры, и функции живых организмов. Подсчитано, что в природе примерно 1010–1012 различных белков, обеспечивающих существование около 106 видов живых организмов различной сложности организации начиная от вирусов и кончая человеком. Каждый организм характеризуется уникальным набором белков. Фенотипические признаки и многообразие функций обусловлены специфичностью объединения этих белков, во многих случаях в виде над- и мультимолекулярных структур, в свою очередь определяющих ультраструктуру клеток и их органелл.
7. Аминокислоты, входящие в состав белков, их строение и свойства. Пептидная связь. Первичная структура белков.
-Аминокислоты представляют собой производные карбоновых кислот, у которых один водородный атом, у -углерода, замещен на аминогруппу (—NH2).
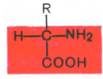
Аминокислоты будут отличаться друг от друга химической природой радикала R, представляющего группу атомов в молекуле аминокислоты, связанную с -углеродным атомом и не участвующую в образовании пептидной связи при синтезе белка. Почти все -амино- и -карбоксильные группы участвуют в образовании пептидных связей белковой молекулы, теряя при этом свои специфические для свободных аминокислот кислотно-основные свойства. Поэтому все разнообразие особенностей структуры и функции белковых молекул связано с химической природой и физико-химическими свойствами радикалов аминокислот. Именно благодаря им белки наделены рядом уникальных функций, не свойственных другим биополимерам, и обладают химической индивидуальностью. В состав белков входят 20 природных аминокислот.
Кислотно-основные свойства. Эти свойства аминокислот определяют многие физико-химические и биологические свойства белков. На этих свойствах основаны, кроме того, почти все методы выделения и идентификации аминокислот. Аминокислоты легко растворимы в воде. Они кристаллизуются из нейтральных водных растворов в форме биполярных (амфотерных) ионов, а не в виде недиссоциированных молекул. В связи с этим, они могут проявлять как основные, так и кислотные свойства, что зависит еще от природы входящего в их состав радикала.
Стереохимия аминокислот. Важнейшим свойством аминокислот, освобождающихся в процессе гидролиза природных белков в условиях, исключающих рацемизацию, является их оптическая активность. Это свойство связано с наличием в молекуле всех природных аминокислот (за ислючением глицина) в -положении асимметрического атома углерода. Стереохимию аминокислот принято оценивать не по оптическому вращению, а исходя из абсолютной конфигурации всех четырех замещающих групп, расположенных вокруг асимметрического атома углерода в вершинах модели тетраэдра. Абсолютную конфигурацию аминокислот принято соотносить стереохимически с соединением, произвольно взятым для сравнения, а именно с глицериновым альдегидом, также содержащим асимметрический атом углерода. Все аминокислоты, образующиеся при гидролизе природных белков в условиях, исключающих рацемизацию, принадлежит к L-ряду. Таким образом, природные аминокислоты имеют пространственное расположение, аналогичное конфигурации L-глицеринового альдегида.
Пептидная связь — вид амидной связи, возникающей при образовании белков и пептидов в результате взаимодействия -аминогруппы (—NH2) одной аминокислоты с -карбоксильной группой (—СООН) другой аминокислоты. Из двух аминокислот (1) и (2) образуется дипептид (цепочка из двух аминокислот) и молекула воды. По этой же схеме рибосома генерирует и более длинные цепочки из аминокислот: полипептиды и белки.
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка. Первичная структура предопределяет все дальнейшие виды организации белковой молекулы.
8. Зависимость биологических свойств белков от первичной структуры. Видовая специфичность первичной структуры белков (инсулины разных животных).
Анализ данных о первичной структуре белков позволяет сделать следующие общие выводы.
1. Первичная структура белков уникальна и детерминирована генетически. Каждый индивидуальный гомогенный белок характеризуется уникальной последовательностью аминокислот: частота замены аминокислот приводит не только к структурным перестройкам, но и к изменениям физико-химических свойств и биологических функций.
2. Стабильность первичной структуры обеспечивается в основном главновалентными пептидными связями; возможно участие небольшого числа дисульфидных связей.
3. В полипептидной цепи могут быть обнаружены разнообразные комбинации аминокислот; в полипептидах относительно редки повторяющиеся последовательности.
4. В некоторых ферментах, обладающих близкими каталитическими свойствами, встречаются идентичные пептидные структуры, содержащие неизменные (инвариантные) участки и вариабельные последовательности аминокислот, особенно в областях их активных центров. Этот принцип структурного подобия наиболее типичен для ряда протеолитических ферментов: трипсина, химотрипсина и др.
5. В первичной структуре полипептидной цепи детерминированы вторичная, третичная и четвертичная структуры белковой молекулы, определяющие ее общую пространственную конформацию.
Первичная структура инсулина у разных биологических видов несколько различается, как различается и его важность в регуляции обмена углеводов. Наиболее близким к человеческому является инсулин свиньи, который различается с ним всего одним аминокислотным остатком: в 30 положении B-цепи свиного инсулина расположен аланин, а в инсулине человека —треонин; бычий инсулин отличается тремя аминокислотными остатками.
9. Конформация пептидных цепей в белках (вторичная и третичная структуры). Слабые внутримолекулярные взаимодействия в пептидной цепи; дисульфидные связи.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Ниже приведены самые распространённые типы вторичной структуры белков:
1) -спирали — плотные витки вокруг длинной оси молекулы, один виток составляют 3,6 аминокислотных остатка, и шаг спирали составляет 0,54 нм (так что на один аминокислотный остаток приходится 0,15 нм), спираль стабилизирована водородными связями между H и O пептидных групп, отстоящих друг от друга на 4 звена. Спираль построена исключительно из одного типа стереоизомеров аминокислот (L). Хотя она может быть как левозакрученной, так и правозакрученной, в белках преобладает правозакрученная. Спираль нарушают электростатические взаимодействия глутаминовой кислоты, лизина, аргинина. Расположенные близко друг к другу остатки аспарагина, серина, треонина и лейцина могут стерически мешать образованию спирали, остатки пролина вызывает изгиб цепи и также нарушает -спирали.
2) -листы (складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,347 нм на аминокислотный остаток) в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в -спирали. Эти цепи обычно направлены N-концами в противоположные стороны (антипараллельная ориентация). Для образования -листов важны небольшие размеры боковых групп аминокислот, преобладают обычно глицин и аланин.
Стабильность вторичной структуры обеспечивается в основном водородными связями (определенный вклад вносят и главновалентные связи – пептидные и дисульфидные). Водородная связь представляет собой слабое электростатическое притяжение (взаимодействие, связь) между одним электроотрицательным атомом (например, кислородом или азотом) и водородным атомом, ковалентно связанным со вторым электроотрицательным атомом. По современным представлениям, водородная связь включает не только электростатические силы притяжения между полярными группами. но и электронные связи такого же типа, как в ряде комплексных соединений. Водородные связи, являясь нековалентными, отличаются малой прочностью. Поскольку в белковой молекуле число водородных связей очень велико (в образование водородных связей вовлечены все пептидные группы), они в сумме обеспечивают скручивание полипептидной цепи в спиральную структуру, сообщая ей компактность и стабильность.
Третичная или трёхмерная структура— пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль. В стабилизации третичной структуры принимают участие:
1) диcульфидная связь — ковалентная связь между двумя атомами серы, входящими в состав серусодержащей аминокислоты цистеина. Образующие дисульфидную связь аминокислоты могут находиться как в одной, так и в разных полипептидных цепях белка. Дисульфидные связи образуются в процессе посттрансляционной модификации белков и служат для поддержания третичной и четвертичной структур белка;
2) ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
3) водородные связи;
4) гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
10.Основы функционирования белков. Активный центр белков и его специфическое взаимодействие с лигандом как основа биологической функции всех белков. Комплементарность взаимодействия молекул белка с лигандом. Обратимость связывания.
Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей его от остальных белков. Набор индивидуальных белков выполняет в клетке множество разнообразных и сложных функций. Необходимое условие для функционирования белков - присоединение к нему другого вещества, которое называют "лиганд". Лигандами могут быть как низкомолекулярные вещества, так и макромолекулы. Взаимодействие белка с лигандом высокоспецифично и обратимо, что определяется строением участка белка, называемого центром связывания белка с лигандом или активным центром.
Активный центр белков - определённый участок белковой молекулы, как правило, находящийся в её углублении ("кармане"), сформированный радикалами аминокислот, собранных на определённом пространственном участке при формировании третичной структуры и способный комплементарно связываться с лигандом. В линейной последовательности полипептидной цепи радикалы, формирующие активный центр, могут находиться на значительном расстоянии друг от друга.Уникальные свойства активного центра зависят не только от химических свойств формирующих его аминокислот, но и от их точной взаимной ориентации в пространстве. Поэтому даже незначительные нарушения общей конформации белка в результате точечных изменений его первичной структуры или условий окружающей среды могут привести к изменению химических и функциональных свойств радикалов, формирующих активный центр, нарушать связывание белка с лигандом и его функцию. При денатурации активный центр белков разрушается, и происходит утрата их биологической активности.
Под комплементарностью понимают пространственное и химическое соответствие взаимодействующих молекул. Лиганд должен обладать способностью входить и пространственно совпадать с конформацией активного центра. Это совпадение может быть неполным, но благодаря конформационной лабильности белка активный центр способен к небольшим изменениям и "подгоняется" под лиганд. Кроме того, между функциональными группами лиганда и радикалами аминокислот, образующих активный центр, должны возникать связи, удерживающие лиганд в активном центре. Связи между лигандом и активным центром белка могут быть как нековалентными (ионными, водородными, гидрофобными), так и ковалентными.
11. Доменная структура и её роль в функционировании белков. Яды и лекарства как ингибиторы белков.
Домен белка — элемент третичной структуры белка, представляющий собой достаточно стабильную и независимую подструктуру белка, чей фолдинг проходит независимо от остальных частей. В состав домена обычно входит несколько элементов вторичной структуры. Сходные по структуре домены встречаются не только в родственных белках (например, в гемоглобинах разных животных), но и в совершенно разных белках. Домены могут выполнять разные функции и подвергаться складыванию (свертыванию) в независимые компактные глобулярные структурные единицы, соединенные между собой гибкими участками внутри белковой молекулы.