Удобрения и биогенные элементы
Газообразные вещества
Монооксид углерода (СО) – угарный газ образуется при неполном сгорании углеродсодержащих веществ. Наибольшие его количества образуются в результате вулканической деятельности и окисления метана в атмосфере. Внутри помещений СО появляется при неполном сгорании топлива в печах и курении.
Монооксид углерода представляет опасность для человека прежде всего потому, что он может связываться с гемоглобином крови (табл. 1.1). Кроме того, СО может образовывать высокотоксичные соединения – карбонилы.
Таблица1.1
Признаки отравления при различном содержании
Комплекса Hb·CO в крови
| Концентрация СО в воздухе, % об. | Содержание Hb·CO в крови, % | Симптомы |
| 0,006 | Ослабление зрения, легкая головная боль | |
| 0,013 | Боли в голове и теле, утомляемость, временная потеря сознания | |
| 0,02 | Потеря сознания, паралич, прекращение дыхания и жизнедеятельности | |
| 0,066 | Полная потеря сознания, паралич, прекращение дыхания | |
| 0,075 | В течение часа наступает летальный исход |
Скорость связывания СО с гемом зависит от его концентрации, интенсивности обмена веществ в организме, в том числе и от частоты дыхания. Насыщение гемоглобина монооксидом углерода при объеме поступающего в легкие воздуха 10 л /мин с содержанием 0,1 % СО происходит через 6 ч, а при тяжелой работе и интенсивном дыхании (30 л/мин) оно достигается уже менее чем через 2 ч.
Накоплению выделяемого в атмосферу СО препятствуют высшие растения, водоросли и особенно микроорганизмы. У высших растений СО может связываться с аминокислотой – серином, также может происходить его окисление до СО2. В почве некоторые микроорганизмы либо частично включают СО в органические соединения, либо окисляют до СО2. Поэтому почва играет особую роль в удалении СО из атмосферы.
Диоксид углерода (СО2) в отличие от монооксида образуется при полном сжигании углеродсодержащего топлива. Атмосферный СО2 находится в состоянии постоянного обмена с почвой, водой и живыми организмами, в результате чего создается его постоянный круговорот в природе.
Загрязнение атмосферы углекислым газом вызывает обоснованное беспокойство. В течение последних десятилетий идет рост содержания СО2 в атмосфере за счет сжигания ископаемого топлива, вырубки лесов, окисления органического вещества почвы. После 1957 г. содержание СО2 увеличивалось на 0,3–0,5 %. Такие темпы прироста СО2 сохраняются, причем наметилась тенденция к их увеличению, а это может привести к нестабильности климата, учащению климатических аномалий (засух, снегопадов, наводнений и т. д.) и в перспективе вызвать изменение климатических зон и глобальное потепление.
Проблему обогащения атмосферы углекислым газом нельзя рассматривать изолированно, в отрыве от других синергических и антагонистических факторов. К синергическим факторам относится влияние таких газов как SO2, N2O,фторхлоруглеводороды (фреоны), CH4 и O3.
Озон. Озон, образующийся у поверхности земли из выхлопных газов автомашин, играет в дальнейшем незначительную роль, так как он быстро разрушается. Озон, образовавшийся фотохимически в высших слоях тропосферы из выхлопных газов самолетов, вносит определенный вклад в нагревание тропосферы. Стратосферный же озон благодаря поглощению энергии в стратосфере вызывает небольшое охлаждение тропосферы. Концентрация озона в стратосфере непрерывно понижается благодаря действию фреонов и других антропогенных продуктов, при этом уменьшается поглощение солнечных лучей в стратосфере и растет доля энергии, которая приходится на земную поверхность. Таким образом, происходит нагревание земной поверхности.
Скорость образования озона зависит от освещенности и поэтому изменяется и в течение времени. Например, максимум образования озона в течение года приходится на периоды интенсивной солнечной активности.
При действии озона на организм человека может наблюдаться отек легких, нарушение нормального движения мерцательных волосков в бронхах. Систематическое вдыхание озона приводит к накоплению в легких ксенобиотиков, увеличивая опасность заболевания раком, поскольку канцерогенные вещества задерживаются в легких дольше обычного. При концентрации озона около 2 мг/м3 наблюдается усталость, головная боль, резь в глазах и раздражение слизистых оболочек.
Озон оказывает токсическое действие и на растительность. Чувствительные виды растений после часовой обработки озоном в концентрации 0,05–0,1 мг/м3 проявляют признаки угнетения. Озон оказывает сильное влияние на структуру биологических мембран, чем, в известной мере, обусловлен его биоцидный эффект.
Окислы азота и серы Немалую опасность представляет попадание в атмосферу, образующихся при сжигании ископаемого топлива (уголь, нефть, газ), окислы азота и серы. Количество выбросов окислов азота вместе с аммиаком оценено приблизительно в 200–350 млн т в год.
Часть присутствующих в атмосфере оксидов (NO, SO) и диоксидов (NO2, SO2) азота и серы образуются в ходе естественно протекающих природных процессов – вулканических извержений, разрядов атмосферного электричества, жизнедеятельности микроорганизмов. Из ежегодно накапливающихся в биосфере оксидов азота на долю природных процессов приходится 1 100 млн т этих соединений, антропогенная часть составляет еще около 53 млн т.
Следует помнить об образовании оксидов азота внутри помещений, накапливающихся в результате эксплуатации бытовых газовых приборов. Немалый вклад в их накопление вносит и курение. Содержание оксида и диоксида азота в табачном дыме соответственно составляет 98–135 и 150–226 мг/м3. Выкуривание одной сигареты сопровождается появлением в воздухе помещения 160–500 мг оксида азота.
Основную токсикологическую опасность из окислов азота представляют диоксиды азота. В концентрации 100 мкг/м3 диоксид не вызывает каких-либо морфологических изменений в органах дыхания у крыс. Однако повышение концентрации диоксида азота до 600 мг/м3 в организме животных приводит к развитию бронхита и начальным проявлениям пневмосклероза.
Длительное воздействие диоксида азота вызывает целый спектр изменений физиологических систем организма животных (нарушение рефлекторной деятельности, гематологические изменения и т. д.). Диоксид азота в концентрациях 40–140 мг/м3 при экспозиции не более часа может вызывать развитие бронхита и бронхопневмонии.
Наиболее опасное проявление острого отравления оксидами азота – отек легких.
При оценке биохимических эффектов диоксидов азота в ранние сроки от начала воздействия в тканях легких и печени прежде всего снижается содержание глутатиона.
В атмосфере крупных промышленных городов постоянными спутниками оксидов азота являются оксиды серы. По существующим данным ежегодно в результате деятельности человека вырабатывается около 150 млн т серы, преимущественно в результате утилизации ископаемого топлива (до 70 % – при сжигании каменного угля и 16 %– при сгорании нефтепродуктов). При выплавке меди, свинца и цинка количество образующегося диоксида серы достигает 15 млн т.
Наиболее реальной мишенью воздействия оксидов серы являются дыхательные пути, что приводит к увеличению респираторных заболеваний у населения, ослабляет иммунную защиту у людей и животных и т. д.
Определенное количество выброшенных в атмосферу окислов азота и серы удаляется в результате сорбции почвой, растительным покровом, водой и кислотных дождей. Образование кислотных дождей происходит с участием УФ-излучений, кислорода воздуха и озона (рис. 1.1).
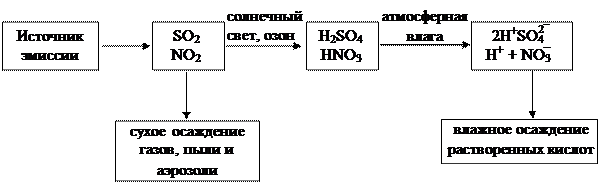
|
| Рис. 1.1. Механизм образования кислотных дождей |
Осаждающие на земную поверхность окислы азота и серы снижают интенсивность фотосинтеза, вызывают гибель наземных растительных сообществ, подкисление водоемов и связанную с ним гибель гидробионтов. Отдельные виды рыб, моллюски весьма болезненно реагируют на закисление среды. Это связано с нарушением кальциевого обмена.
Снижение рН почвы приводит к подавлению развития микроорганизмов, роста растений. Например, кислотные осадки с рН 3,0 снижали образование стручков у бобовых на 7 %.
Фторсодержащие углеводороды. Большую тревогу вызывает их накопление в атмосфере. Общие выбросы углеводородов в атмосферу составляют не менее 200 млн т в год. Особенно опасны для живых организмов полициклические ароматические углеводороды, в частности бенз(а)пирен, образующиеся при сгорании различных видов топлива и других высокотемпературных процессах и вызывающие мутагенные и канцерогенные эффекты.
Фторхлорсодержащие углеводороды вызывают разрушение озонового слоя в стратосфере. Это связано с тем, что под действием УФ-излучения образуются активные радикалы Cl*. При фотолизе кроме хлора образуются ряд других активных соединений, которые могут разрушать фторхлоруглеводороды (ФХУ) с образованием радикалов ClO* и Cl*. Радикалы участвуют в разрушении озона.
Вместе с СО2 галогенуглероды участвуют в создании парникового эффекта в атмосфере, т. к. они поглощают ИК-излучение в области 700–1300 нм, т. е. в той области, в которой СО2 их пропускает.
Разрушение озона в тропосфере приводит к резкому нагреванию тропосферы, т. к. все больше богатых энергией УФ-излучений проникает в тропосферу и поглощается в ней. Поэтому влияние ФХУ на нагревание тропосферы таит в себе еще большую опасность, чем увеличение попадания УФ-лучей на поверхность Земли. УФ-излучение значительно увеличивает опасность раковых заболеваний у людей, особенно со светлой кожей. Кроме того, снижается рост и интенсивность фотосинтеза растений, что приводит к потере урожая. Эти эффекты проявляются уже при незначительной потере озона стратосферой.
Тяжелые металлы
О масштабах загрязнения тяжелыми металлами можно судить из данных, характеризующих общемировое годовое производство. Однако необходимо учитывать и другие источники. Например, 1,5–2 тыс. т ртути ежегодно поступает в биосферу при переработке минералов и руд, 0,1–8 тыс. т – при сжигании топлива; ежегодно в биосферу при сжигании угля попадает около 3,5 тыс. т свинца, 56 тыс. т – в результате выветривания и 110 тыс. т выносят реки.
В списке 20 самых опасных токсикантов, составленном в 2003 году Агенством по токсическим веществам и регистрации болезней совместно с Агенством по защите окружающей среды, тяжелые металлы свинец, ртуть, и кадмий по своей токсичности занимают 2, 3 и 7 места соответственно.
Тяжелые металлы вызывают острое или хроническое отравление. Токсичность тяжелых металлов проявляется в подавлении роста и развития растений и микроорганизмов, нанесения серьезного ущерба здоровью человека и животных. Так, тяжелые металлы вызывают нарушения функционирования центральной нервной системы, изменение состава крови, отрицательно влияют на функции почек, легких, печени и других органов. Длительное воздействие их может вызвать развитие рака, аллергии, физических и неврологических дегенеративных процессов.
Степень токсичности тяжелых металлов для человека и животных, а также для растений неодинакова и колеблется в весьма широких пределах. Они оказывают повреждающее действие на биообъекты в концентрациях, не превышающих 1 мг/л. Так, цинк, титан характеризуются низкой токсичностью для человека и теплокровных животных, но даже в низких концентрациях они оказывают губительное действие на рыб и других обитателей водных экосистем.
Наиболее часто металлы, в том числе и высокотоксичные, попадают в окружающую среду в результате промышленных сбросов в водоемы со сточными водами, не прошедшими эффективной очистки, а также использование пестицидов, в состав которых они входят.
В ряде случаев происходит депонирование металлов в придонных слоях, особенно значительное в холодное время; по мере повышения температуры происходит постепенное их растворение. Для повреждения механизмов природного самоочищения водоемов бывает достаточным даже кратковременное повышение концентрации металлов в водной экосистеме, что весьма существенно при организации мониторинга тяжелых металлов в сточных водах.
Коротко рассмотрим токсикологическую характеристику наиболее распространенных и токсичных металлов-поллютантов.
Свинец попадает в окружающую среду в больших количествах. Ежегодно в земную атмосферу выбрасывается около миллиона тонн его соединений, значительная часть которых водорастворима, что обусловливает экологическую опасность Pb2+. Основной источник – этилированный бензин. Токсикологическая опасность свинца усугубляется его активным всасыванием в пищеварительном тракте человека и животных, значительным объемом распределения в тканях и накоплением в костях. Депонированный в костях свинец способен поступать в кровь, с током которой доставляется в различные органы. Считают, что в организм взрослого человека с водой и продуктами питания за сутки поступает 0,3 мг свинца и еще 0,3 мг попадает из табачного дыма у интенсивных курильщиков.
Случаи хронического отравления свинцом наблюдаются при длительном употреблении питьевой воды, в которой его содержание достигает 0,04 –1 мг/л.
В наибольшей степени опасному воздействию свинца подвергаются рабочие, занятые на его добыче в шахтах, а также при выплавке. В этом случае металл поступает в организм ингаляционным путем.
Примерно 35 % свинца, попавшего в дыхательные пути человека, оседает в легких. Около 10 % свинца, поступившего с продуктами питания в пищеварительный тракт, всасывается. Выведение свинца из организма человека осуществляется преимущественно (более 70 %) почками и в меньшей мере через пищеварительный тракт (~ 10 %).
Проведенные в Гренландии исследования показали, что содержание свинца во льду, образованном примерно в середине XVIII в., оказалось примерно в 25 раз выше, чем во льду, образование которого было отнесено к VIII в. до н. э. С 1750 г. накопление свинца в ледниках Гренландии постоянно возрастает. С 40-х гг. XX в. этот процесс усилился и продолжается до настоящего времени.
Определенную роль в накоплении свинца в экосистемах играют растения, получающие металл не только из атмосферы, но и из почвы. Отмечается видовая специфичность растений при его накоплении. Так, при выращивании растений присутствующий в атмосфере свинец обнаружен в листьях салата и бобов, но практически отсутствует в томатах, кочанной капусте, картофеле и моркови.
Свинцовая интоксикация вызывает нарушение биосинтеза гемоглобина на уровне ингибирования левулинатдегидратазы и гемсинтетазы. Имеются сведения о нарушении синтеза цитохрома Р-450 при свинцовой интоксикации.
Главной мишенью воздействия свинца при хронических отравлениях являются центральная и периферическая нервные системы (свинцовая энцелопатия: появление головной боли, нарушение сна, памяти, возникновение тремора, галлюцинаций и т. д.). Для различных вариантов отравления свинцом характерно поражение почек, пищеварительного тракта.
Ртуть и ее соединения относятся к веществам общетоксического действия, вызывающим у людей летальный исход, попадая в организм с питьевой водой в количестве 75–300 мг в сутки. Наиболее токсична двухлористая ртуть (сулема), однократная летальная доза которой составляет для человека 0,2–0,5 г. Ртуть характеризуется высокой нефротоксичностью, приводящей к быстро развивающейся почечной недостаточности. Выведение ртути осуществляется почками, через пищеварительный тракт, потовыми и молочными железами.
Начиная с концентрации 0,006–0,01 мг/л ртуть в виде водорастворимых солей оказывает губительное влияние на рыб и другие водные организмы.
При отравлениях ртутью, особенно ее органическими соединениями, отчетливо выражены симптомы поражений нервной системы (парезы, параличи, нарушения зрения и слуха).
В 1953 г. в Японии у 121 жителя побережья Минамата было выявлено заболевание, сопровождающееся ломотой в суставах, нарушением слуха и зрения. При этом заболевании, вошедшим в литературу под названием «болезнь Минамата» умерло почти треть больных. Проведенное расследование позволило установить, что на ацетиленовом производстве ртутные отходы сбрасывались в реку, впадающую в бухту Минамата. Ртуть микробиологическим путем превращалась в метилртуть, которая через планктон, моллюсков и рыб в конце концов концентрировалась и дойдя до человека достигала токсичной концентрации.
Такая кумуляции возможна только в том случае, когда токсин поступает быстрее, чем выводится из организма. Биологический период полувыведения ртути велик, он составляет для большинства тканей человека 70-80 дней.
К еще одной экологической катастрофе, связанной с отравлением органическими соединениями ртути, применяемыми в качестве пестицидов, относится массовое отравление людей в 1972 г. в Ираке. Отравление произошло в результате употребления в пищу хлеба, приготовленного из обработанных фунгицидом, содержащим метилртуть, семян. Общее количество госпитализированных пораженных составило 6 530, из которых 500 человек погибло. Содержание метилртути в муке выпеченный из которой хлеб явился непосредствен  ной причиной массового отравления, колебалось в пределах 4,8–14,6 мкг/г. Клиническая картина отравления характеризовалась развитием парестезий, нарушениями координации, атаксией, нарушениями зрения вплоть до полной слепоты, нарушениями слуха. Произведенные расчеты, хотя и весьма приблизительные, позволили выявить зависимость тяжести симптоматики отравления от дозы. Попадание на протяжении нескольких месяцев ртути с хлебом в суммарном количестве около 30 мг вызывало парестезии, а при увеличении дозы до 55 и 170 мг – атаксию и глухоту.
ной причиной массового отравления, колебалось в пределах 4,8–14,6 мкг/г. Клиническая картина отравления характеризовалась развитием парестезий, нарушениями координации, атаксией, нарушениями зрения вплоть до полной слепоты, нарушениями слуха. Произведенные расчеты, хотя и весьма приблизительные, позволили выявить зависимость тяжести симптоматики отравления от дозы. Попадание на протяжении нескольких месяцев ртути с хлебом в суммарном количестве около 30 мг вызывало парестезии, а при увеличении дозы до 55 и 170 мг – атаксию и глухоту.
Аналогичный случай массового отравления при употреблении в пищу кукурузы, обработанной фунгицидом на основе метоксиэтилртути, произошел в Гане. Общее количество пострадавших составило 114, из которых 20 человек погибли. У всех отравленных были отмечены симптомы поражения нервной системы – тремор, гиперрефлексия, в тяжелых случаях (в особенности у детей) – паралич конечностей.
Кадмий относится к числу металлов, которые, попав в живой организм, влияют на него губительно. Весьма важным является фактор длительности воздействия кадмия на организм человека и животных в связи с его способностью накапливаться в печени, почках, поджелудочной и щитовидной железах и др. Кадмий характеризуется выраженной нефротоксичностью при попадании в организм с питьевой водой.
Высокой чувствительностью к действию кадмия характеризуются водные организмы. Так, пребывание рыб (гуппи, карп, карась и др.) на протяжении суток в воде с содержанием Cd2+ 0,001–0,3 мг/л приводит к их гибели.
Для кадмия период полувыведения из организма человека составляет более 10 лет, поэтому при систематическом попадании даже следов кадмия в организм могут в конечном итоге наблюдаться различные неблагоприятные симптомы.
Удобрения и биогенные элементы
Общее потребление минеральных удобрений (N + P2O5 + K2O) составляет около 100 млн т в год. Содержание в воде нитратов и нитритов варьирует от 0 до 200 мг/л.
Особую тревогу вызывает применение азотных удобрений, поскольку повышенное содержание нитратов и нитритов в питьевой воде, в овощах, зеленых кормах для человека и животных представляет токсикологическую опасность.
Растворимые соединения азота, которые присутствуют в питьевой воде, могут оказывать токсическое действие на людей. Попадая вместе с пищей в организм нитраты микробиологическим путем восстанавливаются до нитритов, в результате в крови образуются нитрозил-ионы:
NO2- +H NO+ +OH-
Нитрозил-ионы окисляют двухвалентное железо в гемоглобине до трехвалентного, что препятствует связыванию кислорода гемоглобином в связи с образование координационной связи между железом и кислородом:
Fe2+ + NO+ Fe3+ + NO
В результате возникают симптомы кислородной недостаточности, приводящей к цианозу (синюха).При переходе 60–80 % железа в гемоглобине в трехвалентное наступает смерть. Особенно чувствителен к нитрозил-иону младенцы в первые недели своей жизни. У них недостаточно проявляется деятельность гемоглобинредуктазы, восстанавливающей Fe3+ в Fe2+. У взрослых этот процесс идет активнее и в результате организм не так остро реагирует на присутствие нитратов и нитритов. Однако и взрослые должны избегать чрезмерного попадания в организм нитратов и нитритов, поскольку последние расширяют сосуды и образуют в желудке при низких (кислых) значениях рН азотистую кислоту, вызывающую мутагенные эффекты. Кроме того, нитриты в кислой среде образуют с органическими аминами из растительной и животной пищи нитрозоамины, также обладающие мутагенным действием:
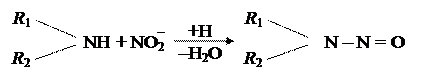
Существуют допустимые нормы содержания нитратов в растительных продуктах питания, которые значительно отличаются. Это объясняют количеством производимой продукции, а отсюда и количеством потребляемой в пищу. Ежедневное потребление нитратов на душу населения в США оценивается примерно в 400 мг: 200 мг с овощами, 115 мг с мясными продуктами и 85 мг с водой. В Англии – 225 мг в сутки с овощами, 110 мг с мясом и 105 с водой (итого 440 мг). У нас эти дозы несколько ниже.
В водопроводной воде содержание нитратов и нитритов недолжно превышать 10 мг/л. При норме 2 л в сутки человек потребляет 20 мг.
Обычно хорошо растворимые в воде удобрения, вымываются дождями и попадают в грунтовые и поверхностные воды. Большую опасность в этом случае для природной среды представляют содержащиеся в удобрениях ионы NO3-, NH4+, H2PO4-, HPO4-, которые способствуют зарастанию водоемов растительностью, т.е. происходит эвтрофирование. Например, содержание 10 мг фосфата в 1 м3 воды приводит к заметному росту планктона. Эвтрофикации подвержены не только внутренние водоемы, но и прибрежные участки океана.
Вместе с некоторыми удобрениями в почву попадают и побочные загрязняющие элементы (например, фтор, кадмий). Растения используют часть внесенных минеральных удобрений. Остальная часть может смываться в водоемы.
Загрязнение почвы биогенами (фосфор, азот) происходит не только при внесении избыточного количества удобрений, но и другими путями (фекальные отходы животноводства, коммунально-бытовые загрязнения и т. д.). Только в США ежегодное поступление биогенов в водоемы составляет: азота – около 5 млн т, фосфора – примерно 250 тыс. т. Все это приводит к эвтрофикации внутренних водоемов, а также прибрежных участков океана.
Органические соединения
Среди большого количества разнообразных органических соединений выделим наиболее распространенные загрязнители, такие, как нефть и нефтепродукты, пестициды, полихлорбифенилы (ПХБ) и поверхностно-активные вещества (ПАВ).
Нефть и нефтепродукты. Глобальное загрязнение этими веществами складывается из эмиссии в атмосферу вследствие испарения и сгорания (40-7- млн т), загрязнений наземных экосистем (~19 млн т)и морской среды (1–2 млн т).
Нефть весьма медленно разлагается в окружающей среде. В основном она состоит из ароматических углеводородов; в некоторых случаях, в зависимости от ее происхождения, она может содержать алициклические углеводороды. В небольших количествах может содержать такие соединения как альдегиды, кетоны и карбоновые кислоты.
Попадает нефть в природную среду различными путями: при бурении скважин, при авариях танкеров, течи в нефтепроводах, при транспортировке, очистке отстойников и т. д.
На поверхности воды она разливается на большие расстояния с образованием тонкой пленки (1 т нефти образует пленку на 12 км2). В этом случае образуется эмульсионный слой нефть-вода, который препятствует газообмену между водой и воздухом. Это приводит к тому, что все живые организмы, находящиеся под этой пленкой задыхаются. При этом прежде всего при дыхании в клетках накапливается СО2, что ведет к ацидозу, т. е. подкислению внутриклеточной среды. У птиц контакт с нефтью приводит к склеиванию оперения, птицы утрачивают способность держаться на воде и быстро гибнут от переохлаждения. Растворимые в воде окисленные компоненты нефти могут обладать токсическим действием. Нефть и ряд нефтепродуктов весьма токсичны для живых организмов, многие ее продукты канцерогенны. Нефть, попавшая в природную среду, подвергается микробиологическому разложению, но этот процесс идет очень медленно (в течение недель и месяцев). За это время ее легколетучие компоненты испаряются, а оставшиеся подвергаются медленному окислению, что приводит к образованию сгустков, которые постепенно опускаются на дно и оказывают влияние на придонные организмы.
Пестициды. Среди ксенобиотиков особое место занимают средства защиты сельскохозяйственных растений от сорняков, насекомых, грибов. Около 14 % всего урожая в мире ежегодно теряется из-за насекомых, 12 % – из-за болезней растений, вызываемых грибами и червями, 9 % – из-за сорняков и 10 % уничтожают грызуны. Общие потери урожая в мире оцениваются примерно в 1,8 млрд т.
В этой связи человек вынужден использовать огромное количество химических средств защиты. Применение пестицидов, в свою очередь, приводит к их попаданию в биосферу, где живые организмы начинают испытывать на себе огромный «пестицидный пресс». Сформировался своеобразный «пестицидный парадокс», смысл которого состоит в том, что человечество, применяя пестициды, само становится мишенью их воздействия.
Кроме того, попадание большого количества пестицидов и других ксенобиотиков в водоемы приводит к деградации водных экосистем и быстрому уменьшению ресурсов чистой воды.
Важное экономическое значение пестицидов обусловливает рост объемов их производства и использования в мировом земледелии. В рамках основных групп пестицидов их применение в отдельных регионах мира в процентах от общего количества характеризуется данными, приведенными в табл. 1.2.
Таблица 1.2