Трансформация и распределение ксенобиотиков
Биоаккумулирование ксенобиотиков
Организмы, обитающие в окружающей среде, содержащей относительно низкую концентрацию какого-либо вещества, могут накапливать его в своих тканях до концентраций, на несколько порядков больших, чем в среде обитания.
Способность накапливать различные элементы даже при очень низком содержании их в среде известна давно. Это явление обычно называется аккумулированием вещества организмом (кумулятивный эффект).
Способность организмов к накоплению веществ характеризуется таким параметром, как коэффициент накопления.
содержание (концентрация) вещества в организме
N = –––––––––––––––––––––––––––––––––––––––––––––
содержание (концентрация) в окружающей среде
С явлением значительной аккумуляции ксенобиотиков в организме специалисты столкнулись при изучении накопления пестицидов, в частности хлорированных углеводородов. В одной из экосистем оз. Мичиган (США) было обнаружено явление биоконцентрации ДДТ в следующем ряду: 0,014 мг/кг (при расчете на сырую массу) – в донном иле; 0,41 мг/кг – в ракообразных, питающихся на дне; 3–6 мг/кг в – рыбах (бельдюговые, язь, елец); 24000 мг/кг – в жировой ткани чаек, питающихся рыбой.
В больших количествах идет накопление организмами ПХБ. Обладая низкой скоростью разложения в окружающей среде (период полураспада около 5 лет), ПХБ поступают в пищевые цепи и в значительных количествах аккумулируются в живых организмах. Например, в угрях, выловленных из воды с содержанием полихлорбифенила 0,1 мкг/л, концентрация этого вещества составила 7,9 мг/кг, т. е. коэффициент накопления ПХБ был равен 80 000.
Включение ПХБ в трофические цепи типа: водоросли (планктон) – ракообразные – рыбы – человек может привести к поступлению в организм человека с продуктами питания до больших количеств этих токсикантов. Поступление ПХБ с материнским молоком в организм ребенка может достигать 3 мкг/кг массы в сутки.
Велика накопительная способность и у растений, особенно водных. Наиболее известный и яркий пример – это накопление йода водорослью ламинарией. Содержание йода в ламинарии достигает 0,3 % при концентрации его в морской воде 0,0001 %. Еще в первой половине нашего столетия большие количества йода добывались из золы ламинарии. Затем были созданы более выгодные в техническом отношении способы добычи на базе минерального сырья. Некоторые представления о накопительной способности водных растений дает табл. 10.1.
Таблица 10.1
Коэффициенты накопления различных элементов
Некоторыми растениями
| Элемент | Кладофора | Низшие растения | Элодея | Высшие растения | Общее среднее |
| Фосфор | |||||
| Кальций | |||||
| Кобальт | |||||
| Цинк | |||||
| Рубидий | |||||
| Стронций | |||||
| Цирконий | |||||
| Иттрий | |||||
| Цезий | |||||
| Церий |
Одно время промелькнул ряд сообщений, к сожалению лаконичных, различных зарубежных фирм о разработке обогатительных установок для извлечения «биологическим методом» из растворов иттрия, ниобия и т. д.
Накопительные свойства растений используются для поиска полезных ископаемых (так называемые фитогеохимические методы). Повышенное содержание многих элементов в почве приводит к резкому увеличению их содержания в растениях. Анализ золы растений-концентраторов позволяет осуществлять выделение биогеохимических провинций. Более того, определенные виды растений имеют склонность произрастать в местах с преобладанием тех или иных элементов (мать-и-мачеха, вьюнок – почвы, богатые кальцием, определенные виды лебеды – на засоленных почвах).
Накопительные свойства водорослей используются для контроля радиоактивности вод Мирового океана – радиоальгологический анализ.
Факторы, влияющие на аккумулирование ксенобиотика.Поскольку явление аккумулирования включает взаимодействие вещества с организмом, то факторы, определяющие степень его накопления, должны включать характеристики как самого ксенобиотика, так и организма. Одной из характеристик самого вещества является устойчивость. Для того чтобы ксенобиотик мог накапливаться в организме, его воздействие на организм должно быть достаточно длительным, особенно когда оно осуществляется через цепь питания. Следовательно, любое аккумулирующееся вещество должно быть устойчивым к возможным в данной среде процессам разрушения. Как уже упоминалось, способность вещества накапливаться в конкретном организме характеризуется его периодом полувыведения из этого организма. Обычно те ксенобиотики, которые устойчивы в окружающей среде, в большинстве организмов имеют относительно продолжительные периоды полувыведения и способны накапливаться в сравнительно больших количествах, но, конечно, при достаточно высокой концентрации их в окружающей среде.
Площадь поверхности. Если процесс аккумулирования включает физические стадии (адсорбция, диффузия), степень накопления чужеродного вещества в большей мере зависит от площади поверхности контакта организма с окружающей средой. Это положение можно применить к таким случаям, как адсорбция растениями пестицида из воздуха после опрыскивания или адсорбция организмами ПХБ в водной среде.
Величина поверхности на единицу массы или объема повышается при уменьшении размера частицы. Следовательно, если адсорбция в процессе аккумулирования играет значительную роль, то можно ожидать, что более мелкие организмы будут накапливать в единице объема большее количество вещества, чем более крупные. Действительно, существуют заметные различия в способности накопления веществ у клеток неодинаковой величины. Так, шесть видов водорослей, различающиеся размерами, в разных количествах накапливали ДДТ. У тех видов, которые имели более крупные клетки, способность накапливать ДДТ была более низкая. Убитая культура клеток водорослей имела приблизительно такую же способность к аккумулированию ДДТ, как и живые организмы. Это возможно при поглощении веществ по адсорбционному механизму, а не по механизму, требующему расхода энергии. Наблюдалось также, что нитчатые водоросли, которые образуют длинные нити с очень большой поверхностью, обладают более высокой способностью аккумулировать вещества из водной среды по сравнению с другими видами, имеющими меньшую поверхность. Следовательно, доступная для вещества поверхность относится к лимитирующим факторам, особенно в тех случаях, когда адсорбция является определяющим процессом в накоплении.
Распределение. Большинство организмов содержит значительные жировые отложения; в этих тканях накапливаются ксенобиотики с большими значениями коэффициента распределения. Содержание жира в организме также указывает на его способность аккумулировать данный тип веществ. Так, способность аккумулировать ПХБ коррелировала с содержанием липида в планктоне. Таким образом, степень аккумулирования зависит от способности веществ распределяться в жировых депо.
Способность данного ксенобиотика распределяться в жировых депо организма также может влиять на его период полувыведения. Жировые ткани в процессах метаболического преобразования являются не самыми активными. Следовательно, если вещество распределилось в таких тканях, оно может сохраняться там до тех пор, пока организм не израсходует весь жир.
Устойчивые в окружающей среде ксенобиотики очень плохо растворяются в воде. Следовательно, среда обитания конкретного организма может существенно влиять на его способность аккумулировать ксенобиотики. Организмы, обитающие на дне среди осадков, подвергаются воздействию более высоких концентраций ксенобиотика, чем находящиеся в верхних слоях того же самого участка водоема.
На процесс аккумулирования может влиять и размер частиц, проглатываемых организмами. Поскольку на более мелких частицах, как уже отмечалось, адсорбированное на их поверхности чужеродное вещество содержится в более высоких концентрациях, организмы, проглатывающие такие частицы, будут подвергаться воздействию более высокого содержания ксенобиотика.
Важным фактором является и количество потребляемой пищи. Организмы, нуждающиеся в относительно большом количестве пищи, могут аккумулировать чужеродное вещество из окружающей среды в большей степени при условии, что процесс накопления ксенобиотика не компенсируется более активным процессом его выведения.
Цепь питания. Ксенобиотики в массовых количествах поступают в неорганические элементы биосферы (воздух, воду, почву). Находясь во внешней среде, чужеродные соединения взаимодействуют с различными органическими элементами биогеоценозов – микроорганизмами, растениями, животными, поступая в конечном итоге по трофическим цепям в организм человека. В этих условиях суммарное количество ксенобиотиков, поступающих в организм человека, в значительной степени определяется интенсивностью их разрушения под действием физико-химических факторов среды (света, воды, тепла и др.), скоростью их деструкции в предшествующих элементах трофических цепей и закономерностями биоконцентрации.
Таким образом, любая экологическая система является совокупностью абиотических элементов, а также живых организмов, обменивающихся химическими компонентами, энергией и связанных между собой пищевыми (трофическими) цепями. При этом организмы – компоненты экосистем – подразделяются на производителей (продуцентов), потребителей (консументов) и разрушителей (редуцентов), разлагающих сложные органические соединения мертвых остатков.
Установлено, что по мере движения ксенобиотика по пищевой цепи к следующему консументу, в организме которого он метаболизируется в незначительной степени, происходит существенное увеличение концентрации чужеродного вещества.
Для понимания этого явления необходимо представлять взаимоотношения, существующие между видами в естественной среде. Вещества поглощаются в определенной последовательности: так, загрязненные растения поедаются травоядными рыбами и животными, этих рыб и животных поедают плотоядные животные и т. д. Таким образом, существуют два механизма перемещения чужеродного вещества в данной конкретной цепи питания – непосредственное его поглощение из среды и перемещение по цепи питания.
При рассмотрении распределения любого ксенобиотика в экосистеме необходимо учитывать биологические аспекты, а также иметь определенные сведения об относительном положении различных видов в цепи питания, информацию о плотности популяций различных организмов и скорости поглощения ими данного вещества.
Аккумулирование ксенобиотика в цепи питания определяется его перемещением по этой цепи, а также тем, что менее 50 % всей массы вещества преобразуется в ткани организма на следующем, более высоком уровне.
Процесс иллюстрируется схемой (рис. 10.1), где показаны также возможные потери ксенобиотика путем экскреции на различных уровнях цепи питания. Проведенный анализ показывает, как концентрация чужеродного вещества постепенно повышается в цепи питания.
Для лучшего понимания закономерностей движения по пищевым цепям продуктов питания, а также попавших в биоценозы ксенобиотиков строятся так называемые экологические пирамиды. В экологических пирамидах схематически учитывают плотности популяций (число особей на 1 м2), биомассы (грамм сухого или влажного вещества на 1 м2) или продуктивность в энергетических эквивалентах (джоулей на 1 м2 в год) для всех членов каждого трофического уровня в данном биоценозе.
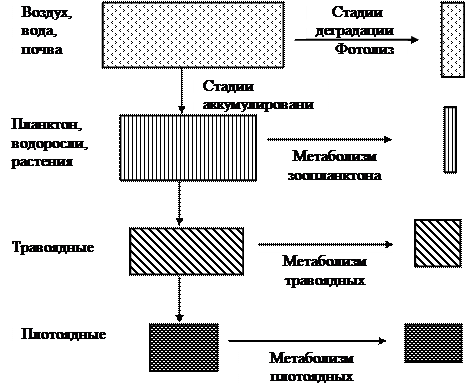
|
| Рис. 10.1. Усиление в цепи питания — схема увеличения концентрации вещества в организмах по мере достижения более высокого трофического уровня |
В условиях поступления в организм чужеродных химических веществ, которые не могут быстро метаболизироваться и полностью экскретироваться во внешнюю среду, начинается накопление этих веществ по ходу пищевой цепи. При этом, поскольку организмы-потребители, стоящие на более высоких уровнях экологической пирамиды, обладают меньшей суммарной биомассой по сравнению с организмами предыдущего уровня, происходит последовательная биоконцентрация токсикантов, достигающая максимальных значений у конечных консументов, которыми могут являться люди.
Накопление наночастиц гидробионтами, например диоксида титана, происходит достаточно быстро (в течение 45 суток) и в больших количествах (коэффициент накопления в диапазоне 1001000). Аккумулируются наночастицы как водорослями (Chlorella vulgaris) – первичными потребителями пищевой цепи, так и мелкими ракообразными из зоопланктона – дафниями (Daphnia magna). Поскольку планктонные беспозвоночные являются связующим звеном в пищевой и энергетической линиях между первичными потребителями (водоросли) и вторичными консументами (например, рыбы), то вполне возможным оказывается поступления техногенных наночастиц в пищевые цепи рыбоводства и промышленной аквакультуры.
По мнению известного эколога Море, вследствие явления биоконцентрации воздействие пестицидов на человечество по пищевым цепям представляет гораздо большую опасность, чем радиоактивность от АЭС.
Накопление токсических элементов в компонентах экосистем может оказывать разнообразное негативное действие, приводя к нарушению устойчивости экосистем к неблагоприятному влиянию на организм человека. Так, вследствие длительного и значительного накопления ДДТ и других химикатов в водоемах и промышленных стоках в 1989 г. была запрещена продажа рыбы из городских водоемов населению Западного Берлина.
В результате передачи через почву растениям и сельскохозяйственным животным свинца, входящего в состав этилированного бензина, возможно поступление этого токсиканта в организм человека.
С явлениями биоконцентрации связаны и кадмиевые катастрофы, происшедшие в 70-е гг. в ФРГ и Японии. Тысячи японских граждан пали жертвой болезни «итай-итай» вследствие употребления зараженных кадмием питьевой воды и овощей в результате выбросов в окружающую среду отходов нефтекомбинатов.
Итак, в результате процессов абсорбции, распределения и биоконцентрации, зависящих как от физико-химических свойств ксенобиотиков, так и от экологических взаимоотношений в пищевых цепях, в организмах человека, животных и растений происходит аккумулирование ксенобиотиков, сопровождающееся в ряде случаев их специфическим токсическим действием. При этом интегральная реакция организма на действие токсиканта определяется также наличием эволюционно выработанных защитных систем, к которым относятся физиолого-биохимические системы биотрансформации, экскреции ксенобиотиков и система иммунного гомеостаза.
В водных и наземных системах механизмы аккумулирования ксенобиотиков различны, причем они могут отличаться даже в пределах одной системы.
В водной среде аккумулирование ксенобиотика может протекать по двум механизмам:
– непосредственной адсорбции вещества и (или) его распределения из водной среды;
– распределения по цепи питания.
Возникает вопрос: какой из этих механизмов более важен? В большинстве случаев отмечается, что непосредственное поглощение из водной среды имеет большее значение, чем распределение по цепи питания. Распределение непосредственно из среды обитания может быть определяющим процессом, но при условии, что поверхность контакта организма с водой не является лимитирующим фактором. Рыбы очень эффективно аккумулируют чужеродные вещества из водной среды, так как имеют жабры с развитой поверхностью, через которые проходит большой объем воды. В организме тюленя подобного органа нет, следовательно, аккумулирование ксенобиотика должно быть связано с цепью питания.
При обсуждении поступления и накопления ксенобиотиков водными организмами специалисты различают следующие процессы:
- биоконцентрирование – накопление химических соединений (ХС) организмом в результате прямого поступления из окружающей среды без учета попадания с продуктами питания;
- биоумножение – накопление в организме ХС непосредственно из продуктов питания. В природной среде этот процесс идет одновременно с биоконцентрированием;
- биоаккумуляция – накопление в организме за счет прямого поступления из среды и питания;
Экологическое накопление – прирост концентрации вещества в экосистеме или цепи питания при переходе от низкого к более высокому трофическому уровню.
В условиях наземной среды чужеродные вещества в конечном итоге оказываются в почве, и их аккумулирование организмами должно происходить по цепи питания. Воздействие на организм ксенобиотика из атмосферы вследствие испарения из почвы может показаться аналогичным его общему воздействию на организм в водной среде. Однако концентрация чужеродного вещества в воздухе при испарении очень мала, а его способность рассеиваться в открытом пространстве настолько велика, что в большинстве случаев аккумулирование ксенобиотика по механизму распределения из атмосферы минимально. Исключение могут составлять роющие животные, существующие в более ограниченной среде.
В отличие от водных организмов у наземных животных биоаккумулирование происходит в основном за счет питания. У наземных высших растений накопление происходит, главным образом, за счет поступления ХС из почвы.
Таким образом, процесс аккумулирования ксенобиотика наземными организмами должен включать его поглощение организмами, обитающими в почве, и последующее перемещение по наземной цепи питания.
Степень, до которой организм аккумулирует определенный ксенобиотик, зависит не только от положения организма в цепи питания, но и от его физиологических и морфологических особенностей.
Трансформация и распределение ксенобиотиков
В экосистемах
Ксенобиотики в массовых количествах поступают в неорганические элементы биосферы (воздух, вода, почва). Находясь во внешней среде они взаимодействуют с различными органическими элементами биогеоценозов – микроорганизмами, растениями, животными и человеком. В этих условиях влияние ксенобиотиков на экосистемы связано с интенсивностью процессов их превращений и разрушений. Эти процессы и определяют экологическую опасность чужеродных соединений.
Для ксенобиотиков, попавших в экосистемы и входящие в них организмы, можно выделить следующие явления:
- реакции превращения ксенобиотиков,
- адсорбция ксенобиотиков на частицах биологического и абиотического происхождения.
- переход ксенобиотиков из одной среды в другую.
Реализация этих этапов в реальных биогеоценозах происходит при теснейшем взаимодействии между различными факторами.
Реакции превращения ксенобиотиков включают такие основные стадии как окислительно-восстановительные и гидролитические реакции, реакции конъюгации в организмах экосистем как с участием ферментативных процессов, так и распад (деградация) ксенобиотиков под действием физико-химических факторов: света, воды, окислительно-восстановительного потенциала среды.
Охарактеризуем влияние каждого из перечисленных факторов на характер поведения ксенобиотиков в экосистемах.
На экосистемы чрезвычайно важное влияние имеет скорость превращения ксенобиотиков. Высокая скорость превращения обычно приводит к исчезновению вещества и, следовательно, к исчезновению проблемы, связанной с загрязнением окружающей среды; при медленном разрушении вещество сохраняется длительное время, что может вызвать его концентрирование.
Ферментативные превращения. Как уже отмечалось нами неоднократно, конечный путь обезвреживания чужеродных веществ в многоклеточных организмах – конъюгация этих веществ с различными органическими молекулами.
В организме животных, растений и др. биологический смысл конъюгации ксенобиотиков заключается в том, чтобы придать им повышенную водорастворимость и вывести их в виде водорастворимых конъюгатов. Однако с биогеоценотической точки зрения проблема все равно остается, поскольку ксенобиотик (в форме конъюгата) попадает в почву или в воду и продолжает циркулировать в биогеоценозе.
Продукты конденсации некоторых пестицидов (или их метаболитов) с веществами растений разлагаются медленнее, чем исходные вещества. Такова, например, ситуация, возникающая при конъюгации некоторых фосфорорганических пестицидов (винфос) с веществами растительной клетки, в частности с лигнином.
Одним из типов конъюгирования ксенобиотиков может считаться их алкилирование. Для дальнейшей судьбы ксенобиотика в организме и биогеоценозе очень важно, что при алкилировании может существенно изменяться водо- и жирорастворимость (липофильность) данного соединения, а последнее свойство вещества определяет его переходы из гидрофильной среды в гидрофобную и обратно.
Эти переходы определяют прохождение ксенобиотика через гидрофобный слой мембран, окружающий живые клетки, и последующие его воздействия. Кроме того, именно гидрофобность ряда ксенобиотиков (в т. ч. многих хлорорганических соединений) обусловливает их повышенную способность к биоаккумулированию.
Еще один аспект важности перехода ксенобиотиков из гидрофильной среды в гидрофобную (и обратно) состоит в том, что при этом изменяется доступность молекулы для ферментов. Подавляющее большинство ферментов действует в водной среде. Переход молекулы ксенобиотика из водной среды в гидрофобную означает уменьшение их доступности для ферментов, а следовательно, снижается вероятность их биотрансформации и детоксикации.
Превращения ксенобиотик под воздействием физико-химических факторов среды.Остановимся на таких физико-химических процессах превращения ксенобиотиков в среде, как фотохимические, окислительно-восстановительные и гидролитические реакции.
Фотохимические превращения. Широко распространенная в естественных условиях солнечная радиация хорошо поглощается некоторыми молекулами. Во многих случаях поглощенная энергия способна индуцировать изменения в молекуле. Ультрафиолетовое излучение наряду с видимой областью спектра также поглощается молекулами некоторых ксенобиотиков. В противоположность этому ионизирующее излучение, также присутствующее в окружающей среде, не настолько сконцентрировано, чтобы вызвать заметный эффект. Энергия широко распространенного в природной среде инфракрасного излучения достаточна лишь для продуцирования минимальных молекулярных изменений, но не для полного превращения молекул.
Фотохимические превращения проходят в три стадии:
– акт абсорбции, который приводит к поглощению излучения определенной длины волны и появлению возбужденного состояния;
– первичный фотохимический процесс, включающий преобразование электронно-возбужденного состояния и его переход в невозбужденное состояние;
– вторичные или «темновые» реакции, происходящие в результате первичного фотохимического процесса. Активные частицы, образующихся в первичных фотохимических процессах, особенно свободные радикалы, могут реагировать с другими молекулами в своем непосредственном окружении, например, с молекулами кислорода или воды. Эти реакции называются «темновыми», а вещества, которые мы обнаруживаем при завершении фотохимических процессов, образуются в результате этих дополнительных изменений. Возбужденные молекулы, т. е. молекулы, эффективно поглощающие энергию излучения, могут также передавать ее молекулам другого ксенобиотика, который затем разрушается. Переход молекулы в возбужденное состояние зависит от распределения электронов, их плотности и т. д.
Чтобы произошла фотохимическая деструкция молекулы ксенобиотика, она должна поглощать солнечное излучение. Поэтому способность вещества перемещаться в атмосфере или оставаться на поверхности определяет степень его деструкции в фотохимических процессах. Ксенобиотики, легко проникающие в глубь почвы, недоступны для фотохимического разрушения.
Степень деструкции ксенобиотика в фотохимических процессах зависит от его свойств. Вещество должно поглощать электромагнитное излучение в доступном интервале длин волн и, кроме того, обладать потенциальной способностью к химическому изменению, т. е. иметь реагирующие на воздействие излучения связи, которые при соответствующих уровнях энергии могут перестраиваться или разрываться.
Окислительно-восстановительные превращения. Многие неорганические и органические вещества могут принимать (восстанавливаться) или отдавать электроны (окисляться). При обсуждении поведения ксенобиотиков в окружающей среде этот процесс приобретает важное значение по следующим причинам:
– окисленные и восстановленные формы данного ксенобиотика могут существенно различаться по биологическим и экологическим свойствам;
– существуют довольно значительные вариации в окислительных или восстановительных условиях в окружающей среде, что влияет на трансформацию ксенобиотиков.
Окислительно-восстановительная (ОВ) способность окружающей среды характеризуется величиной р. Эта характеристика позволяет установить, в какой форме в данной среде может существовать ксенобиотик.
ро = – lg [е-],
где р – показатель активности электрона, указывающий на способность среды отдавать или принимать электроны; рН – показатель активности протона – lg[Н+], т. е. высокий рН соответствует низкой активности Н+, низкий рН – высокой активности Н+.
Поэтому можно провести аналогию между рН как показателем активности протона и р как показателем активности электрона (см. табл. 10.2).
Таблица 10.2
Сопоставление величин рН и р
| рН | Р |
| рН = - lg[Н+] | р = - lg[е-] |
| Высокий рН соответствует низкой активности Н+ | Высокий р соответствует низкой активности электронов |
| Соединение диссоциирует | Соединение находится в «обедненной электронами» или окисленной форме |
| Низкий рН соответствует высокой активности Н+ | Низкий р соответствует высокой активности электронов |
| Соединение не диссоциирует | Соединение «обогащено» электронами или восстановлено |
| рН = рКа + lg ([А-] / [НА]) | р = ро + lg [окисл] / [восст] |
| рКа = рН и [А-] = [НА] | Ро = р и [окисл] = [восст] |
Например, ртуть может существовать в виде двухзарядного катиона, способного выпадать в осадок при взаимодействии с рядом анионов или превращаться микроорганизмами в производные метилртути. Ртуть, восстановленная до элементарной формы, обладает совершенно другими реакционными свойствами и, кроме того, становится довольно летучей. Таким образом, чтобы понять, как она будет вести себя в естественных условиях, очень важно уметь определять, в каких условиях Hg2+ превращается в элементарную ртуть и наоборот.
Другой пример: азот (в зависимости от окислительно-восстановительной способности, присущей природным водам) может существовать в различной степени окисления.
Уровень содержания нитратов в некоторых поверхностных водах, поступающих из сельскохозяйственных угодий или животноводческих ферм, может создать серьезную экологическую проблему. Нитраты содержат азот в самой высокой степени окисления и образуются при высоких значениях р. Являясь сами по себе токсичными, нитраты в ряде случаев способны восстанавливаться до нитритов. Присутствие последних опасно для здоровья людей вследствие их специфического сродства к гемоглобину. Еще более опасна способность нитритов образовывать нитрозоамины, которые являются канцерогенами. Нитриты далее могут восстанавливаться до аммиака, который при природных величинах рН существует в виде ионов аммония.
При низких значениях р азот существует в виде ионов аммония, а в промежуточной области значений р– в форме нитритов.
Таким образом, всесторонний анализ неорганических систем показал, что ОВ характеристики могут оказать существенное влияние на их поведение в природной среде.
Подобный анализ органических систем затруднен, а в принципе и невозможен, но, тем не менее, при определении поведения органических веществ следует также учитывать ОВ характеристики среды. Например, было показано, что скорость деструкции ДДТ четко связана с ОВ потенциалом системы.
Окисление ксенобиотиков может происходить в водной среде за счет растворенного в воде кислорода посредством перекиси водорода, которая выделяется в воду некоторыми гидробионтами, и окислением с участием свободных радикалов.
Токсичность продуктов окисления ряда ксенобиотиков (пестицидов) выше, чем токсичность исходных веществ. Такова ситуация при окислении гептахлора, альдрина, фосфамида.
Вода. Способность вещества вступать в реакции с водой обусловливает реакции гидролиза. Вода, особенно при нагревании, быстро разрушает многие вещества. Эфирные связи, например, в молекулах фосфорорганических соединений, высокочувствительны к действию воды, чем определяется умеренная стойкость этих соединений в окружающей среде.
В этих реакциях, так же как и в фотохимических процессах, необходимо учитывать распределение электронов в молекуле, особенно если это связано с появлением в ней зарядов.
Способность вещества реагировать в воде с ионами водорода или гидроксила в большей степени определяется распределением заряда в его молекуле. При оценке способности вещества вступать в реакции гидролиза необходимо учитывать влияние рН.
Большинство химических реакций включает отталкивание или притяжение электронов, и наиболее сильными атакующими группами в молекуле являются те, которые способны принимать электроны от атакуемой молекулы или отдавать ей их. Водородные ионы и другие группы с дефицитом электронов называются электрофильными («друзья» электронов). Электрофильные группы особенно сильно притягиваются к атому с небольшим отрицательным зарядом, к свободной электронной паре или электронам двойной связи. В катализируемой кислотой реакции разрыва эфирных связей электрофильный ион водорода воздействует на карбонильный кислород и индуцирует небольшой суммарный положительный заряд на карбонильном атоме углерода, который затем реагирует со свободной электронной парой молекулы воды.
Вещества с избытком несвязывающихся электронов являются нуклеофилами. В том же примере молекулы воды действуют как нуклеофилы, поскольку они притягиваются к положительному заряду на карбонильном атоме углерода. В противоположность этому ион гидроксила основания при расщеплении эфира является более сильным нуклеофилом, чем вода, и способен реагировать непосредственно с карбонильным атомом углерода без влияния иона водорода.
Наиболее изучены по сравнению с другими реакции гидролиза эфиров. С другой стороны, замещение гидроксильных групп у фосфорорганических соединений (фосфорной кислоты) азотсодержащими заместителями или галогенами, а также замещение кислорода серой приводят к образованию разнообразных соединений.
Многие галогензамещенные соединения также чувствительны к гидролизу, так как различия в электроотрицательности атомов галогена и углерода обусловливают необходимость разделения заряда.
Адсорбция ксенобиотиков на частицах. Доступность ксенобиотика для ферментов, а также вообще его «деградабельность» снижается в результате еще одного процесса – сорбции молекул на частицах биологического или абиотического происхождения. Процессы сорбции–десорбции ксенобиотиков нередко определяют их устойчивость и взаимосвязаны с переносом в биосфере на большие расстояния.
Из многочисленных примеров важности подобных процессов можно привести следующие. Многие пестициды в почве гидролизуются с образованием соединений, которые адсорбируются на частицах почвы, связываются с гумусом и благодаря этому сохраняются длительное время, т. е. возрастает устойчивость этих токсикантов. В адсорбированном состоянии они не разлагаются фотохимически и не гидролизуются водой. По мере разрушения гумуса грибами (что является ферментативным процессом) ранее связанные молекулы пестицида освобождаются и могут проявить свое токсическое действие на организмы данной экосистемы. Интересно отметить, что подобные пестициды в чисто химическом эксперименте (в водном растворе без почвы) малоустойчивы.
Именно условия реальных биогеоценозов вносят ощутимые поправки в поведение и экологическое значение данного вещества, которые нелегко предсказать исходя только из стандартного набора его физико-химических свойств.
Переходы веществ из одной среды в другую. Изменения физико-химических свойств веществ в результате модификации структуры их молекул, сорбция ксенобиотиков на частицах и др. оказываются существенными при переходе веществ (и продуктов их превращений) из одного блока биогеоценоза в другой. Таковы переходы ксенобиотиков из воды в воздух и обратно, из организмов в воду и обратно, из почвы в воду и т. д.
Подобные переходы могут иметь решающее значение для крупномасштабного перемещения ксенобиотиков в атмосфере. Например, летучесть ряда пестицидов (особенно хлорорганических), их переход в результате испарения из почвы или воды в воздух обусловливает их дальнейший перенос на большие расстояния.
Данные, полученные в последнее время, показывают, что способность ксенобиотиков к миграции значительно выше, чем полагали ранее.
Ксенобиотики переносятся воздушными массами и выпадают в виде пыли, с атмосферными осадками в значительных количествах. Так, ксенобиотик может переноситься из Южного в Северное полушарие и загрязнять среду даже в тех странах, где его применение полностью запрещено.
Подсчитано, например, что в некоторых регионах ежемесячно на землю выпадает 45–270 г ДДТ на 1 км2. С другой стороны, установлено, что из Африки в Америку перемещается 100–400 млн т пыли в год, причем пыль достигает Южной Америки всего лишь за 4–5 суток.
Итак, высокая способность ксенобиотиков и их метаболитов переходить из одного блока экосистемы (почвы или воды) в другие (воздух, биота) порождает экологические проблемы.
По некоторым данным, ДДТ исчезает из почвы за время до 30 лет, альдрин и хлордан – до 15 лет, диэльдрин – до 25 лет, гептахлор – до 14 лет и т. д.
Однако не менее серьезные проблемы возникают и вследствие затрудненности перехода подобного типа. Например, переход ртути из почвы в воду происходит очень медленно (период полувыведения из почвы в поверхностные воды составляет 850 лет). Попавшая в водоемы ртуть далеко не безвредна: она метилируется и накапливается в гидробионтах. Поэтому возникает огромное запаздывание в миграции ртути по биосфере, которое затрудняет борьбу с ртутным загрязнением. В самом деле, даже если удалось бы сегодня полностью прекратить антропогенное загрязнение биосферы (в частности, почвы) ртутью, то все равно еще сотни лет будет продолжаться ее выход (вымывание) из почвы в водоемы, а следовательно, их загрязнение и последующее накопление в гидробионтах.