ОПРЕДЕЛЕНИЕ ПАРЦИАЛЬНЫХ МОЛЬНЫХ ОБЪЕМОВ КОМПОНЕНТОВ БИНАРНОГО РАСТВОРА
ТЕРМОДИНАМИКА РАСТВОРОВ.
ПАРЦИАЛЬНЫЕ МОЛЬНЫЕ ВЕЛИЧИНЫ
РАБОТА № 3
ОПРЕДЕЛЕНИЕ ПАРЦИАЛЬНЫХ МОЛЬНЫХ ОБЪЕМОВ КОМПОНЕНТОВ БИНАРНОГО РАСТВОРА
Цель работы: познакомиться с методами расчета парциальных мольных характеристик, определить парциальные мольные объемы растворителя и растворенного вещества в бинарном растворе.
Только для идеальных растворов общий объем раствора определяется простым суммированием объемов чистых компонентов:
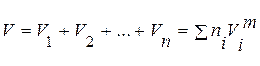 , (1)
, (1)
где V – общий объем раствора, 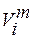 - мольный объем i-того компонента, ni – количество i-того компонента в молях.
- мольный объем i-того компонента, ni – количество i-того компонента в молях.
В реальных растворах суммируются парциальные мольные объемы  компонентов раствора:
компонентов раствора:
 . (2)
. (2)
По определению парциальных мольных величин парциальный мольный объем i-того компонента характеризует изменение общего объема раствора при добавлении к нему 1 моля i-того компонента и при условии, что число молей всех остальных компонентов раствора неизменно.
Математически парциальный мольный объем выражается как частная производная общего объема раствора по числу молей i-того компонента в изобарно-изотермических условиях и при постоянном количестве молей всех остальных компонентов раствора.
 (3)
(3)
На примере бинарного раствора рассмотрим простой способ нахождения парциальных мольных объемов.
Удельный объем раствора Vуд – величина, легко определяемая экспериментально путем измерения плотности раствора:
 , (4)
, (4)
где m – масса раствора, – плотность раствора.
Удельный объем раствора связан с его молярным объемом соотношением:
 , (5)
, (5)
 , (6)
, (6)
где  - средняя молекулярная масса раствора данной концентрации, M1 и M2 – молярные массы растворителя и растворенного вещества; х1 и х2 – мольные доли растворителя и растворенного вещества соответственно, которые рассчитывают из соотношения:
- средняя молекулярная масса раствора данной концентрации, M1 и M2 – молярные массы растворителя и растворенного вещества; х1 и х2 – мольные доли растворителя и растворенного вещества соответственно, которые рассчитывают из соотношения:
 , (7)
, (7)
 - количество молей i-того компонента раствора.
- количество молей i-того компонента раствора.
Очевидно, что для бинарного раствора уравнение (7) примет вид:
 ,
,  , (8)
, (8)
n1 и n2 – число моль растворителя и растворенного вещества соответственно.
Парциальные молярные объемы растворенного вещества или растворителя в растворе заданной концентрации  могут быть найдены графическими методами: методом отсечения (рис. 1) и методом касательных (рис. 2), если установлена зависимость молярного объема раствора от его состава.
могут быть найдены графическими методами: методом отсечения (рис. 1) и методом касательных (рис. 2), если установлена зависимость молярного объема раствора от его состава.
Оба метода основаны на построении касательной к зависимости молярного объема раствора от его состава в точке, отвечающей заданной концентрации. Молярный объем раствора этой концентрации  находят из графика как значение ординаты в этой точке (рис. 1 и 2). Методом отсечения определяют парциальный молярный объем растворителя
находят из графика как значение ординаты в этой точке (рис. 1 и 2). Методом отсечения определяют парциальный молярный объем растворителя  , экстраполируя касательную на ось ординат (рис.1). Методом касательных находят парциальный молярный объем растворенного вещества
, экстраполируя касательную на ось ординат (рис.1). Методом касательных находят парциальный молярный объем растворенного вещества  как угол наклона построенной касательной (рис.2) .
как угол наклона построенной касательной (рис.2) .
Методы отсечения и касательных позволяют найти графически парциальный мольный объем только одного из компонентов раствора (растворителя или растворенного вещества). Неизвестный парциальный мольный объем второго компонента раствора вычисляют, используя свойство аддитивности парциальных мольных величин
 . (9)
. (9)
Экспериментальная часть
Для работы необходимы: набор ареометров для измерения плотности растворов (диапазон измеряемых от 800 до 1200 кг/м3), цилиндры без делений емкостью 100 мл, мерная колба на 100 мл, колбы для приготовления растворов объемом 100-150 мл.
По заданию преподавателя готовят 6-8 растворов разных концентраций, растворяя различные количества вещества g (в граммах) в 100 г воды. Объем воды измеряют мерной колбой на 100 мл, навески взвешивают с точностью 0,01 г.
Растворение, как правило, сопровождается тепловым эффектом, поэтому приготовленные растворы термостатируют (выдерживают) в течение 20-30 минут при комнатной температуре, после чего приступают к измерению плотности.