Предмет орг.химии. Этапы развития. Сырьевые источники. Функциональная группа. Классификация и номенклатура
Изучение соединений углерода – их строения, химических превращений – и составляет предмет органической химии.
Органическая химия как наука оформилась в XIX веке; однако знакомство человека с органическими веществами и применение их для практических целей, несомненно,, начались еще в глубокой древности. Однако в средние века (период алхимии) были известны лишь немногие индивидуальные органические вещества.
Слияние химии соединений растительного и животного происхождения в единую химическую науку органической химии осуществил Й.Берцелиус, который ввел сам термин и понятие органического вещества.
В первой половине 19 в. был накоплен обширный опытный материал и сделаны первые обобщения, определившие бурное развитие органической химии: развиты методы анализа органических соединений (Берцелиус, Ю.Либих,), создана теория радикалов (Вёлер, Ж.Гей-Люссак, Либих, Дюма) как групп атомов, переходящих неизменными из исходной молекулы в конечную в процессе реакции; теория типов (Ш.Жерар, 1853), в которой органические соединения конструировались из неорганических веществ - "типов" (тип водорода, воды, хлористого водорода, аммиака) замещением в них атомов на органические фрагменты; введено понятие изомерии (Берцелиус).
Исследования Э.Франклендом (1852) металлоорганических соединений позволили установить четырехвалентность углерода, заложить основы теории валентности (Ф.Кекуле, 1858) и постулировать существование углерод-углеродных простых и двойных связей.
Бутлеров (1861), который создал классическую теорию химического строения (атомы в молекулах соединяются согласно их валентностям, химические и физические свойства соединений определяются природой и числом входящих в их состав атомов, а также типом связей и взаимным влиянием непосредственно несвязанных атомов). Теория химического строения определила дальнейшее бурное развитие органической химии.
К середине 20 в. органический синтез претерпевает бурное развитие.
Сырьевые источники:
нефть, смолы, природный газ, бурый и каменный угли, горючие сланцы, торф, древесина, растения.
Функциональная группа -Это атом или группа атомов, связанных определённым образом, наличие которых в молекуле органического вещества придаёт ему характерные свойства. (ОН – спирты, NO2 – нитросоединения, например)
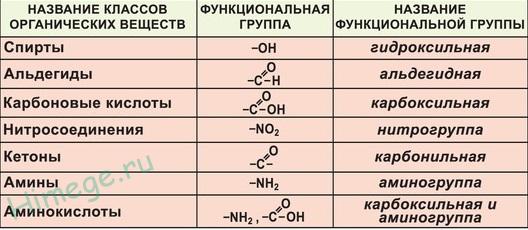
Все органические соединения подразделяют на следующие основные ряды:
I. Ациклические соединения— с открытой цепью углеродных атомов (их называют также алифатическими соединениями, или соединениями жирного ряда):
1. Предельные (насыщенные).
2. Непредельные (ненасыщенные).
II. Циклические соединения— с замкнутой в кольцо цепью атомов.
1. Карбоциклические (изоциклические),— в кольцевую систему которых входят только углеродные атомы:
а) алициклические (предельные и непредельные), б) ароматические.
2. Гетероциклические соединения — в их кольцевую систему, кроме углеродных атомов, входят атомы других элементов — гетероатомы (кислород, азот, сера и т. д.).
Номенклатура.
Тривиальные названия не вытекают из каких-либо единых систематических принципов номенклатуры; они не выражают строения соединения и обычно отражают историю, происхождение веществ, выделение их из природных продуктов, путь синтеза и т. п. (например, рудничный газ, муравьиная кислота, винный спирт, бензол, ванилин, стрептоцид)
По рациональной номенклатуре за основу наименования органического соединения обычно принимают название наиболее простого (чаще всего первого) члена данного гомологического ряда. Все остальные соединения рассматривают как производные этого простейшего гомолога, образованные замещением в нем атомов водорода углеводородными или иными радикалами, атомами или атомными группами.
По Женевской номенклатуре основой (корнем) названия органического соединения является название нормального углеводорода, содержащего наиболее длинную углеродную цепь в называемом соединении. Приставки (префиксы) и окончания (суффиксы) показывают наличие в этой главной цепи боковых цепей (углеводородных радикалов), функциональных групп, нефункциональных заместителей и кратных связей; при этом цифрами обозначают положение боковых цепей, групп или кратных связей в главной углеродной цепи, а греческими (иногда латинскими) числительными — число одинаковых замещающих групп или кратных связей.
2. Типы ХС. Ионная и ковалентная связь. Свойства ковалентной связи. Донорно-акцепторная связь и водородная. Дипольный момент
КОВАЛЕНТНАЯ СВЯЗЬ
Осуществляется за счет электронной пары, принадлежащей обоим атомам. Различают обменный и донорно-акцепторный механизм образования ковалентной связи.
1) Обменный механизм. Каждый атом дает по одному неспаренному электрону в общую электронную пару:
| H• + •H ® H : H | 
| ® | 
|
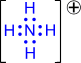
2) Донорно-акцепторный механизм. Один атом (донор) предоставляет электронную пару, а другой атом (акцептор) предоставляет для этой пары свободную орбиталь;
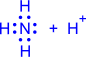
| ® | 
|
Если электронная плотность расположена симметрично между атомами, ковалентная связь называется неполярной (одинаковые элементы)
Если электронная плотность смещена в сторону одного из атомов, то ковалентная связь называется полярной (разные).
ИОННАЯ СВЯЗЬ
Ионы - это заряженные частицы, в которые превращаются атомы в результате отдачи или присоединения электронов.

| ® | 
|
ВОДОРОДНАЯ СВЯЗЬ
Водородная связь - зто связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы. Водородная связь имеет частично электростатический, частично донорно-акцепторный характер.
Характерные свойства ковалентной связи – направленность, насыщаемость, полярность, поляризуемость.
Направленность связи обусловливает молекулярное строение органических веществ и геометрическую форму их молекул.
Насыщаемость – способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей.
Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов. По этому признаку ковалентные связи подразделяются на неполярные и полярные.
Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы.