Гальванічний елемент. Електродні потенціали
Кафедра хімії
Лабораторна робота №7
Взаємодія металів з кислотами.
виконав: Рожненко В.
перевірив: Побережний Л. Я.
Івано-Франківськ
(рік)
Короткі теоретичні відомості
Гальванічний елемент. Електродні потенціали
Характерною властивістю металів є їх здатність лише віддавати електрони, тобто вільні метали можуть виступати тільки в ролі відновників.
Здатність металів до утворення вільних позитивно заряджених йонів яскраво виявляється в реакціях витіснення металів з їхніх солей іншими, активнішими металами або під час взаємодії з кислотами-неокисниками. Наприклад, під час взаємодії цинку з хлоридною або розбавленою сульфатною кислотою відбувається окисно-відновна реакція витіснення Гідрогену Цинком.
Здатність різних металів віддавати електрони оцінюють за реакціями витіснення цих металів з їхніх солей іншими металами. Так, якщо цинкову пластинку занурити в розчин купрум (ІІ) сульфату, то відбудеться окисно-відновна реакція
Zn + Cu2+ = Cu + Zn2+.
Ця реакція відбувається, наприклад, у гальванічному елементі, в якому цинкова пластинка (один електрод) занурена у розчин цинк сульфату, а мідна (другий електрод) – у розчин купрум (ІІ) сульфату. Сполучивши цинковий та мідний електроди з гальванометром і з’єднавши розчини
U-подібною трубкою, заповненою розчином електроліту, дістають гальванічний елемент. Після встановлення у гальванічному колі контакту стрілка гальванометра відхиляється у напрямку до мідного електрода. Це свідчить про те, що під час роботи гальванічного елемента електрони рухаються від цинкового електрода до мідного. Гальванічний елемент - це прилад, що служить для перетворення хімічної енергії окисно-відновної реакції на електричну. У гальванічному елементі електрони переходять від відновника до окисника не безпосередньо, а по провіднику електричного струму – по зовнішньому колу. Цей напрямлений потік електронів і є електричним струмом.
На цинковому електроді елемента відбувається розчинення цинку з перетворенням його атомів на йони, тобто процес окиснення:
Zn - 2e = Zn2+,
а вивільнені електрони по провіднику переходять на мідний електрод, де відбувається розряджання катіонів Купруму (процес відновлення), що супроводжується виділенням металічної міді:
Cu2+ + 2е = Cu.
Сумарне рівняння реакції, внаслідок якої у колі виникає електричний струм, матиме вигляд
Zn+Cu2+ = Zn2+ + Cu.
Електрод, на якому відбувається процес окиснення, називається анодом, а електрод, на якому відбувається процес відновлення,– катодом.
Електрорушійною силою E гальванічного елемента називається максимальне значення напруги гальванічного елемента, що відповідає перебігу реакції в прямому і зворотному напрямках.
Електрорушійна сила гальванічного елемента дорівнює різниці потенціалів між його електродами.
Для обчислення E від величини потенціалу катода слід відняти величину потенціалу анода. В гальванічному елементі, як уже зазначалось, катодом є позитивно заряджений електрод, анодом – негативно заряджений (під час електролізу – навпаки).
Якщо стандартна е. р. с. гальванічного елемента E° має додатну величину (ΔG° < 0), то це означає, що дана реакція йде в прямому напрямку, а якщо від’ємну – у зворотному.
Виміряти абсолютні значення електродного потенціалу φ неможливо, оскільки в будь-якому гальванічному елементі одночасно відбуваються дві електродні реакції, і його напруга дорівнює різниці електродних потенціалів. Тому на практиці користуються відносними електродними потенціалами. Електродом порівняння є стандартний водневий електрод, потенціал якого умовно прийняли таким, що дорівнює нулю.
На практиці як електроди порівняння найчастіше застосовують хлорсрібний і каломельний.
Окисно-відновним електродним потенціалом, або редокс-потенціалом, системи називають різницю потенціалів між електродом, зануреним у дану хімічну систему, і стандартним водневим електродом.
Отже, редокс-потенціал системи можна оцінити за електрорушійною силою гальванічного елемента, один з електродів якого занурений у суміш окисненої (Ox) та відновленої (Red) форм досліджуваного елемента, що містяться в розчині, а другим є стандартний водневий електрод.
Стандартний електродний потенціал – це значення потенціалу за стандартних умов і активностей окисненої та відновленої форм елемента, що бере участь у реакції, які дорівнюють одиниці.
Якщо активності речовин у розчині, що досліджується, не дорівнюють одиниці, то е. р. с. гальванічного елемента, який складається з водневого і досліджуваного електродів, наприклад електрода Fe3+/ Fe2+, обчислюють за рівнянням Нернста:
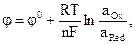
де φ° – стандартний електродний потенціал; R – універсальна газова стала; T – абсолютна температура; n – число електронів, що беруть участь у процесі; F – число Фарадея; а0х і аRed – активності відповідно окисненої і відновленої форм елементів, що беруть участь у процесі.