Отчёт по лабораторной работе № 8
Кафедра общей и технической физики
Тема: «Определение показателя адиабаты при адиабатическом расширении газа»
Выполнил: студент гр. ГМ-12 ______________ /Аткачёв С.В./
(подпись) (Ф.И.О.)
Проверил: доцент ____________ /Левин К.Л./
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2013 г.
Цель работы: – изучить законы идеального газа и основные положения классической теории теплоёмкости; определить коэффициент Пуассона g - отношение теплоёмкости при постоянном давлении Ср к теплоемкости при постоянном объеме CV методом адиабатического расширения (методом Клемана - Дезорма).
Общие сведения
Количество тепла, которое необходимо сообщить одному молю вещества, чтобы повысить его температуру на 1 К, называют молярной теплоемкостью.
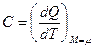
где Q – количество тепла, подводимого к системе, Т – абсолютная температура, M – масса газа, m – масса одного моля газа.
Как показывают теория и опыт, теплоемкость зависит от условий, при которых нагревается газ, т.е. от характера термодинамического процесса.
Теплоёмкость газа при постоянном давлении (Сp) больше теплоёмкости при постоянном объёме (Cv). Это легко показать качественно на основании первого начала термодинамики: количество тепла Q, подводимого к системе, идет на увеличение внутренней энергии системы DU и на совершение этой системой работы A над внешними телами.
Q=dU+A (1)
Если газ нагревается при постоянном объеме, то работа не совершается и все подводимое тепло идет на увеличение запаса его внутренней энергии U, т.е. только на повышение температуры газа. Если же газ нагревается при постоянном давлении, он расширяется и производит работу, требующую дополнительного расхода тепла. Таким образом, для повышения температуры газа на определённую величину в изобарном процессе требуется большее количество теплоты, чем при изохорном.
Как следует из теории
Cp = CV + R (2)
где R – универсальная газовая постоянная.
Выражение (2) носит название соотношения Р.Майера.
Отношение g=Ср/CV входит в уравнение Пуассона, описывающее адиабатический процесс, т.е. процесс, идущий без теплообмена с окружающей средой (Q = 0):
 . (3)
. (3)
Здесь p1 и V1 - давление и объем газа в первом состоянии; p2 и  - давление и объем газа во втором состоянии .
- давление и объем газа во втором состоянии .
Полную теплоизоляцию газа от внешней среды осуществить невозможно. Однако, если параметры состояния газа изменяются очень быстро, процесс можно приближенно считать адиабатическим. На практике адиабатический процесс совершается в некоторых тепловых двигателях (например, в двигателе Дизеля); распространение звука в газах (быстрое периодическое изменение давления в малых областях пространства) также протекает адиабатически.