Технология приготовления сусла 5 страница
Таблица 2.10. Показатели затора в зависимости от температуры
| Температура, °С | 50/60 | ||||
| Конечная степень сбраживания, % | 87,5 | 86,5 | 76,8 | 54,0 | 88,2 |
| Температура, °С | |||||
| Продолжительность осахаривания, мин | |||||
| Значение pH | 6,08 | 5,86 | 5,64 | 5,42 | 5,19 |
| Конечная степень сбраживания, % | 72,7 | 76,5 | 77,0 | 77,4 | 69,9 |
| Продолжительность осахаривания, мин | 20-25 | 10-15 | 15-20 |
Конечная степень сбраживания и состав сахаров улучшается, если затирание проводить при температурах ниже оптимальных. В этом случае происходит растворение эндосперма под действием ферментов, которое при наступлении оптимальных температур может усилиться. Осахаривание при температуре 76 °С идет так быстро потому, что уже в ходе нагревания конгрессного сусла наблюдаются описанные выше процессы набухания, клейстеризации и ферментативного расщепления. Например, при относительно высоких температурах затирания вполне возможно, что инактивация ферментов будет происходить быстрее, чем расщепление составных частей эндосперма. В этом случае затор не будет характеризоваться нормальным йодным окрашиванием и, следовательно, скорость нагревания затора до температуры осахаривания влияет и на конечную степень сбраживания, и на продолжительность осахаривания.
Реакционная способность затора влияет как на конечную степень сбраживания, так и на продолжительность осахаривания, что объясняется различным оптимумом значения pH для обеих амилаз. Если снижение значения pH с 5,8 до 5,4 способствует усилению активности ß-амилазы, то действие α-амилазы при этих значениях pH уже ограничено. Кроме того, затирание с использованием воды с высокой остаточной щелочностью отрицательно сказывается на конечной степени сбраживания сусла.
Увеличение продолжительности осахаривания приводит к повышению конечной степени сбраживания сусла лишь при пониженных температурах (табл. 2.11).
Таблица 2.11. KCC в зависимости от продолжительности осахаривания
| Продолжительность осахаривания, мин | ||
| Конечная степень сбраживания: | ||
| при 62 °С | ||
| при 70 °С |
При 70 °С дальнейшего повышения степени сбраживания не происходит, так как ß-амилаза уже инактивирована, однако может наблюдаться дальнейшее расщепление высокомолекулярных декстринов в низкомолекулярные.
Влияние концентрации затора на расщепление крахмала при хорошо растворенном солоде незначительно. При высокой концентрации (1 : 2,5) несколько возрастает образование мальтозы (благодаря действию защитных коллоидов), однако действие α-амилазы может ингибироваться, что проявляется в увеличении продолжительности осахаривания.
Тонкость помола определяет скорость экстрагирования фермента и субстрата, однако она больше сказывается на образовании гексоз, чем на общем количестве сбраживаемых Сахаров. При этом уменьшается время до наступления нормального йодного окрашивания.
2.3.1.2. Расщепление белков имеет такое же важное значение, как и гидролиз крахмала, хотя в процессе расщепления участвует и относительно небольшое их количество. При солодоращении гидролиз азотсодержащих веществ происходит значительно интенсивнее, чем гидролиз крахмала, и при затирании образуется значительно больше труднорастворимых соединений азота, чем при солодоращении.
Между процессами расщепления крахмала и белка имеются существенные отличия. Если крахмал солода выступает в процессе затирания как однородное вещество со сравнительно простой структурой, то белковые вещества солода представляют собой смесь всевозможных азотсодержащих веществ - от высокомолекулярных нативных белковых соединений до простейших структурных элементов белковой молекулы (аминокислот). Кроме того, расщепляющие белок ферменты представляют собой не два вполне определенных фермента, а многообразный комплекс эндо- и экзопетидаз, действующих в различных условиях, причем часть белков может осаждаться под влиянием температуры или pH затора.
Важнейшие для нас азотсодержащие соединения можно разделить на собственно белки и продукты их расщепления. Первые уже присутствовали в ячмене (они или не были расщеплены во время проращивания, или в ходе проращивания снова накопились в листке зародыша). Речь идет о нерастворимых в заторе и сусле глютелинах и проламинах, а также о растворимых белковых веществах, например, альбуминах и (частично) о глобулинах (см. раздел 1.1.2.8).
Важнейшими продуктами расщепления белка солода, образующимися при проращивании под действием протеолитических ферментов, являются макропептиды, полипептиды, простые пептиды и аминокислоты (см. раздел 1.4.1.2). При затирании солода растворимые азотсодержащие вещества переходят в затор. В ходе затирания они подвергаются дальнейшему расщеплению протеолитическими ферментами (в случае их способности к расщеплению). Первоначально нерастворимые белковые вещества под воздействием ферментов переходят в растворимую форму, хотя большая их часть остается в дробине нерасщеплённой. Содержание растворимого азота во время затирания увеличивается: эндопептидазы воздействуют на нативный белок и расщепляют его с образованием полипептидов и (при увеличении длительности воздействия) низкомолекулярных соединений, а экзопептидазы переводят эти продукты расщепления в аминокислоты.
Хотя в процессе затирания происходит абсолютное увеличение доли низкомолекулярного азота (в первую очередь аминокислот), под действием эндопептидаз из протеинов образуются высокомолекулярные соединения, благодаря чему практически не наблюдается снижения содержания высокомолекулярных фракций.
Растворенные в сусле нативные белковые вещества, например альбумины и глобулины, осаждаются при высоких температурах затирания, особенно во время кипячения. Высокомолекулярные продукты расщепления белков также могут быть склонны к коагуляции благодаря реакции с дубильными веществами солода, а средне- и низкомолекулярные фракции в сусле всегда сохраняют растворимую форму.
Содержание проламинов, представляющих собой резервные белки, зависит от сорта ячменя и растворимости солода. При гидролизе они дают в основном пролин и глютаминовую кислоту, а также цистеин и цистин. Проламины частично расщепляются при затирании и переходят в растворимую форму. Благодаря процессам окисления образуются высокомолекулярные полипептиды, которые при повышенных температурах затирания становятся нерастворимыми и образуют в дробине своего рода «тесто». Они могут затруднять процесс фильтрования сусла. Аналогичное поведение свойственно и так называемым «гельпротеинам», образующимся в ходе солодоращения в результате редуцирования дисульфидных мостиков. Благодаря процессам окисления при затирании они могут образовывать высокомолекулярные соединения, в состав которых входят глютелины и альбумины. Благодаря гидрофобным свойствам глютелинов происходит также адсорбция липидов. Мелкие зерна крахмала, β-глю-каны и пентозаны, связанные с протеинами, также участвуют в образовании белковых комплексов, образующих указанное «тесто» и могут затруднить высвобождение зерен крахмала и тем самым - действие амилаз; замедляется также фильтрование.
Следует упомянуть также гликопротеиды, представляющие собой белки, связанные с углеводородной группой ковалентной связью. При солодоращении они расщепляются по мере процесса растворения, а при затирании - во время длительных пауз при температурах 50-65 °С. При температуре 70-72 °С в течение 60-90 мин происходит высвобождение из гликопротеидов высокомолекулярных групп, которые больше не расщепляются, в результате чего возрастает вязкость сусла. Гликопротеиды способствуют повышению пеностойкости пива.
Значение высокомолекулярных групп, с одной стороны, для пенообразующих свойств пива, полноты вкуса, способности связывать углекислоту, для небиологического помутнения, а с другой - значение аминокислот для питания дрожжей позволяют сделать вывод о том, что процесс расщепления белков не должен быть ни очень коротким, ни излишне глубоким. Следствием слишком низкого расщепления белков может стать недостаточная стабильность пива, а также неудовлетворительное питание дрожжей. В результате излишне глубокого расщепления белков при данном качестве солода получается пиво с неполным вкусом и недостаточной стойкостью пены, а при определенных обстоятельствах - пиво, подверженное инфицированию.
Получение желаемой степени расщепления белков зависит от степени растворимости белка и содержания ферментов в солоде, а также от условий затирания, в частности, от температуры и продолжительности ее воздействия, от pH затора и его концентрации.
У солода с высокой степенью растворения белка следует избегать слишком интенсивного расщепления белков, а у малорастворенного солода в ходе затирания требуется соответствующая коррекция расщепления белков. Оптимальные условия для действия протеолитических ферментов (протеаз) приведены в табл. 2.12.
Таблица 2.12. Оптимальные pH и температура для действия протеаз
| Фермент | Значение pH | Температура, °С |
| Эндопептидаза | 5,0 | 40-50(60) |
| Карбоксипептидаза | 5,2 | 50 (60) |
| Дипептидаза | 8,2 | 40-45 |
| Аминопептидаза | 7,2 | 40-45 |
Оптимальные значения pH и температуры для действия эндо- и карбоксипептидаз примерно совпадают, но первые более чувствительны к действию температуры и продуцируют меньше свободных концевых групп, тогда как карбоксипептидазы могут гидролизировать белки до аминокислот.
Таким образом, содержание и активность эндопептидаз является лимитирующим фактором для дальнейшего расщепления образовавшихся пептидов до аминокислот. Карбоксипептидазы отвечают за образование 80 % аминокислот, выделяющихся при затирании, так как дипептидазы при значениях pH затора действуют ограниченно, а аминопептидазы расщепляют пептиды до аминокислот только при пониженных температурах и значениях pH затора более 6.
Температурный интервал, наиболее благоприятный для гидролиза белка, сравнительно широк (40-60 °С), причем при температуре 50 °С наблюдается явный пик. Вне этих температурных границ протеолиз постоянно уменьшается, а при температуре около 80° С полностью прекращается. При температурах 45-50 °C доля низкомолекулярных азотсодержащих соединений по сравнению с высокомолекулярными несколько возрастает, а при температурах 60-70 °С происходит усиленное образование коллоидных высокомолекулярных азотистых соединений. При этом возможность воздействия на этот процесс с учетом указанных выше сходных оптимальных условий для действия эндопептидаз и карбоксипептидаз, невелика. После температур расщепления белка, которые в большинстве случаев поддерживаются на уровне 47-53 °С в виде «белковой паузы», применяют более высокие температуры, необходимые для осахаривания затора. При 65-70 °C еще отмечается заметное растворение белка, идущее тем интенсивнее, чем больше ферментов сохранилось при пониженных температурах. Растворимые протеазы при температуре 70 °С быстро инактивируются, а ферменты, первоначально нерастворимые и перешедшие в раствор после гидролиза соединений, находящихся в протоплазме, при этой температуре способны некоторое время действовать. Можно предположить, что именно эти десмоферменты ответственны за то, что даже при высоких температурах затирания не удается довести растворение белка ниже значения, заданного сортом солода. Ускорение процесса расщепления белков и, таким образом, увеличение содержания растворимого азота происходит в том случае, если затирание проводится при температурах ниже оптимальных, так что к моменту наступления температур гидролиза азотсодержащие соединения эндосперма и ферменты оказываются уже растворенными. При декокционном способе затирания температурный интервал между белковой паузой и температурой затора после возвращения отварки также влияет на растворение и состав азотсодержащих веществ. Чем выше разность температур после возвращения первой и второй отварок, тем хуже растворяются в сусле белковые вещества, причем при этом происходит изменение фракционного состава белковых и увеличение содержания высокомолекулярных азотистых соединений.
Влияние продолжительности белковой паузы определяется соответствующей температурой. При постоянной температуре затирания содержание различных фракций азота сначала непрерывно возрастает, и хотя содержание высокомолекулярного азота растет в абсолютном отношении, его доля в общем азоте сокращается. Доля низкомолекулярпых соединений, в первую очередь аминокислот, увеличивается как в абсолютном, так и процентном отношении, однако в ходе белковой паузы скорость инактивации ферментов превышает скорость их растворения. Так, например, протеолитическая активность оставшейся части затора при двухотварочном способе во время примерно двухчасового нахождения в заторном аппарате при температуре 50 °С снижается примерно в 2 раза по сравнению с исходным значением. Благодаря введению отварки она еще раз кратковременно активизируется, однако при температуре около 65 °С эта фаза сменяется быстрым и продолжительным спадом протеолптической активности.
Нa активность протеаз существенно влияет значение pH затора. Чем больше оно приближается к 5,0, тем больше возрастает содержание всех фракций, включая низкомолекулярные азотсодержащие соединения. Вода с высокой остаточной щелочностью замедляет протеолиз, и напротив, устранение карбонатной жесткости воды, добавление гипса, хлорида кальция или даже подкисление может значительно его усилить.
Концентрация затора важна для ферментативной активности вследствие действия защитных коллоидов. В концентрированных заторах (в первой и второй отварке - 1 : 2,5) содержание низкомолекулярного азота возрастает сильнее, чем в разбавленных частях.
Контроль расщепления белков можно вести путем определения содержания растворимого азота, коагулируемого азота и высокомолекулярных фракций. Желательно проводить регулярную проверку доли ассимилируемого азота в общем азоте горячего охмеленного сусла, которую можно примерно определить по содержанию формольного азота (33 %) или по содержанию α-аминного азота (22 %). Высокомолекулярный азот, стимулирующий ценообразование и полноту вкуса, следует указывать в процентах к растворимому азоту. Контролируемой величиной является также интенсивность затирания по Кольбаху (число Кольбаха), нормальное значение которого составляет 104, высокое - более 110, а низкое - ниже 100. Простого и ускоренного оперативного метода контроля расщепления белков (типа йодной пробы для определения степени расщепления крахмала), до сих пор не выработано.
2.3.1.3. При затирании продолжается также расщепление гемицеллюлоз и гумми-веществ, начавшееся при солодоращении. Изначально гемицеллюлозы солода нерастворимы. Они состоят из высокомолекулярных ß-глюканов и пентозанов и связаны с высокомолекулярными белковыми соединениям клеточных стенок одной эфирной связью (гидроксильная группа ß-глюканов с карбоксильной группой протеинов). В результате воздействия ß-глюкансолюбилазы - карбоксипептидазы, которая может действовать и как эстераза, гемицеллюлозы переходят в раствор при температурах выше 55 °С и до 70 °С. Они повышают вязкость затора и сусла. Высвободившиеся ß-глюканы состоят из глюкозных единиц с ß-1,4-и ß-l,3-cвязями (в отношении 70 : 30). Хотя последовательность из двух-трех ß-l,4-cвязeй преобладает над ß-l,3-cвя-зью, могут также существовать цепочки из ß-1,4- и ß-13-связей, которые затрудняют расщепление с помощью эндо-ß-1,4-глюканазы, а также неспецифической эндо-ß-глюканазы (оптимальная температура - 40-45 °С, pH 4,7-5,0, инактивация при температуре выше 50 °С) и менее эффективной эндо-ß-1,3-глюканазы (оптимальная температура 60 °С, pH 4,6/5,5, инактивация при температуре выше 70 °С). Экзо-ß-глюканазы еще более чувствительны, чем эндо-ß-1,4-глюканаза. Так как ß-глюкансолюбилаза оказывает заметное действие в интервале температур 63-70 °С, то эндо-ß-глюканазы способны лишь ограниченно расщеплять высокомолекулярный вязкий ß-глюкан, высвободившийся при этих температурах. Расщепление пентозанов, состоящих из арабоксилана, происходит под действием эндо- и экзоксиланаз (оптимальная температура 45 °С), а также арабинозидазы (оптимальная температура 40-45 °С), причем степень превращений здесь существенно меньше, чем под действием глюканаз.
Расщепление гемицеллюлоз протекает в несколько этапов:
a) сначала в раствор переходят свободные гумми-вещества, уже имеющиеся в солоде, повышая вязкость затора;
b) в диапазоне температур 35-50 °С под действием эндо-ß-1,4-глюканаз и неспецифических эндо-ß-глюканаз происходит расщепление этих высокомолекулярных соединений до глюкано-декстринов и веществ с более низкой молекулярной массой. Вязкость снижается;
c) при температурах 45-55 °С при участии эндо-ß-глюканаз продолжается растворение экстракта с высвобождением β-глюканов, которые вследствие ослабления действия эндо-ß-глюкана-зы расщепляются довольно медленно. При этом возможно действие эндо-ß-1,3-глюканазы;
d) начиная с температуры 55 °С и до 70 °С ß-глюкансолюбилаза отщепляет высокомолекулярный ß-глюкан от его соединений с белком. Содержание ß-глюкана и вязкость возрастают тем больше, чем выше температура в интервале 60-70 °С, так как при 60 °C эндо-ß-1,3-глюканаза еще способна оказывать определенное воздействие, а начиная с температуры 65 °С она все больше ингибируется. Эндо-ß-1,4-глюканаза больше не действует, так как она была инактивпрована уже при температуре 50-55 °С.
Количество ß-глюкана, освободившегося при затирании, зависит в первую очередь от степени и однородности растворения солода. Содержание ß-глюкана в сусле из солода с разной степень растворения может различаться в 10-14 раз. Особенно неблагоприятными являются смеси из солода со значительно различающимся цитолизом компонентов, особенно их солода с непроростками.
На расщепление вязких веществ влияют температура затирания, белковые паузы и, в меньшей степени, значение рH затора. Такое расщепление лучше всего протекает при температурах около 45 °С, а более низкие температуры затирания, например 35 °С перед паузой при 50 °C, существенно усиливают процесс превращений. Следствием повышенных температур затирания (порядка 62 °С) является быстрая инактивация эндо-ß-глюканаз, и в этом случае сусло характеризуется высоким содержанием гумми-веществ. Тем не менее подбором способа затирания содержание ß-глюкана при работе со слаборастворенным солодом можно скорректировать лишь примерно на 30%.
Содержание пентозанов изменяется в меньшей степени. Большие различия наблюдаются у слабо и неравномерно растворенного солода также в содержании в дробине гумми-веществ, которые могут замедлять процесс фильтрования. Так как гумми-вещества влияют на пенообразование и полноту вкуса пива, то слишком глубокого расщепления белков в случае хорошо растворенного солода следует избегать. В данном случае целесообразнее использовать повышенные температура затирания (55-62 °С). Контроль расщепления ß-глюкана можно осуществлять по вязкости горячего охмеленного сусла (ниже 1,85 мПа в 12%-ном экстракте) или непосредственно по содержанию в сусле ß-глюкана (менее 200 мг/л).
2.3.1.4. Изменение содержания фосфатов. Содержащиеся в солоде кислые фосфатазы расщепляют органические фосфаты солода. При этом выделяется фосфорная кислота, которая затем реагирует с первичными фосфатами и диссоциирует ионы водорода. Вследствие этого повышается кислотность затора, что проявляется в снижении значения pH и повышении буферности затора, сусла и пива. Оптимальные условия для действия фосфатаз - pH 5,0 и температура 50-53 °С. Эти ферменты действуют и при более высоких температурах, так как каждая пауза (при 50, 62, 65 и даже при 70 °С) повышает буферность, но их активность снижается (наиболее предпочтительна температура 50 °С). Самые низкие значения pH, а также самая низкая буферность затора достигаются при температуре затирания 62-65 °С. Снижение значения pH затора приводит к повышению буферности, которая впоследствии может ослабить снижение pH в ходе брожения.
2.3.1.5. Расщепление липидов. Вместе с солодом в затор вносятся липиды, состоящие в основном из триглицеридов, моно-и диглицеридов, свободных жирных кислот и нейтральных липидов (например, фосфолипидов). На расщепление липидов влияют два различных фактора. С одной стороны, на них действуют липазы, расщепляющие липиды до глицеридов (глицерина) и свободных жирных кислот (оптимальные температуры - 35-40 и 65-70 °С). Благодаря действию липаз возрастает содержание свободных жирных кислот. С другой стороны, жирные кислоты окисляются липоксигеназами (при 35-50 °С), что проявляется в уменьшении содержания линолевой и линоленовой кислот по сравнению с их первоначальным содержанием в солоде. После инактивации липоксигеназ при температуре 65 °С (втором оптимальном диапазоне для липаз) наблюдается существенное увеличение содержания линолевой и линоленовой кислот. Действие липоксигеназ зависит от потребления кислорода при затирании.
Содержание липидов в заторе при правильном фильтровании удерживается на определенном уровне или они осаждаются в процессе кипячения сусла.
2.3.1.6. На содержание полифенолов и антоцианогенов при затирании влияют несколько процессов. С повышением температуры и продолжительности затирания увеличивается их растворение. Фенольные и полифенольные соединения освобождаются в ходе двух параллельно протекающих реакций расщепления, например, расщепления белков и гликозидов. Их количество уменьшается также под действием пероксидаз (в диапазоне температур 40-50 °С) или полифенолоксидаз, наиболее активных при температуре 60-65 °С. Так как изменения в содержании полифенолов особенно четко выражены при температурах 40-50 °С (особенно если при одноотварочном способе затирания или в результате перемешивания происходит аэрация затора), то повышенные температуры затирания, например до 62 °С, вызывают увеличение содержания полифенолов в заторе и сусле. При доступе воздуха происходит снижение общего содержания полифенолов и антоцианогенов, в результате чего ухудшается индекс полимеризации. Из сильно растворенного солода в затор переходит больше полифенолов желаемого состава (см. раздел 1.4.1.6); в солоде, высушенном при высоких температурах, присутствует лишь незначительное количество оксидаз, благодаря чему поддерживается высокое содержание в сусле полифенолов и антоцианогенов.
2.3.1.7. Содержание цинка в заторе важно потому, что этот микроэлемент входит в состав алкогольдегидрогеназы. Недостаток цинка в начальном сусле проявляется в плохом размножении дрожжей, затяжном главном брожении и дображивании, а также в неполном восстановлении диацетила или его предшественника 2-аце-толактата. В солоде содержится 3-3,5 мг цинка на 100 г CB, причем наибольшая концентрация цинка отмечается во внешних слоях зерна (оболочке и алейроновом слое). При затирании в раствор переходит лишь 20-25% цинка, после чего содержание цинка постоянно уменьшается до 0,05-0,20 мг/л (в отфильтрованном пивном сусле). Еще одно сильное снижения содержания цинка происходит при кипячении сусла. Его содержание не должно превышать 0,15 мг/л.
Эксперименты показали положительное влияние следующих параметров затирания на содержание цинка: проведение затирания при температуре 45-50 °С, пауза в течение 30-60 мин, значение pH 5,45, небольшой главный налив при затирании (соотношение засыпь : налив - 1 : 2,5) и добавление горячей воды в ходе повышения температуры до соотношения засыпь : налив 1 : 4.
2.3.1.8. Окисление компонентов затора на фракции проламина или гельпротеинов может препятствовать расщеплению крахмала, β-глюканов и белков. Содержание полифенолов снижается, но прежде всего уменьшается содержание более чувствительных антоцианогенов и танноидов. Этот процесс фермеитативно катализируется пероксидазами (оптимальная температура - 45 °С) и полифенолоксидазами (оптимальная температура - 65 °С). Получаемые в результате сусло и пиво характеризуются более темным цветом, более размытым и менее стабильным вкусом.
Степень поглощения кислорода при затирании зависит от оборудования, например, от устройств подачи затора, подсоса воздуха при перекачивании, а также от интенсивности перемешивания. Имеет значение и форма заторных аппаратов - например, в прямоугольных заторных аппаратах для получения хорошего затора требуется более интенсивное перемешивание. Рекомендуется подача затора солода в аппарат снизу и перекачивание затора через сливные клапаны. Прямое определение содержания кислорода в заторе невозможно из-за активности оксидаз; косвенную оценку поглощения кислорода получают путем моделирования затирания с помощью раствора сульфита натрия по расходу этого реагента. В неблагоприятных условиях его расход составляет до 200 мг/л в течение всего процесса затирания, а в оптимизированных условиях варочных цехов - около 30-40 мг/л.
Отсутствие доступа кислорода при затирании приводит к усиленному расщеплению белков, проявляющемуся в повышении содержания растворимого азота и снижении содержания высокомолекулярных фракций в пользу свободного α-аминного азота. Расщепление ß-глюка-на проходит интенсивнее, как и расщепление крахмала, что проявляется в повышении конечной степени сбраживания и более благоприятных значениях йодной пробы. Содержание полифенолов (особенно антоцианогенов и танноидов) существенно возрастает. Во избежание слишком глубокого расщепления белков необходимо при известных условиях скорректировать параметры затирания.
Практика затирания
2.3.2.1 Процесс затирания начинается со смешивания дробленого солода с заторной водой. При этом большое значение имеют количество воды, используемой для растворения дробленого солода (то есть соотношение солода и воды), а также температура, при которой заторная вода добавляется к данному количеству солода.
2.3.2.2. Количество солода, которое должно быть переработано за одну варку, называют засыпью, а количество воды, используемой для этого процесса, - наливом. Смесь солода и воды называется затором. Налив подразделяют на главный налив и долив. Общее количество воды, необходимое для приготовления сусла, добавляется к засыпи не за один раз - сначала добавляется вода, требующаяся для растворения компонентов солода и биохимических превращений (главный налив). Получаемый раствор экстракта называют первым суслом. Промывная вода предназначена для вымывания остатков экстракта, сохранившихся в дробине после фильтрования первого сусла.
Для состава первого сусла большое значение имеет главный налив, а количество промывной воды влияет на полноту выделения экстракта. Оба эти фактора взаимосвязаны - если главный налив больше, то количество промывных вод меньше, и наоборот. Соотношение этих двух показателей у светлых и темных сортов пива принципиально отличается. Распределение общего количества воды на главный налив и промывные воды называются ведением налива.
Состав сусла зависит от объема главного налива, так как концентрация затора влияет на ферментативную активность. При высокой концентрации действие некоторых ферментов замедляется, а отдельные процессы расщепления протекают интенсивнее и глубже, чем в жидких заторах. В основном это сказывается на скорости осахаривания, которая в более плотных заторах замедляется. Объем главного налива влияет и на фильтрование. Количество экстракта, остающегося в дробине после выпуска первого сусла, тем больше, чем меньше главный налив и чем выше концентрация первого сусла, причем изменяется не только доля выхода экстракта, приходящаяся иа первое сусло и промывные воды, но и способ промывания дробины. Чем больше первого сусла задерживается в дробине, тем сильнее ее необходимо промывать. Уменьшение выхода экстракта с первым суслом обусловливает увеличение его выхода с промывными водами. Необходимость усиленного промывания дробины способствует повышенному выщелащиванию красящих и других веществ, неблагоприятно сказывающихся на качестве светлого пива. Таким образом, величина главного налива является одним из основных факторов, обусловливающих тип и качество пива, так как от нее зависит целый ряд последующих технологических мероприятий. Она должна быть строго определенной и не изменяться от варки к варке. Расчет главного налива и общего объема затора производится по приведенным ниже формулам.
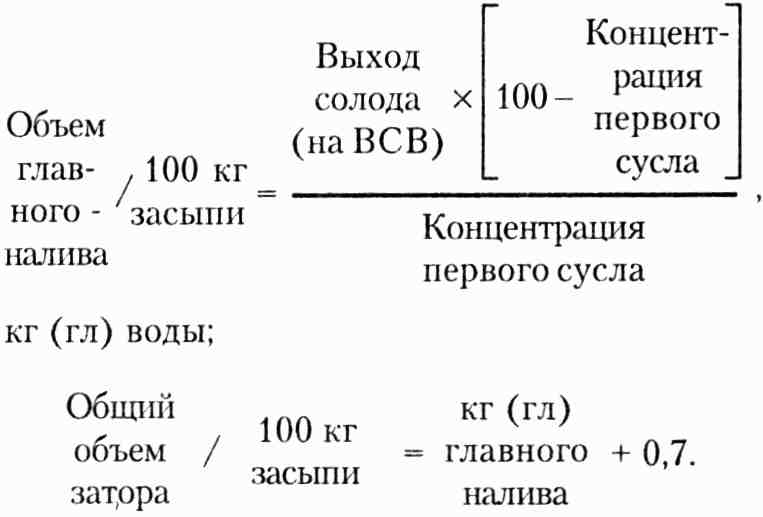
С помощью слагаемого 0,7 учитывается объем затираемого дробленого солода на 100 кг.
На практике расход воды несколько выше, так как, во-первых, при кипячении затора вода испаряется, а во-вторых, вода по-разному подкачивается для опорожнения емкостей и трубопроводов. Во избежание колебания соотношения первого сусла и промывных вод первое сусло всегда должно иметь одну и ту же концентрацию, для чего рекомендуется провести калибровку заторного и фильтрационного аппаратов и определять количество затора, получаемого в каждой варке.