Опреснение воды с использованием прямого осмоса
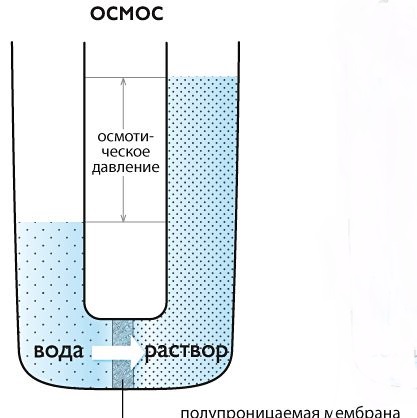
Прямой осмос — процесс односторонней диффузии (проникновения) молекул воды через полупроницаемую мембрану в раствор с большей концентрацией растворённого вещества. Создаваемое при этом давление, называется осмотическим.
Например, дерево обеспечивает свое питание водой за счет осмоса: в его «теле» в соках растворены сахара, и поэтому вода из грунта стремится попасть через поверхность корней внутрь, создавая избыточное давление, которое и гонит воду наверх.
 Прямой осмос (или обычный осмос) – это физический процесс самопроизвольного перехода растворителя (чистая вода) в раствор (вода с растворёнными солями) через полупроницаемую мембрану.
Прямой осмос (или обычный осмос) – это физический процесс самопроизвольного перехода растворителя (чистая вода) в раствор (вода с растворёнными солями) через полупроницаемую мембрану.
Если сосуд разделить полупроницаемой мембраной и слева налить раствор любого вещества, а справа – чистый растворитель, то будет наблюдаться явление переноса чистого растворителя в раствор и достраивание гидратных оболочек (если растворитель вода). Чем выше концентрация растворенного вещества в сосуде слева, тем больше молекул воды должно перейти через мембрану в раствор.
Количественно этот перенос выражается величинойосмотического давления (Р0):
Р0 = C*R*T,
где С– массовая концентрация растворенного вещества;R – газовая постоянная; Т – абсолютная температура.
Если осмотическое давление (Р0) превышает гидравлическое (Рr), то происходит прямой осмос.
Движущей силой прямого осмоса (обычного осмоса) при первом приближении является разность концентраций двух растворов, разделённых полупроницаемой мембраной. Чем она больше, тем выше объем и скорость потока на мембране, а, следовательно, и количество энергии. Это свойство прямого осмоса в последнее время представляет огромный интерес для генерации электроэнергии. Первая электростанция прямого осмоса запущена в 2009 году в Норвегии.
Опреснение воды с использованием прямого осмоса
Суть процесса состоит в следующем: с одной стороны полунепроницаемой мембраны находится солёная вода, которую нужно опреснить; с другой стороны мембраны — концентрированный раствор специально подобранного вещества. Под действием сил прямого осмоса пресная вода просачивается сквозь мембрану со стороны солёной воды в сторону концентрированного раствора, разбавляя его. После чего меняют температуру полученного раствора, вещество покидает (разлагается либо выпадает в осадок) раствор, и в итоге получается раствор концентрации меньшей, чем исходная солёная вода.
Далее уже полученный раствор подвергается опреснению тем или иным методом, — в том числе можно использовать метод, описанный выше, — но теперь для приготовления концентрированного раствора используется другое специально подобранное вещество. Так как концентрация растворённых веществ в полученном растворе ниже, чем в исходном, то дальнейшее его опреснение требует меньших затрат энергии (например, при использовании метода обратного осмоса). В результате использования данного метода часть дорогостоящей электрической энергии заменяется на дешёвую низкопотенциальную (порядка 100 °C) тепловую энергию (в частности, солнечную).
Пример 1
Берётся концентрированный раствор карбоната аммония, который находится по другую сторону полупроницаемой мембраны от солёной воды. Пресная вода проникает в раствор карбоната аммония, разбавляя его. Затем раствор карбоната аммония нагревается до температуры 60-80 °С, карбонат аммония разлагается и покидает раствор, — и в итоге получается почти дистиллированная вода. Её можно дополнительно опреснить или использовать без обработки в целях орошения. Карбонат аммония при этом регенерируется и используется многократно.