Построение кривых охлаждения сплавов
Компоненты, фазы и структуры в системе Fe- Fe3C
Компонентами сплавов являются железо и углерод. Оба полиморфные. Железо имеет две основные (всего 4) модификации: от температуры плавления 1539 до 911 °С – g с ячейкой ГЦК и ниже - a, имеющей ОЦК ячейку с периодом примерно в 1,3 раза меньшим. Поэтому поры (промежутки) в решетке ОЦК небольшие и меньше растворимость уг-лерода в ней. ГЦК решётка более компактна, поэтому при перестроении атомов Fea в Feg объём железа примерно на 1% уменьшается. Но рас-творимость углерода в решётке ГЦК больше, чем в ОЦК примерно в 100 раз (из-за большей поры в центре куба).
Углерод имеет две модификации: графит и алмаз. Графит стабилен, имеет слоистую гексагональную решётку со слабой молекулярной связью между слоями, поэтому он очень непрочен.
Углерод может растворяться в железе, образовывать с ним химическое
соединение – карбид Fe3C и, наконец, может находиться в высокоуглеродистых сплавах в свободном состоянии, в виде графита.
Фазы (однородные части сплава) в системе Fe-C
Жидкость – вещество с близкой межатомной связью, равномерно распределёнными компонентами, обладающее текучестью.
Аустенит – твёрдый раствор внедрения углерода и других элементов в g – железе с ограниченной растворимостью, достигающей 2,14% С. Условное обозначение: А или Feg (C).
Феррит – ограниченный твёрдый раствор внедрения углерода в a-железе: Ф или Fea (C).
| |
Графит – слоистая непрочная модификация углерода: Г.
| Структура | Тип соединения компонентов или фаз | Концентрация углерода, % | Число фаз | Примерные показатели механических свойств | Оценка по механическим свойствам | ||
| Gв, | d, % | НВ | |||||
| Сверхчистое железо | Химический элемент | (примесей<0,01) | Очень пластично, непрочно | ||||
| Феррит | Твёрдый раствор углерода в a-железе | до 0,006 (при 20 ºC), до 0,02 (при 727 ºC) | Пластичен, непрочен | ||||
| Аустенит | Твёрдый раствор углерода в g-железе | до 2,14 | Очень пластичен | ||||
| Цементит | Химическое соединение Fe3C | 6,67 | Очень твёрд и хрупок | ||||
| Перлит | Механи-ческая смесь Ф+Ц | 0,8 | Средне-прочен и плас- тичен | ||||
| Ледебурит | Механи-ческая смесь П + Ц | 4,3 | — | Твёрд и хрупок |
Из таблицы видно, что феррит – мягкая, пластичная фаза (НВ 80, d»40%, sв » 300 МПа). Аустенит более пластичен (d»60 %, НВ 180-200), но прочнее феррита из - за большей растворимости углерода и больших искажений решётки.
Цементит очень твёрд, выше 210 °С немагнитен, плавится при 1260 °С.
Пластичные железоуглеродистые сплавы содержат до 2,14% С — это стали, при большей концентрации углерода при наличии эвтектики сплавы хрупки, это — чугуны.
В железоуглеродистых сплавах из растворимых фаз при низких тем-пературах имеются: феррит, цементит и графит. Кроме того, в состав сплавов входят смеси: эвтектика и эвтектоид. Их рассмотрим, изучая превращения в сплавах.
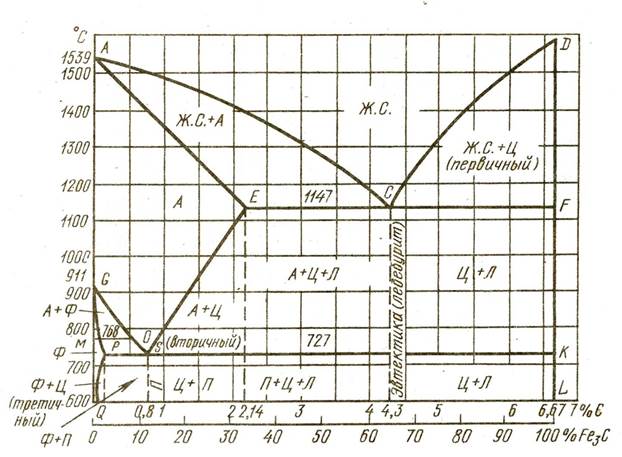
Диаграмма Fe – Fe3C
На диаграмме крайние ординаты соответствуют чистому железу (при С=0) и цементиту (при С=6,67, по другим источникам 6,69%). Первая ордината является и шкалой температур. Абсцисса – шкала концентраций по C и Fe3C.
Рассмотрим упрощённую диаграмму, детально верхний левый угол не рассматриваем.
Однофазные области содержат: 1. Жидкость (Ж);
2. Аустенит (А); 3. Феррит (Ф).
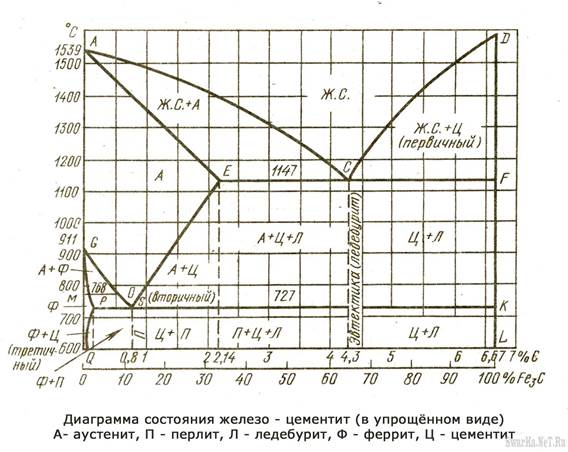 Остальные области и наклонённые линии – двухфазные. По три фазы имеются только на горизонталях ECF и PSK.
Остальные области и наклонённые линии – двухфазные. По три фазы имеются только на горизонталях ECF и PSK.
Линии:
ACD – ликвидус; AECF – солидус;
CD – первичного цементита, кристаллизующегося из жидкости;
ES – вторичного и PQ – третичного цементита, выделяющегося из аустенита и феррита, соответственно. Здесь и далее все процессы рассматриваются при охлаждении.
AC – линия начала кристаллизации аустенита;
AE – линия окончания кристаллизации аустенита;
GS – линия начала перекристаллизации аустенита в феррит; GP – линия окончания перекристаллизации (A ® Ф);
ECF – линия изотермического превращения жидкости, имеющей концентрацию точки C (4,3% C) в эвтектику Жс ® [Аe + Ц];
PSK – линия изотермического превращения аустенита, содержащего 0,8 % С, в эвтектоид («сплав, похожий на эвтектику») As ® [Фр + Ц].
PSK линия перлитного превращения, т.к. эвтектоид в системе Fe – C называют перлитом, а эвтектику – ледебуритом. Очень важная особенность строения этих смесей – мелкое зерно.
Построение кривых охлаждения сплавов
Кривые охлаждения можно построить с помощью правилафаз:
С=К+1,
где: С – число степеней свободы; К – число компонентов;
Ф – число фаз в сплаве.
Для двухкомпонентной системы С=3–Ф
Возможные значения С при числе фаз от 1 до 3:
С=0 – это означает, что фазы находятся в равновесии при T=Const, которая не может быть изменена до окончания процесса (уменьшения числа фаз). Итак, при С=0 – на кривой охлаждения будет горизонталь – температурная остановка.
С=1 – какая – то скорость охлаждения. С=2 – более высокая скорость охлаждения.
 Кривые охлаждения для варианта №7
Кривые охлаждения для варианта №7