Назначение цементации и режим термической обработки после цементации
Государственное образовательное учреждение
Пермский Государственный Технический Университет
Кафедра металловедения и термической обработки металлов.
Контрольная работа по материаловедению.
Вариант 48.
Работу выполнил:
Барсаев Н. М.
студент 2 курса
МТФ ТМКУ-07
Работу проверила:
Некрасова Т. В.
г. Пермь, 2009 г.
ВАРИАНТ 48
КОНТРОЛЬНАЯ РАБОТА 1
1. Чем объясняются высокие электро- и теплопроводность металлов?
Классическая электронная теория металлов представляет твердый проводник в виде системы, состоящей из узлов кристаллической ионной решетки, внутри которой находится электронный газ из коллективизированных (свободных) электронов. В свободное состояние от каждого атома металла переходит от одного до двух электронов. К электронному газу применялись представления и законы статистики обычных газов. При изучении хаотического (теплового) и направленного под действием силы электрического поля движения электронов был выведен закон Ома.
При столкновениях электронов с узлами кристаллической решетки энергия, накопленная при ускорении электронов в электрическом поле, передается металлической основе проводчика, вследствие чего он нагревается. Рассмотрение этого вопроса привело к выводу закона Джоуля—Ленца.
Таким образом, электронная теория металлов дала возможность аналитически описать и объяснить найденные ранее экспериментальным путем основные законы электропроводности и потерь электрической энергии в металлах.
Оказалось возможным также объяснить и связь между электропроводностью и теплопроводностью металлов. Кроме того, некоторые опыты подтвердили гипотезу об электронном газов металлах, а именно:
1. При длительном пропускании электрического тока через цепь, состоящую из одних металлических проводников, не наблюдается проникновения атомов одного металла в другой.
2. При нагреве металлов до высоких температур скорость теплового движения свободных электронов увеличивается, и наиболее быстрые из них могут вылетать из металла, преодолевая силы поверхностного потенциального барьера.
3. В момент неожиданной остановки быстро двигавшегося проводника происходит смещение электронного газа по закону инерции в направлении движения. Смещение электронов приводит к появлению разности потенциалов на концах заторможенного проводника, и стрелка подключаемого к ним измерительного прибора отклоняется по шкале.
4. Исследуя поведение металлических проводников в магнитном поле, установили, что вследствие искривления траектории электронов в металлической пластинке, помещенной в поперечное магнитное поле, появляется поперечная ЭДС и изменяется электрическое сопротивление проводника.
Однако выявились и противоречия некоторых выводов теории с опытными данными. Они состояли в расхождении температурной зависимости удельного сопротивления, наблюдаемой на опыте и вытекающей из положений теории; в несоответствии теоретически полученных значений теплоемкости металлов опытным данным. Наблюдаемая теплоемкость металлов меньше теоретической и такова, как будто электронный газ не поглощает теплоту при нагреве металлического проводника.
Эти противоречия удалось преодолеть, рассматривая некоторые положения с позиций квантовой механики.
В отличие от классической электронной теории в квантовой механике принимается, что электронный газ в металлах при обычных температурах находится в состоянии вырождения. В этом состоянии энергия электронного газа почти не зависит от температуры, т. е. тепловое движение почти не изменяет энергию электронов. Поэтому на нагрев электронного газа теплота не затрачивается, что и обнаруживается при измерении теплоемкости металлов.
В состояние, аналогичное обычным газам, электронный газ приходит при температуре порядка тысяч Кельвинов.
Представляя металл как систему, в которой положительные ионы скрепляются посредством свободно движущихся электронов, легко понять природу всех основных свойств металлов: пластичности, ковкости, хорошей теплопроводности и высокой электропроводности.
2. Детали из меди, штампованные в холодном состоянии, имели низкую пластичность. Объясните причину этого явления и укажите, каким способом можно восстановить пластичность? Назначьте режим обработки и приведите характер изменения структуры и свойств.
Ручная ковка была исторически первым из применяемых до сих пор способов формоизменяющей обработки металлов. Первый паровой молот, появившийся в 1843, деформировал металл силой падения груза, а пар служил для поднятия последнего. Вслед за таким молотом простого действия в 1888 появился молот двойного действия, верхняя «баба» которого при движении вниз дополнительно разгоняется силой пара.
Ковка и объемное штампование могут выполняться на молоте или на прессе. Ковка бывает свободная и в штампах. Штампы объемного штампования молотовые и для горячештамповочных прессов состоят из верхней (закрепляемой на верхней головке молота или пресса) и нижней частей, на соприкасающихся поверхностях которых имеются ручьи для последовательного формообразования изделий. Штампы для листового штампования (вырубные, пробивные, гибочные и др.) состоят из двух основных деталей – матрицы и входящего в нее пуансона, а иногда одна и та же часть штампа служит и пуансоном, и матрицей.
3. Вычертите диаграмму состояния железо-цементит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 2,7 % углерода. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
Обычно на диаграмме фазового равновесия системы железо-углерод наносят одновременно систему железо-карбид железа (Fe-Fe3C) – сплошные линии диаграммы – метастабильное равновесие и пунктирные линии – стабильное равновесие Fe-C. В настоящем домашнем задании мы рассматриваем только упрощенную (без перитектического превращения) диаграмму фазового равновесия железо-цементит.
В сплавах системы Fe-Fe3C встречаются следующие фазы: жидкий раствор, твердые растворы на основе различных кристаллических модификаций железа, химическое соединение Fe3C (цементит). На рис.1 представлена диаграмма состояния железо-цементит в фазовом виде.

Рис.1. Фазовая диаграмма состояния железо-цементит
В системе железо-цементит (Fe - Fе3С) имеются следующие фазы: жидкий раствор, твердые растворы - феррит и аустенит, а также химическое соединение - цементит.
Феррит может иметь две модификации - высоко- и низкотемпературную. Высокотемпературная модификация d-Fe и низкотемпературная - a-Fe представляют собой твердые растворы углерода, соответственно, в d- и a- железе.
Аустенит g-Fe - твердый раствор углерода в g-железе. Предельная растворимость углерода в g-железе 2,14%. Он устойчив только при высоких температурах, а с некоторым примесями (Мn, Сг и др.) при обычных (даже низких) температурах. Аустенит обладает высокой пластичностью, низкими пределами текучести и прочности. Твердость аустенита 160...200 НВ.
Цементит Fе3С - химическое соединение железа с углеродом, содержащее 6,67% углерода. Между атомами железа и углерода в цементите действуют металлическая и ковалентная связи. Температура плавления ~1250°С. Цементит является метастабильной фазой; область его гомогенности очень узкая и на диаграмме состояния он изображается вертикалью. Время его устойчивости уменьшается с повышением температуры: при низких температурах он существует бесконечно долго, а при температурах, превышающих 950°С, за несколько часов распадается на железо и графит. Цементит имеет точку Кюри (210°С) и обладает сравнительно высокими твердостью (800 НВ и выше) и хрупкостью. Прочность его i растяжение очень мала (s =40 МПа).
В системе железо - цементит имеются две тонкие механические смеси фаз - эвтектическая (ледебурит) и эвтектоидная (перлит).
Ледебурит является смесью двух фаз g-Fe + Fе3С, образующихся при 1130°С в сплавах, содержащих от 2,0 до 6,67%С, и наблюдается визуально как структурная составляющая железоуглеродистых сплавов, главным образом, чугунов. Ледебурит обладает достаточно высокими прочностью (НВ>600) и хрупкостью.
Перлит (до 2,0%С) представляет собой смесь a-Fe + Fе3С (в легированных сталях -карбидов), образующуюся при 723°С и содержании углерода 0,83% в процессе распада аустенита, и наблюдается визуально как структурная составляющая железоуглеродистых сплавов. Механические свойства перлита зависят от формы и дисперсности частичек цементита (прочность пластинчатого перлита несколько выше, чем зернистого): s=800...900 МПа; d< 16%; НВ 180..,220.
В зависимости от содержания углерода (%) железоуглеродистые сплавы получили следующие названия:
• менее 0,83 - доэвтектоидные стали;
• 0,83 - эвтектоидные стали;
• 0,83...2 - заэвтектоидные стали;
• 2...4,3 - доэвтектические чугуны;
• 4,3...6,67 - заэвтектические чугуны.
Таким образом, сплав, содержащий 2,7 % углерода – это доэвтектический чугун.
4. Вычертите диаграмму изотермического превращения аустенита для эвтектоидной стали, нанесите на нее кривую режима изотермической обработки с выдержкой при температуре 600 оС. Укажите, как этот режим называется, опишите сущность превращений и как такой сплав называется.
На рис. 2 показан верхний участок упрощенной диаграммы Fe-Fe3C.
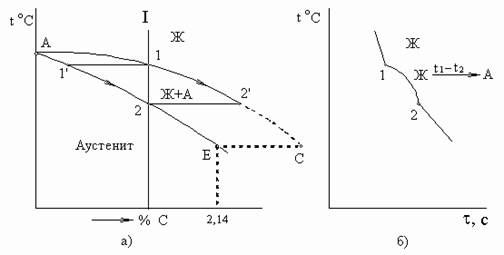
Рис. 2. Верхний левый участок упрощенной диаграммы состояния железо-цементит.
а) Первичная кристаллизация сплавов до 2,14 %С (сталей); б) кривая охлаждения сплава 1
В сталях из жидкой фазы кристаллизуется аустенит. Состав жидкой фазы меняется по проекции линии АС на ось концентраций, твердой фазы по проекции линии АЕ.
Превращения в твердом состоянии. Окончательное формирование структуры стали происходит в результате превращений аустенита при дальнейшем охлаждении. Основой этого превращения является полиморфизм, связанный с перегруппировкой атомов из ГЦК решетки аустенита в ОЦК решетку феррита, а также изменение растворимости углерода по линии ES в аустените и PQ в феррите. В сплавах с содержанием от 0,025 до 2,14 %С вторичные превращения начинаются при температурах, соответствующих линиям GS и SE и заканчиваются при температуре ниже 727 оС и линии PSK, в результате эвтектоидной реакции.
5. Определите металлургическое качество, назначение, а также среднее содержание углерода и легирующих элементов в сталях: 20ХН3А, сталь 20, У9, 5ХВ2С.
1) Сталь 20Х3А (Гост 4543-71) имеет плотность 7850 кг/м.куб.
Назначение: шестерни, валы, втулки, силовые шпильки, болты, червяки, муфты и другие цементируемые детали, к которым предъявляются требования высокой прочности, пластичности и вязкости сердцевины и высокой поверхностной твердости, работающие под действием ударных нагрузок и при отрицательных температурах.
Химический состав: Кремний:0.17-0.37, Марганец:0.30-0.60, Медь:0.30, Никель:2.75-3.15, Сера:0.025, Углерод:0.17-0.24, Фосфор:0.025, Хром:0.60-0.90.
2) Сталь У9 (ГОСТ 1435-99). Плотность7745 кг/м.куб.
Назначение: инструмент-слесарный, монтажный, калибры. Не применяется для сварных конструкций.
Химический состав: Кремний:0.17-0.33, Марганец:0.17-0.33, Медь:0.25, Никель:0.25, Сера:0.028, Углерод:0.86-0.93, Фосфор:0.030, Хром:0.20.
4) Сталь 20 (ГОСТ 1050-88) имеет плотность7859 кг/м.куб.
Назначение этой стали: панели, основания, платы, кронштейны, угольники, ребра жесткости, а также детали после цементации и термообработки, работающие на трение, для изготовления деталей, обрабат. резанием, сваркой, холодной высадкой и в виде поковок и штамповок.
Сваривается без ограничений, кроме деталей после химико-термической обработки. Способы сварки РДС, АДС под флюсом и газовой защитой, КТС.
Химический состав: Кремний:0.17-0.37, Марганец:0.35-0.65, Медь:0.25, Никель:0.25, Сера:0.04, Углерод:0.17-0.24, Фосфор:0.035, Хром:0.25, Мышьяк:0.08.
4) Сталь 5ХВ2С. Плотность7800 кг/м.куб.
Назначение: ножи при холодной резке металла, резьбонакатные плашки, пуансоны и обжимные матрицы при холодной работе, штампы сложной формы, работающие с повышенными ударными нагрузками.
Химический состав: C 0.45 - 0.55; Si 0.8 - 1.1; Mn 0.15 - 0.45; Ni до 0.35; S до 0.03; P до 0.03;Cr 0.9 - 1.2; Mo до 0.3;W 1.8 - 2.3; V до 0.3; Cu до 0.3
КОНТРОЛЬНАЯ РАБОТА 2
Назначение цементации и режим термической обработки после цементации.
Цементация – химико-термическая обработка, заключающаяся в диффузионном насыщении поверхностного слоя атомами углерода при нагреве до температуры 900…950 oС.
Цементации подвергают стали с низким содержанием углерода (до 0,25 %).
Нагрев изделий осуществляют в среде, легко отдающей углерод. Подобрав режимы обработки, поверхностный слой насыщают углеродом до требуемой глубины.
Глубина цементации (h) – расстояние от поверхности изделия до середины зоны, где в структуре имеются одинаковые объемы феррита и перлита ( h. = 1…2 мм).
Степень цементации – среднее содержание углерода в поверхностном слое (обычно, не более 1,2 %).
Более высокое содержание углерода приводит к образованию значительных количеств цементита вторичного, сообщающего слою повышенную хрупкость.
На практике применяют цементацию в твердом и газовом карбюризаторе (науглероживающей среде).
Участки деталей, которые не подвергаются цементации, предварительно покрываются медью (электролитическим способом) или глиняной смесью.
Цементация в твердом карбюризаторе
Почти готовые изделия, с припуском под шлифование, укладывают в металлические ящики и пересыпают твердым карбюризатором. Используется древесный уголь с добавками углекислых солей ВаСО3, Na2CO3 в количестве 10…40 %. Закрытые ящики укладывают в печь и выдерживают при температуре 930…950 oС.
За счет кислорода воздуха происходит неполное сгорание угля с образованием окиси углерода (СО), которая разлагается с образованием атомарного углерода. Образующиеся атомы углерода адсорбируются поверхностью изделий и диффундируют вглубь металла.
Недостатками данного способа являются:
· значительные затраты времени (для цементации на глубину 0,1 мм затрачивается 1 час);
· низкая производительность процесса;
· громоздкое оборудование;
· сложность автоматизации процесса.
Способ применяется в мелкосерийном производстве.
Газовая цементация
Процесс осуществляется в печах с герметической камерой, наполненной газовым карбюризатором.
Атмосфера углеродосодержащих газов включает азот, водород, водяные пары, которые образуют газ-носитель, а также окись углерода, метан и другие углеводороды, которые являются активными газами.
Глубина цементации определяется температурой нагрева и временем выдержки.
Преимущества способа:
· возможность получения заданной концентрации углерода в слое (можно регулировать содержание углерода, изменяя соотношение составляющих атмосферу газов);
· сокращение длительности процесса за счет упрощения последующей термической обработки;
· возможность полной механизации и автоматизации процесса.
Способ применяется в серийном и массовом производстве.
На поверхности изделия образуется слой заэвтектоидной стали, состоящий из перлита и цементита. По мере удаления от поверхности, содержание углерода снижается и следующая зона состоит только из перлита. Затем появляются зерна феррита, их количество, по мере удаления от поверхности увеличивается. И, наконец, структура становится отвечающей исходному составу.
Термическая обработка после цементации
В результате цементации достигается только выгодное распределение углерода по сечению. Окончательно формирует свойства цементованной детали последующая термообработка. Все изделия подвергают закалке с низким отпуском. После закалки цементованное изделие приобретает высокую твердость и износостойкость, повышается предел контактной выносливости и предел выносливости при изгибе, при сохранении вязкой сердцевины.
Комплекс термической обработки зависит от материала и назначения изделия.
Если сталь наследственно мелкозернистая или изделия неответственного назначения, то проводят однократную закалку с температуры 820…850oС. При этом обеспечивается получение высокоуглеродистого мартенсита в цементованном слое, а также частичная перекристаллизация и измельчение зерна сердцевины.
При газовой цементации изделия по окончании процесса подстуживают до этих температур, а затем проводят закалку (не требуется повторный нагрев под закалку).
Для удовлетворения особо высоких требований, предъявляемых к механическим свойствам цементованных деталей, применяют двойную закалку.
Первая закалка (или нормализация) проводится с температуры 880…900oС для исправления структуры сердцевины.
Вторая закалка проводится с температуры 760…780oС для получения мелкоигольчатого мартенсита в поверхностном слое.
Завершающей операцией термической обработки всегда является низкий отпуск, проводимый при температуре 150…180oС. В результате отпуска в поверхностном слое получают структуру мартенсита отпуска, частично снимаются напряжения.
Цементации подвергают зубчатые колеса, поршневые кольца, червяки, оси, ролики.