Мембрана является амфипатической структурой.
Мембраны. Виды трансмембранного транспорта. Роль холестерола в жидкостности мембран. Введение в обмен веществ. Биохимия питания и пищеварения.
Функции мембран
1. Отделяют клетки от окружающей среды. Обладают избирательной проницаемостью, содержат специфические транспортные системы. Внутренние мембраны клеток ограничивают органеллы и формируют обособленные внутриклеточные отсеки - компартменты. Они обеспечивают функциональную специализацию клетки.
2. Мембраны играют центральную роль в системе межклеточных взаимодействий. В них располагаются рецепторы, воспринимающие химические, физические и другие внешние сигналы. Некоторые мембраны сами способны генерировать сигнал (химический или электрический).
3. Мембраны участвуют в процессах превращения энергии (фотосинтез, окислительное фосфорилирование).
Структура мембран
Характеристика мембран.Все биологические мембраны имеют общие признаки строения.
1. Мембраны являются сложными структурами, построенными из липидов, белков и углеводов. Основу мембран составляет липидный бислой, имеющий толщину 6-10 нм.
2. Соотношение белков и липидов в мембранах варьирует от 1:4 до 4:1 и зависит от типа клеток и органелл.
3. Мембраны являются асимметричной структурой с наружной и внутренней поверхностями.
4. Мембрана стабилизируется нековалентными связями и является термодинамически стабильной и метаболически активной.
5. Специфические белки встроены в мембраны и выполняют специфические функции рецепции управляющих сигналов, межклеточного взаимодействия, транспорта веществ и пр.
6. Мембраны – это жидкостные структуры.
7. Большинство мембран способны к поляризации (для внутренней поверхности мембран типично 60 мВ). Мембраны играют ключевую роль в транспорте, преобразовании энергии и хранении энергии.
Липиды мембран.Основными липидами мембран являются фосфолипиды, гликолипиды и холестерол.
1. В мембранах присутствуют 2 основных класса фосфолипидов:
1.1. Глицерофосфоглицериды являются основным компонентом большинства мембран и состоят из спирта глицерола, 2-х остатков жирных кислот, остатка фосфорной кислоты и спирта: холина (фосфатидилхолин), этаноламина (фосфатидилэтаноламин), серина (фосфатидилсерин), глицерола (фосфатидилглицерол), глицеролфосфата, треонина или инозитола (рис. 1, таблица 1).
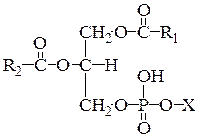
Рис. 1. Строение глицерофосфолипидов. Х – спирт.
Таблица 1.
Структура глицерофосфолипидов
| Глицерофосфолипид | Спирт |
| Фосфатидилэтаноламин | НО–СН2–СН2-NH2 |
| Фосфатидилхолин | НО–СН2–СН2–N+(СH3)3 |
| Фосфатидилсерин | НО–СН2–СHNН2–СООН |
| Фосфатилилинозитол | 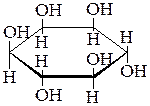
|
| Фосфатидилглицерол | 
|
Жирные кислоты содержат четное число атомов углерода (чаще 16 и 18). Жирные кислоты неразветвленные и могут быть насыщенными (чаще в 1 положении глицерофосфолипида) и ненасыщенными (чаще во 2 положении глицерофосфолипида).
Жирные кислоты – это углеводородные цепи различной длины и степени насыщенности, заканчивающиеся карбоксильной группой. Системное наименование происходит от родительского углеводорода с окончанием –овая. Например, С18 насыщенная жирная кислота называется октадекановая кислота, поскольку родительский углеводород – октадекан. С18 ненасыщенная жирная кислота с одной двойной связью называется октадеценоевая кислота, с двумя двойными связями – октадекадиеновая кислота, а с тремя двойными связями – октадекатриеновая кислота. Запись 18:0 означает С18 жирную кислоту без двойных связей; запись 18:2 означает, в жирной кислоте есть две двойные связи. Нумерация углеродных атомов начинается от карбоксильной группы. По другой классификации углеродные атомы 2 и 3 обозначают как α и β углеродные атомы, соответственно. Наиболее отдаленный от карбоксильной группы концевой атом углерода называют ω-углеродный атом. Положение двойной связи обозначают символом Δ. Например, цис-Δ9 означает наличие двойной связи между 9 и 10 углеродными атомами.
Жирные кислоты ионизированы при физиологическом значении рН, поэтому они получают суффикс –ат, например, пальмитат, олеат.
1.2. Сфингомиелины содержат спирт сфингозин. Жирная кислота присоединяется амидной связью к аминогруппе сфингозина. Первичная гидроксильная группа сфингозина эстерифицируется фосфорилхолином. Сфингомиелины находятся преимущественно в миелиновых оболочках.

1.3. Гликолипиды являются сахаросодержащими липидами и делятся на ганглиозиды и цереброзиды. Цереброзиды вместо фосфорилированного спирта содержат остаток гексозы (глюкозу или галактозу). Ганглиозиды содержат цепь из 3 и более остатков углеводов (например, сиаловые кислоты), которые присоединяются к первичной спиртовой группе сфингозина.
1.4. Стероиды. Основным стероидом в мембранах является холестерол (рисунок 2), который находится преимущественно в плазматической мембране клеток.

Рис.2. Холестерол
Холестерол в основном встречается в наружном слое плазматической мембраны. Молекула холестерола встраивается в фосфолипидный бислой, причем гидроксильная группа в положении 3 образует водородные связи с полярными головками фосфолипидов, а сочлененные кольца палочкообразной формы располагаются в гидрофобной зоне ацильных остатков фосфолипидов бислоя.
Мембрана является амфипатической структурой.
1.Все молекулы липидов, входящих в состав мембран, имеют гидрофильную и гидрофобную области и поэтому являются амфипатическими.
2.Амфипатические липиды мембран имеют полярную головку и неполярные гидрофобные хвосты (рисунок 3). Полярные головки нейтральны или имеют отрицательный заряд.

Рис. 3. Структура липидов мембран
3.Насыщенные жирные кислоты имеют прямые хвосты, ненасыщенные жирные кислоты имеют цис-конформацию и изогнутые хвосты, что делает мембрану менее жесткой и более текучей.
4. Липиды формируют бислой, в котором гидрофобная область фосфолипидов защищена от воды, а гидрофильная область обращена к воде (рисунок 7.5). Липидный бислой получают in vitro в виде липосом.
Белки мембран
По расположению белков в мембране, способу их ассоциации с липидным бислоем их можно разделить на: поверхностные (периферические) мембранные белки, связанные с гидрофильной поверхностью липидного бислоя; интегральные мембранные белки, погруженные в гидрофобную область бислоя.
Прошивающие мембрану белки имеют конформацию α-спирали во внутренней части мембраны. В этой части белка преобладают гидрофобные аминокислотные остатки. Такая структура была впервые установлена при исследовании бактериородопсина (7 тесно упакованных α-спиралей, пересекающих мембрану размером 4,4 нм).
Поры или каналы в мембранах образуются β-структурами белков. Антипараллельные β-структуры связаны водородными связями и извиваясь формируют полый цилиндр, который выполняет функции поры. Важно, что остатки гидрофобных аминокислот взаимодействуют с гидрофобными группами внутримембранного окружения канала, а внутренняя поверхность канала образуется радикалами гидрофильных аминокислот.
Если основные структурные особенности биологических мембран определяются свойствами их липидного бислоя, то специфические функции мембран – белками.
1. Мембранные белки можно разделить на две группы: структурныеидинамические белки. Структурные белки поддерживают структуру всей мембраны. Это, как правило, периферические белки, выступающие в роли «молекулярного бандажа». Динамические белки непосредственно участвуют в процессах, происходящих на мембране. Выделяют три класса таких белков:
1) транспортные – участвующие в трансмембранном переносе веществ;
2) каталитические – это ферменты, интегрированные в мембрану и катализирующие происходящие там реакции;
3) рецепторные – это мембранные рецепторы, специфически связывающие такие соединения, как гормоны, нейромедиаторы, токсины, на наружной стороне мембраны, что служит сигналом для изменения метаболических процессов в мембране или внутри клетки.
Углеводы мембран.В составе мембран углеводы находятся только в соединении с белками (гликопротеины и протеогликаны) и липидами (гликолипиды). В мембране гликозилировано около 10% всех белков и 5-25% липидов. Углеводные цепи белков колеблются по составу от 2-х членных структур до разветвленных 18-членных полисахаридов.
Функции углеводов:
1) определяют межклеточное взаимодействие;
2) участвуют в системе иммунитета (антигенные детерминанты групп крови);
3) входят в состав рецепторов.
Модели строения мембран
С.Дж.Сингер и Л.Г.Никольсон в 1972 г. предложили «жидкостно-мозаичную модель» строения мембраны. Согласно этой модели мембрана представляет собой липидный бислой, в котором расположены глобулярные белки. Каждая молекула липидов расположена так, что ее неполярная углеводородная часть направлена внутрь бислоя, а полярные головки находятся на поверхности, контактируя с водой. По этой модели, мембрана представляет собой динамическую систему, в которой молекулы белка относительно свободно «плавают в липидном море в виде айсбергов». Прямые измерения показали, что белки движутся в сотни раз медленнее из-за переплетения углеводных цепей на поверхности мембраны (гликокаликс). Кроме того компоненты мембраны с внутренней стороны связаны с системой белков цитокаркаса.
Существует решетчато-мозаичная модель. Молекулы белков, которые связаны с цитокаркасом, малоподвижны. Те белки, которые с цитокаркасом не связаны, могут относительно свободно перемещаться в плоскости мембраны.