Тақырыбы: Газ тәрізді заттардың молекулалық массасын анықтау.
Жұмыстың мақсаты:Көміртегі (IV) оксидін алу және оның молекулалық массасын тәжірибе жүзінде анықтау.
Жалпы мағлұматтар:Газ тәрізді заттардың молекулалық салмағын анықтау үшін оның берілген температура және қысымда көлемін білу қажет.
Авагадро заңы бойынша кез келген газдың тең көлемінде молекула саны бірдей болатынын ескерсек:
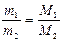
бұдан 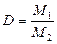 . Мұндағы М1 және М2 газдардың молекулалық массалары.
. Мұндағы М1 және М2 газдардың молекулалық массалары.
Газдардың салыстырмалы тығыздығы (  ) бір газдың екінші газдан қанша ауыр не жеңіл екендігін көрсетеді. Бұл формула арқылы газдардың молекулалық массасын анықтауға болады.
) бір газдың екінші газдан қанша ауыр не жеңіл екендігін көрсетеді. Бұл формула арқылы газдардың молекулалық массасын анықтауға болады.

Әдетте газдардың салыстырмалы тығыздығын сутегі арқылы анықтайды. Бұл кезде екінші газдың молекулалық массасы  болады. Егер салыстырмалы тығыздық ауа арқылы табылса,
болады. Егер салыстырмалы тығыздық ауа арқылы табылса,  болады. Мұнда 29 ауаның орташа молекулалық массасы. Сонымен қатар Менделеев-Клапейрон формуласы бойынша есептеуге болады.
болады. Мұнда 29 ауаның орташа молекулалық массасы. Сонымен қатар Менделеев-Клапейрон формуласы бойынша есептеуге болады.

мұндағы р – газдың қысымы, V – көлем, m – масса, М – молекулалық масса, R – универсаль газ тұрақтысы, Т – абсолютті температура.
Құрал-жабдықтар, реактивтер:
1. Техникалық таразы; 1000 мл цилиндр; Кипп аппараты;
2. Тығыны бар 500-1000 мл колба; Барометр, қарындаш; Мрамор, тұз қышқылы.
Жұмыстың жасалу реті:
Құрғақ әрі таза колбаны тығыздап каучукті тығынмен жабыңдар. Тығынның пробирка мойнындағы төменгі деңгейін шыныға жазатын карандашпен белгілеп алып, техникалық таразыда 0,02 г-ға дейінгі дәлдікпен өлшеңіз. Тығынды ашып, колбаның түбіне дейін Кипп приборының газ шығарушы түтікшесін салып, 3-5 мин уақыт аралығында СО2 жіберіңіз. Белгіге дейін колбаны тығындап, таразыға СО2 бар колбаны өлшеңіз. Өлшенген өлшемдер бірдей болғанша өлшеу қайталана береді. Бұл жағдайда, колбаның ішіндегі ауаның толық ығысып шығып, оны орнының толығымен СО2 толтырылғанына сенімді болу керек. СО2 көлемін (V) өлшеу үшін, колбаны белгісіне дейін сумен толтырып, су мөлшерін өлшеу цилиндрмен өлшеңдер. Тәжірибе барысындағы термометр мен барометр көрсеткішін жазып алыңыз.
Тәжірибе нәтижелері мен есептеулер:
1. Тығындалған ауасы бар колбаның массасы (m1), г.
2. Тығындалған СО2 бар колбаның массасы (m2), г.
3. Колба көлемі (V), л.
4. Абсолюттік температура (Т0=273К).
5. Бөлме температурасы, 0С.
6. Қ.ж. колба ішіндегі газдың көлемі (V0), л.  формуласымен есептеледі.
формуласымен есептеледі.
7. Колба көлеміндегі ауаның массасы (қ.ж. 1л ауаның массасы 1,239 г деп алыңыз) (m3), г. m3=1,293∙ V0.
8. Атмосфералық қысым (Р), кПа. 1 атм. = 760мм.с.б.
9. Ауасыз колбаның массасы (m4), г. m4 = m1 – m3.
10. Көміртегі оксидінің (IV) массасы (m5 = m2 – m4), г.
11. СО2 ауамен салыстырғандағы тығыздығы,  .
.
12. СО2 молекулалық массасын мына формулалар бойынша есептеңіз:
 ;
;  (мұндағы р=1 атм., R=0,082
(мұндағы р=1 атм., R=0,082  );
); 
Тапсырма:
1. Көміртегі (IV) оксидінің ауа және сутегімен салыстырғандағы тығыздығын есептеңіз.
2. Жоғарыда көрсетілген теңдеу бойынша молекулалық масса және тәжірибенің салыстырмалы қателігін есептеңіз.
Зертханалық жұмысқа әдістемелік нұсқаулар:
1. Бірімжанов Б, Нұрахметов Н. Жалпы химия. Алматы «Ана тілі», 1992ж.
2. Ахметов Н.С. Общая и неорганическая химия. М. «Высшая школа», 2001г.
3. Практикум по неорганической химии под ред. Воробьева А.Ф., Дракина С.Н. М., Химия, 1987.
Жұмыста қолданатын негізгі схемалар мен формулалар:
Кипп аппаратының сызбанұсқасы. Тищенко шынысы, Менделеев-Клапейрон теңдеуі.
Бақылау сұрақтары:
1. Салыстырмалы тығыздық дегеніміз не?
2. Газдың көлемін Менделеев-Клапейрон теңдеуі бойынша есептеңіз.
3. Көміртегі оксидінің ауа және сутегімен салыстырғандағы салыстырмалы тығыздығын есептеңіз.