Взаємодія розведеної сульфатної кислоти з солями більш слабких кислот 1 страница
ЖУРНАЛ ЗВІТІВ
ЛАБОРАТОРНИХ РОБІТ
З ПРЕДМЕТУ «ХІМІЯ»
Розробив студент 1____ групи
| ||||
| (Прізвище, ім’я ) Перевірив викладач _________________________ |
Херсон 2016
ПРАВИЛА ТЕХНІКИ БЕЗПЕКИ
при виконанні
лабораторних робіт з хімії
1. Заходити та знаходитися в кабінеті хімії можна тільки з дозволу
викладача та під його наглядом.
2. Виконувати тільки ті хімічні досліди та у такій послідовності, яка
відповідає плану даної роботи та погоджено з викладачем.
3. Не куштувати речовини на смак.
4. Наливати та насипати реактиви над столом.
5. Реактиви для дослідів брати тільки в тих кількостях, які зазначені в
інструкції або вказані викладачем.
6. Нюхати всі речовини з обережністю, не нахилятися над посудиною, а
спрямовувати до себе пару чи газ рухами руки.
7. При нагріванні розчинів у пробірці користуватися дерев'яним тримачем. Уважно стежити за тим, щоб отвір пробірки був спрямований убік від оточуючих, бо рідина внаслідок перегріванняможе викинутися з пробірки.
8. При нагріванні рідин стежити, щоб не перегрівалися стінки посудини
над рідиною (особливо, коли її мало), бо при попаданні на перегріте
скло крапель рідини посудина може тріснути.
9. Якщо реактив потрапив в очі, на шкіру або одяг, негайно сповістити
викладача, ретельно змити реактив водою, а потім нейтралізуючою
речовиною (кислоту - слабким розчином питної соди, а луг - слабким
розчином борної кислоти).
10. Відпрацьовані реактиви після їх нейтралізації зливати у спеціальний
посуд.
11. Після закінчення роботи прибрати своє робоче місце, відключити
електронагрівальні прилади й обов'язково ретельно вимити руки.
З правилами техніки безпеки ознайомлений ___________________
| ЛАБОРАТОРНА РОБОТА № 1 ТЕМА: ХІМІЧНІ ВЛАСТИВОСТІ СУЛЬФАТНОЇ КИСЛОТИ. ВИЯВЛЕННЯ СУЛЬФАТ-ЙОНУ МЕТА:дослідити хімічні властивості розведеної сульфатної кислоти; навчитися проводити якісну реакцію на сульфат-йон Література: 1.Буринська Н.М., Величко Л.П. Хімія —10,11 класи —К.: Перун, 2001. —198 . 2. Бабич Л.В., Балезин С.А. Практикум по неорганической химии— М.: Просвещение, 1991.—320. Реактиви: розчини: сульфатна кислота (1:5), натрій карбонат, барій хлорид, натрій гідроксид. тверді речовини: гранули цинку, магнію, заліза, міді. індикатори: фенолфталеїн, універсальний індикаторний папір. Обладнання: пробірки (10), штатив для пробірок, нагрівальне обладнання, сірники. | |||
| № | Назва досліду та рівняння реакцій | Спостереження | Висновки |
Взаємодія розведеної сульфатної кислоти з металами
В 4 пробірки покласти гранули маг-нію, цинку, заліза та міді.
Додати до кожної по 0,5 мл розве-деної сульфатної кислоти. Газ, що виділився, перевірити на чистоту.
1)
| 2) |
| 3) |
| 4) |
| 5) |
Реакція нейтралізації
Налити в пробірку 0,5 мл натрій
гідроксиду та додати 1 краплину фенолфталеїну. По краплинах додавати розчин сульфатної кислоти до утворення нейт-рального середовища.
1)
| 2) | |
|
Взаємодія розведеної сульфатної кислоти з солями більш слабких кислот В пробірку налити 1 мл сульфатної кислоти та додати до неї 1 мл на-сиченого розчину натрій карбонату. 1)
| ||||||||||||||||||||||||||||||||||||||
| Якісна реакція на сульфат-йон До розчинів сульфатної кислоти, натрій сульфату об’ємом 0,5 мл додати розчин барій хлориду. | ||||||||||||||||||||||||||||||||||||||
| Висновок: | ||||||||||||||||||||||||||||||||||||||
ПИТАННЯ ДЛЯ САМОКОНТРОЛЮ:
| ||||||||||||||||||||||||||||||||||||||
| ХХХХХ | арк | |||||||||||||||||||||||||||||||||||||
| зм | лист арк | № док | підп | дата | ||||||||||||||||||||||||||||||||||
| ЛАБОРАТОРНА РОБОТА № 2 ТЕМА: ДОБУВАННЯ АМОНІАКУ. ВИВЧЕННЯ ЙОГО ВЛАСТИВОСТЕЙ. СОЛІ АМОНІЮ МЕТА:дослідити властивості водного розчину амоніаку та солей амонію, навчитись проводити якісну реакцію на йон амонію. Література: 1.Буринська Н.М., Величко Л.П. Хімія —10,11 класи —К.: Перун, 2001. —198с. 2.Бабич Л.В., Балезин С.А. Практикум по неорганической химии— М.: Просвещение,1991.—320 с. Реактиви: розчини: амоній сульфат, натрій гідроксид, хлоридна кислота (ρ=1,18г/мл), барій хлорид тверді речовини: амоній хлорид, кальцій гідроксид індикатори: фенолфталеїн, універсальний індикаторний папір Обладнання: пробірки (4), штатив для пробірок, нагрівальне обладнання, сірники, скляна паличка, хімічний стакан, корк з газовідвідною трубкою, ступка. | |||||||||||
| № | Назва досліду та рівняння реакцій | Спостереження | Висновки | ||||||||
Добування амоніаку та
дослідження його властивостей
У пробірку насипати на 1/3 об’єму ретельно розтертих амоній хлориду та кальцій гідроксиду, закрити корком з газовідвідною трубкою та нагрівати. Газ, що виділяється, збирати в іншу пробірку 2-3 хв. Пробірку закрити корком. Розчинити газ у воді. Дослідити забарвлення індикаторів у розчині амоніачної води.
| |||||||||||
| 2 | Взаємодія амоніаку з кислотами
Дві скляні палички змочити розчинами хлоридної кислоти та водним розчином амоніаку. З’єднати.
| ||||||||||
Якісна реакція на йон амонію
У пробірку налити 0,5 мл амоній
сульфату, додати 1 мл натрій гідрок-сиду та нагріти. До отвору пробірки піднести вологий індикаторний папір.
| |||||||||||
| Лабораторна робота № 2 | |||||||||||
| зм | арк | № докум. | підп. | дата | |||||||
| розроб. | Добування амоніаку, вивчення його властивостей | літ | арк | арк | |||||||
| перевір. | Литвиненко | н | |||||||||
| ________________ | |||||||||||
| н. конт. | |||||||||||
| затверд | |||||||||||
| 4* | Визначити за допомогою якісних
реакцій розчин амоніачної води, калій сульфату та натрій гідроксиду.
|
| пробірка № 1— пробірка № 2 — пробірка № 3 — | |||||||||||||||||||||||||||||||||
| Висновок: | ||||||||||||||||||||||||||||||||||||
ПИТАННЯ ДЛЯ САМОКОНТРОЛЮ:
| ||||||||||||||||||||||||||||||||||||
| ХХХХХ• | арк | |||||||||||||||||||||||||||||||||||
| вим | лист арк. | № док | підп | дата | ||||||||||||||||||||||||||||||||
| ЛАБОРАТОРНА РОБОТА № 3 ТЕМА: ДОБУВАННЯ КАРБОН(ІV) ОКСИДУ І ВИВЧЕННЯ ЙОГО ВЛАСТИВОСТЕЙ. ВЗАЄМОПЕРЕТВОРЕННЯ КАРБОНАТІВ ТА ГІДРОГЕНКАРБОНАТІВ МЕТА:навчитися добувати вуглекислий газ в лабораторії, дослідити умови взаємоперетворення карбонатів і гідрогенкарбонатів; навчитись проводити якісну реакцію на карбонат-йон. Література: 1.Буринська Н.М., Величко Л.П. Хімія —10,11 класи —К.: Перун, 2001. —198 . 2.Бабич Л.В., Балезин С.А. Практикум по неорганической химии— М.: Просвещение,1991.—320. Реактиви: розчини: хлоридна кислота, натрій карбонат, сульфатна кислота, вапняна вода, амоніачна вода, барій хлорид. тверді речовини: кальцій карбонат, натрій гідрогенкарбонат. індикатори: універсальний індикаторний папір. Обладнання: пробірки (11), штатив для пробірок, нагрівальне обладнання, сірники, корк з газовід водною трубкою, пробіркотримач. | ||||||||||||
| № | Назва досліду та рівняння реакцій | Спостереження | Висновки | |||||||||
Добування карбон(ІV) оксиду
У пробірку покласти декілька шматочків крейди та долити хлоридної кислоти. Швидко закрити пробірку корком з газовідвідною трубкою, кінець якої занурити в пробірку з вапняною водою.
| ||||||||||||
Якісна реакція на карбонат-йон
Налити в пробірку 1 мл натрій карбонату, долити 0,5 мл хлоридної
кислоти й одразу закрити корком з газовідвідною трубкою, кінець якої
занурити в пробірку з вапняною
водою.
| ||||||||||||
| Лабораторна робота № 3 | ||||||||||||
| зм | арк | № докум. | підп. | дата | ||||||||
| розроб. | Добування карбон(ІV) оксиду і вивчення його властивостей | літ | арк | арк | ||||||||
| перевір. | Литвиненко | н | ||||||||||
| ________________ | ||||||||||||
| н. конт. | ||||||||||||
| затверд | ||||||||||||
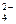 :
А) Ba2+;
В) Cu2+;
С) Cl—
:
А) Ba2+;
В) Cu2+;
С) Cl—