Вопрос 3. Реакция замещения, соединения, разложения, гидролиз. Кислотно-основные реакции, реакции осаждения.
Вопрос 2. Особая роль биогенных хим. элементов. Экологический фактор.
Элементы необходимые организму для построения и жизнедеятельности клеток и органов, называют биогенными элементами.
Биогенные элементы участвуют в ферментативных реакциях организма, регулируют осмотические процессы, являются основными частями буферных систем и регуляторами проницаемости биологических мембран.
Природные условия, оказывающие влияние на ЖД организма, называют экологическим фактором.
Экологический фактор может быть:
Физическим
Химическим
Биологическим
Экологические факторы среды могут оказывать на живые организмы воздействия разного рода:
раздражители, вызывающие приспособительные изменения физиологических и биохимических функций (например, повышение температуры воздуха ведет к увеличению потоотделения у млекопитающих и к охлаждению тела);
ограничители, обусловливающие невозможность существования в данных условиях (например, недостаток влаги в засушливых районах препятствует проникновению туда многих организмов)
модификаторы, вызывающие анатомические и морфологические изменения организмов (например, запыленность окружающей среды в индустриальных районах некоторых стран привела к образованию черных бабочек березовых пядениц, сохранивших свою светлую окраску в сельских местностях);
сигналы, свидетельствующие об изменении других факторов среды.
В характере воздействия экологических факторов на организм выявлен ряд общих закономерностей.
Закон оптимума – положительное или отрицательное влияние фактора на организмы - зависит от силы его воздействия. Недостаточное или избыточное действие фактора одинаково отрицательно сказывается на жизнедеятельности особей. Благоприятная сила воздействия экологического фактора называется зоной оптимума. Одни виды выносят колебания в широких пределах, другие - в узких. Широкая пластичность к какому-либо фактору обозначается прибавлением частицы «эври», узкая - «стено» (эвритермные, стенотермные - по отношению к температуре, эвриотопные и стенотопные - по отношению к местам обитания).
Вопрос 3. Реакция замещения, соединения, разложения, гидролиз. Кислотно-основные реакции, реакции осаждения.
1. Реакции соединения
В реакциях соединения хотя бы два элемента образуют один продукт:
2Na + Cl2 → 2NaCl - образование поваренной соли.
2. Реакции разложения
Эти реакции являются, как бы, противоположными по сути, реакциям соединения. В результате реакции разложения вещество распадается на два (3, 4...) более простых элемента (соединения):
2H2O → 2H2 + O2 - разложение воды
3. Реакции замещения
В результате реакций замещения, более активный элемент замещает в соединении менее активный:
Zn + CuSO4 →ZnSO4 + Cu
5. Кислотно-основные реакции
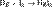 |
В реакциях переноса протона всегда принимает участие пара сопряжённых кислот и оснований. Степень диссоциации кислотно-основной пары зависит от концентрации Н+. Чаще всего приводится не собственно концентрация протонов, а её отрицательный логарифм, величина pH. В качестве меры химического потенциала переноса протона кислотно-основной пары служит величина рКа — отрицательный логарифм константы диссоциации кислоты Ka. Чем сильнее кислота, тем меньше её рКа. Кислоты с небольшимирКа могут протонировать основания с высокими рКа (зелёная стрелка).
6. Реакция осаждения
Реакции осаждения широко используют в качественном и количественном химическом анализе. Наиболее часто, по крайней мере в неорганическом анализе, используют реакции комплексообразования.