В072000-Бейорганикалы заттарды химиялы технологиясы мамандыыны Бейорганикалы химия пні бойынша Midterm сратары
| V1 | осылыстардаы галогендерді тотыу дрежелері (F-дан баса): |
| -1; | |
| +1; | |
| +5; |
| V1 | Mn- Tc – Re жай заттар атарыны |
| жалпы химиялы активтілігі тмендейді; | |
| сйытылан ккірт жне тз ышылымен тек ана Mn рекеттеседі; | |
| кернеу атарында барлы металдар сутекке дейін орналасан; |
| V1 | Фтор: |
| атомны электронды конфигурациясы 1s22s22p5; | |
| р-элемент; | |
| электртерістілігі е кшті элемент; |
| V1 | F2 – Cl2 – Br2 – J2 атарындаы |
| е берік молекула Cl2 | |
| тотысыздандырышты активтігі жоарылайды; | |
| тек ана F2 суды тотытырады; |
| V1 | Cl2 –ды рекеттестіру арылы алуа болады: |
| MnO2 + HCl (конц.) | |
| KMnO4 + HCl (конц.) | |
| K2Cr2O7 + HCl (конц.) |
| V1 | HF – HCl – HBr – HJ атарында |
| молекула беріктігі тмендейді; | |
| тотысыздандырыш асиеті кшейеді; | |
| тек ана балытыш ышыл ышылды тз тзеді; | |
| V1 | Хлор сілтімен (KOH) рекеттескенде тзілуі ммкін: |
| калий гипохлориті; | |
| калий хлораты; | |
| калий хлориді; |
| V1 | Жадайа байланысты HClO –ны айырылу тедеулері: |
| HClO HCl + O; | |
| HClO Cl2O + H2O; | |
| HClO HClO3 +HCl; |
| V1 | HClO–HСlO2 – HСlO3- HClO4 ышылдар атарында: |
| ышылды асиеттері кшейеді; | |
| молекуланы тратылыы жоарылайды; | |
| тотытырышты активтігі тмендейді; |
| V1 | Хлорлы ышылды асиеті: |
| тссіз, ауада ттінденетін сйы; | |
| оай ыдырайды; | |
| е кшті минералды ышыл; |
| V1 | Натрий гипохлоритімен Ni(OH)2 тотыу німі: |
| NiO(OH); | |
| NaCl; | |
| H2O; |
| V1 | Калий манганаты (VI) этил спиртімен рекеттескенде тзіледі: |
| марганец (1V) оксиді; | |
| CH3COH; | |
| KOH; |
| V1 | Платиналы металдара жатады: |
| Rh; | |
| Pd; | |
| Pt; |
| V1 | Калий перманганаты мен натрий сульфитіні ышылды ортада (H2SO4) ерітіндісімен рекеттескенде тзілетін німдер: |
| калий сульфаты; | |
| марганец (II) cульфаты; | |
| натрий сульфаты; |
| V1 | Калий перманганатын термиялы айыруда тзілетін нім: |
| калий манганаты; | |
| марганец (IV) оксиді; | |
| O2; |
| V1 | Тотыу дрежесі жоары фосфор ышылдары: |
| H3PO4; | |
| HPO3; | |
| H4P2O7; |
| V1 | Галогендерді реттік нмірі артан сайын : |
| атомды радиустары артады; | |
| бейметалды асиеті тмендейді; | |
| тотытырышты абілеті тмендейді; |
| V1 | Хлор гі … |
| хлорид пен кальций гипохлоритіні оспасы; | |
| формуласы - CaOCl2; | |
| кшті тотытырыш; |
| V1 | Иодсутек пен азотты ышыл рекеттескенде тзіледі: |
| азот (II) оксиді; | |
| J2; | |
| су; |
| V1 | Ккіртті аллотропиялы тр згерістері: |
| ромбалы ккірт - S8; | |
| моноклиндік ккірт - S8; | |
| пластикалы ккірт - S; |
| V1 | Сульфандар – бл… |
| кпккіртті сутекті осылыс; | |
| H2S3; | |
| H2S5; |
| V1 | Натрий дисульфиді тз ышылымен рекеттескенде тзіледі: |
| натрий хлориді; | |
| ккіртті сутек; | |
| бос ккірт; |
| V1 | ндірістік жадайда SO2 – ні SO3 –ке тотыуыны негізгі дістері: |
| нитрозды, NO2-ні олданады; | |
| контактты: tº = 400-600º C; катализатор. | |
| контактты:tº = 400-600º C; катализаторсыз. |
| V1 | Ккірт пероксоышылдары: |
| H2SO5; | |
| H2S2O8; | |
| ышылдар жне оларды тздары – кшті тотытырыш; |
| V1 | VI–А негізі топ эленттеріні жоарыдан тмен арай |
| атом радиустары артады; | |
| металды асиеттері кшейеді; | |
| тменгі о тотыу дрежесіндегі осылыстарыны тратылыы артады; |
| V1 | Хлорлы, хлорлылау жне ккіртті ышылдарды тздарыны атауы: |
| хлориттер; | |
| хлораттар; | |
| сульфиттер; |
| V1 | Суда жасы ериді: |
| Na2S; | |
| CaS; | |
| BaS; |
| V1 | Тз ышылында ериді: |
| FeS; | |
| MnS; | |
| ZnS; |
| V1 | Ккірт, селен жне теллур оксидтері: |
| SO3; | |
| SeO2; | |
| TeO2; |
| V1 | Кшті ышылдар: |
| ккірт; | |
| селенді; | |
| бромдысутек; |
| V1 | Ккіртсутек - |
| жаымсыз иісі бар газ; | |
| те улы; | |
| кшті тотысыздандырыш; |
| V1 | H2S тотыанда тзілетін нім болуы ммкін: |
| S | |
| SO2 | |
| H2SO4 |
| V1 | Ккіртсутек ышылы: |
| лсіз ышыл; | |
| кшті тотысыздандырыш; | |
| 2 атарда тз тзеді: ышылды жне орта; |
| V1 | Пирит: |
| оны SO2 –ні жау арылы алады ; | |
| сутек дисульфид тзы; | |
| темірді тотыу дрежесі: +4 |
| V1 | Калий нитритін калий дихроматыны ышыл (H2SO4) ерітіндісінде рекеттескендіргенде тзіледі: |
| калий нитраты; | |
| хром (III) сульфаты; | |
| калий сульфаты; |
| V1 | Сутек - … |
| е жеіл газ; | |
| суда аз ериді; | |
| осылыстарда крсететін тотыу дрежесі: +1 жне -1 |
| V1 | Галогендерді физикалы асиеттері: |
| хлор – оай сыылатын газ; | |
| бром – сйы; | |
| йод – атты зат; |
| V1 | лсіз ышыл: |
| селенді; | |
| теллурлы; | |
| ортофосфор; |
| V1 | осылыстарда ккіртті тотыу дрежесі: |
| -2; | |
| +4; | |
| +6; |
| V1 | Олеумны рамында бар: |
| H2S2O7; | |
| H2S3O10; | |
| H2S4O13; |
| V1 | -S-S-S- гомотізбегі мына осылыстарда кездеседі: |
| сульфандарда; | |
| полисульфидтерде; | |
| политион ышылдарында; |
| V1 | Аллотропты модификация тзуші элемент: |
| фосфор; | |
| ккірт; | |
| оттек; |
| V1 | Ккірт атомыны тотыу дрежесі тмен болатын осылыстар: |
| Na2S; | |
| BaS; | |
| SnS; |
| V1 | Калий перманганаты калий сульфитімен сілтілік (KOH) ортада рекеттескенде тзіледі: |
| калий сульфаты; | |
| калий манганаты; | |
| су; |
| V1 | Концентрлі ккірт ышылы тотысыздананда тзіледі: |
| SO2; | |
| H2S; | |
| S; |
| V1 | Ккірт ышылы – |
| кшті ышыл; | |
| ылал тартышты асиеті бар; | |
| тек ана сйытылан кйде тотытырыш асиет крсетеді; |
| V1 | Балытыш ышыл -.. |
| кші орташа ышыл; | |
| шынымен рекеттеседі; | |
| лсіз ышыл; |
| V1 | Аммоний дихроматын термиялы айыруда тзіледі: |
| хром (III) оксиді; | |
| азот; | |
| су; |
| V1 | Азотты-сутек оспасынан аммиакты алу дерісі - … |
| айтымды деріс; | |
| экзотермиялы; | |
| гетерогенді-катализдік; |
| V1 | Тменгі азотты тотыу дрежесі: |
| Аммиак; | |
| аммоний сульфаты; | |
| аммоний хлориді; |
| V1 | S Se Te Po атарында: |
| тотытырышты асиет тмендейді; | |
| тотысыздандарышты абілеті кшейеді; | |
| металды сипаты жоарылайды; |
| V1 | Элементтік ккірт тмендегідей реакцияа тсуге абілетті: |
| тотыу; | |
| тотысыздану; | |
| диспропорциялану; |
| V1 | Фосфорды аллотропиялы тр згерістері: |
| а фосфор; | |
| ызыл фосфор; | |
| ара фосфор; |
| V1 | Хлорды оттекті ышылдары: |
| HClO; | |
| HClO3; | |
| HClO4; |
| V1 | Калий перманганаты ышылды (H2SO4) ортада ккіртті сутекпен рекеттескенде тзіледі: |
| марганец (II) cульфаты; | |
| калий сульфаты; | |
| ккірт; |
| V1 | Ккірт ышылы олданылады: |
| мнайды тазартуда; | |
| тыайтыш ндірісінде; | |
| опарылыш заттар ндірісінде; |
| V1 | Ккіртті осылыстарда крсететін тотыу дрежелері: |
| -2-ден +6-а дейін; | |
| +4; | |
| +6; |
| V1 | Купорос: |
| FeSO4 7 H2O; | |
| CuSO45 H2O; | |
| ZnSO4 7H2O; |
| V1 | SO2 тзетін реакциялар: |
| S + O2 | |
| S +H2SO4(конц.) | |
| Ag + H2SO4 (конц.) |
| V1 | Гидролизі айтымсыз, аяына дейін жретін сульфидтер: |
| Al2S3; | |
| Cr2S3; | |
| Fe2S3; |
| V1 | Металл сульфидін алуа болады: |
| Алмасу реакциясы арылы; | |
| жай заттардан; | |
| кміртекті ыздыру арылы сульфатты тотысыздандыру; |
| V2 | Жер ыртысында е кп таралатын элементтер |
| Оттек | |
| Кремний | |
| Темір |
| V2 | 8 электронды ішкі абаты бар атомдар немесе иондар: |
| С-4 | |
| N-3 | |
| V+5 |
| V2 | Кремнийді айсысында ерітуге болады? |
| HF+HNO3оспасында | |
| за уаыт бойы су буымен | |
| КОН |
| V2 | SiO2 рамды жартылай асыл тастар |
| Сутас (Горный хрусталь) | |
| Жылтыр тас (Опал) | |
| Яшма |
| V2 | Екідайлы асиет крсететін электролиттер |
| Al(OH)3 | |
| Zn(OH)2 | |
| Cr(OH)3 |
| V2 | лсіз электролиттер |
| NH4 OH | |
| H2 CO3 | |
| Al(OH)3 |
| V2 | Тменде келтірілген ышылдарды е кштілері |
| HNO3 | |
| H 2SO4 | |
| НСlO4 |
| V2 | IVA топшасыны элементтеріне тн тотыу дрежелері |
| +4 | |
| +2 | |
| -4 |
| V2 | IVВ топшасыны элементтеріне тн тотыу дрежелері |
| +4 | |
| +2 | |
| -4 |
| V2 | VВ топшасыны элементтеріне тн тотыу дрежелері |
| +3 | |
| -3 | |
| +5 | |
| +1 | |
| -1 | |
| +2 | |
| -2 |
| V2 | VA топшасыны элементтеріне тн тотыу дрежелері |
| +3 | |
| -3 | |
| +5 |
| V2 | IІІA топшасыны элементтеріне тн тотыу дрежелері |
| +3 | |
| +1 | |
| +2 |
| V2 | IІІ В топшасыны элементтеріне тн тотыу дрежелері |
| +3 | |
| +1 | |
| +2 |
| V2 | ай металдарды концентрлі ккірт ышылы пассивтендіреді |
| Al | |
| Cr | |
| Fe |
| V2 | Гидразин – бл .... |
| Бифункциональды негіз | |
| Сілтілік ерітінділердегі кшті тотысыздандырыш | |
| Ауа рамындаы оттекте оай тотыатын азот бар осылыс |
| V2 | Азотты табиатта бос кйінде кездесетін осылыстары |
| NH3 | |
| NO2 | |
| N 2O5 |
| V2 | Тмен температураларда сйытылан азот ышылымен рекеттесетін металдар |
| Mg | |
| Cu | |
| Zn |
| V2 | Мына N2+ 3H2 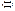 2NH3+ Q реакция бойынша аммиакты шыымын жоарылатуа сер ететін дйектер 2NH3+ Q реакция бойынша аммиакты шыымын жоарылатуа сер ететін дйектер
|
| Температура | |
| ысым | |
| ршіткі |
| V2 | Ккірт молекуласыны алыпты жадайдаы жне 800оС-ден 1000оС-ге дейін ыздыру кезіндегі рамы |
| S | |
| S2 | |
| S8 |
| V2 | Табиатта халькогендер детте мына осылыстар трінде кездеседі: |
| оксидтер ЭО2 | |
| FeS2 | |
| хлоридтер ЭСl2 |
| V2 | Кеістікте рылымы тетраэдр болып келетін, фосфор элементімен полимерлі бинарлы осылыс тзе алатын элементтер |
| O | |
| N | |
| S |
| V2 | СО2 -ны зертханада алу реакциясы |
MgСО3 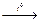
| |
СаСО3+ HCl 
| |
MgСО3+ HCl 
|
| V2 | Кміртекті тотысыздандырышты асиет крсететін осылыстары |
| CO | |
| НСООН | |
| КСN |
| V2 | Силан, силицид, германидті химиялы формулалары |
| Cа2Si | |
| SiH4 | |
| Mg2Ge |
| V2 | Кремний жне германий диоксидтері - бл.... |
| А тсті заттар | |
| Кристалды заттар | |
| Кптеген полиаморфты модификациялара ие заттар |
| V2 | Сулы ерітіндіде бор элементі келесі осылыстар трінде бола алады.... |
| B(ОН) 3 | |
| (В4О7)2- рамды оксоиондар | |
| B(ОН)4- |
| V2 | SiO2 –ны ерітетін заттар |
| HF | |
| КОНсйы | |
| Na2CO3 балыма |
| V2 | Тменде келтірілген бинарлы осылыстарды айсысын боридтар деп атауа болады |
| Mg3B2 | |
| Ве4В | |
| TiB |
| V2 | Борды ыздыранда мына заттармен рекеттеседі: |
| S | |
| N2 | |
| C |
| V2 | Кміртек мен концентрлі азот ышылыны рекеттесуі барысында мына зат блінеді. |
| су | |
| Кміртек диоксиді | |
| Азот диоксиді |
| V2 | AgNO3 + H3PO2+ H2O  реакциясы барысында мыналар блінеді реакциясы барысында мыналар блінеді
|
| Ag | |
| H3PO4 | |
| HNO3 |
| V2 | Конденсирленген фосфаттарыны рылымы мынадай болуы ммкін |
| Тізбекті рылымды | |
| Циклды рылымды | |
| Аралас рылымды |
| V2 | "А кшн" – бл ... зат |
| As2 O3рамды | |
| А тсті | |
| Суда нашар еритін |
| V2 | Алюминийді сйытылан азот ышылымен ыздыру кезінде рекеттесуі барысында мыналар тзіледі. |
| Алюминий нитраты | |
| Аммоний нитраты | |
| Су |
| V2 | Бураны "анатшалары" - бл: |
| Ауыр металдарды полиметабораттары | |
| Алуан трлі тстерге ие заттар | |
| Аналитикалы практикада d-элементтерді анытау шін олданылады |
| V2 | ns2 (n-1)d3 электронды конфигурацияа тн атомдар |
| V | |
| Nb | |
| Ta |
| V2 | ns2(n-1)d2 электронды конфигурацияа тн атомдар |
| Ti | |
| Zr | |
| Hf |
| V2 | ns2(n-1)d1 электронды конфигурацияа тн атомдар |
| Sc | |
| Y | |
| La |
| V2 | ыздыру кезінде азот блетін заттар |
| (NH4)2 Cr2 O7 | |
| NH4 NO2 | |
| N2H4+ KMnO4 |
| V2 | Сумен рекеттестіру арылы ыздыру кезінде аммиак блетін заттар |
| Li3N | |
| Mg3N2 | |
| Cl3N |
| V2 | NO алуа болатын реакция тедеулері |
Cu + HNO3сй 
| |
NH3+ O2  (ршіткі атысында) (ршіткі атысында)
| |
HNO2  (ыздыру жне жары тсіру) (ыздыру жне жары тсіру)
|
| V2 | NO2 алуа болатын реакция тедеулері |
Cu + HNO5конц 
| |
N2 O3 
| |
HNO3  (ыздыру жне жары тсіру) (ыздыру жне жары тсіру)
|
| V2 | Концентрлі азот ышылы андай металдарды пассивтендіреді |
| Al | |
| Cr | |
| Fe |
| V2 | Фосфинді РН3алуды ммкін болатын реакциялары |
Pа+ KOHконц 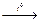
| |
| Mg3P2+H2O= | |
Ca3P2+ HCl 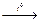
|
| V2 | Р2О5ысты суда еріткенде тзілетін ышылдар |
| H3(PO3)3 | |
| H3 PO4 | |
| H4 P2O7 |
| V2 | Фосфорды маызды тыайтыштарына жатады |
| Суперфосфат | |
| ос суперфосфат | |
| Преципитат |
| V2 | Фосфорды биологиялы жйелердегі маызы андай? |
| Р-О-Р фосфатты топтар РН рамына кіреді | |
| Р-О-Р фосфатты топтар ДН рамына кіреді | |
| Фосфор осылыстары биогенді заттара жатады, ал фосфор -биогенді элемент |
| V2 | Кміртек – шексіз кп органикалы осылыстарды тзуге бейім. Оны себебі мынада,.... |
| С-С байланысы осы топша элементтеріні екі атомы арасындаы байлансыа араанда лдеайда берік | |
| Кміртек атомыны гибридтелуге абілеті жоары | |
| Кміртек атомыны кіші млшеріне байланысты оны атысымен тзілетін байланыстар аса берік |
| V2 | Минералды тыайтыштар былай жіктеледі.... |
| жай | |
| Крделі | |
| Аралас |
| V2 | С-Si-Ge-Sn-Pb атарында бейметаллды асиеттерді металдыа ауысуы аны байаланымен, бл баытта элементтерді асиеттері біралыпты згермейді. Атап айтса.... |
| Кміртектен алайыа арай иондану энергиясы кемиді, біра орасында сл артады | |
| Кміртекті балу температурасы максималды, кремнийде 2 есе кемиді, кейін германий мен алайыда тмендейді де, орасында сл артады | |
| Топ номеріне сйкес келетін валенттік (4) кміртек мен кремнийге тн жне оны ролі алайы мен орасына арай тмендейді (В=2) |
| V2 | ыздыру кезінде кремний мынадай заттармен рекеттеседі... |
| NaOHконц | |
| Mg | |
| HNO3+ HF |
| V2 | Кміртекті аллотропты трзгерістері |
| Алмас | |
| Графит | |
| Карбин |
| V2 | Германий кремнийге сас, біра кміртектен те ерекшеленеді, атап айтса... |
| Кристаллды германий атомдары sp3 –гибридтелген алмас рылымына ие | |
| Германийдін электрткізгіштігі топшаны алдыны элементтеріне араанда аса жоары | |
| Блме температурасында германий жартылайткізгіш болып табылады |
| V2 | Бос кйінде борды алуды химиялы реакция тедеулері |
B2 O3+ Mg 
| |
ВI3 
| |
B2H6 
|
| V2 | алыпты жадайда борды ерітетін ышылдар |
| H2 SO4 сйыт. | |
| HNO3 | |
| НСl+3 HNO3 |
| V2 | Металды кальцийді аса сйытылан азот ышылында еріткенде тзілетін осылыстар |
| Ca(NO3)2 | |
| H2O | |
| NH4NO3 |
| V2 | Ерімейтін анодтарды андай материалдардан жасап шыарады |
| кмір | |
| графит | |
| платина |
| V2 | Сурик тз ышылын тотытырады, соны нтижесінде мынадай осылыстар тзіледі... |
| PbCl2 | |
| H2O | |
| Cl2 |
| V2 | Bi(OH)3 мен Na2SnO2 рекеттесуі кезінде мынадай осылыстар тзіледі... |
| Bi | |
| Na2SnO3 | |
| H2O |
| V2 | Аммиак синтезіні барлы нерксіптік рылылары циркуляция станымын олдану арылы жмыс жасайды: |
| Реакциядан кейін газдар оспасы суытылады | |
| Газдар оспасыны рамындаы аммиак конденсацияланады жне блініп алынады | |
| рекеттеспей алан азот пен сутек жаа газ оспасымен араластырылып, катализатора айта жіберіледі |
| V2 | S пен HNO3 рекеттесуі кезінде мынадай осылыстар тзіледі... |
| H2SO4 | |
| NO2 | |
| H2O |
| V2 | NaOH мен NO2 рекеттесуі кезінде мынадай осылыстар тзіледі... |
| NaNO3 | |
| NaNO2 | |
| H2O |
| V2 | Висмут (III) сульфидін концентрлі азот ышылында еріткенде тзілетін заттар: |
| Bi(NO3)3 | |
| NO | |
| S |
| V2 | Пероксоккірт ышылдарыны рамы: |
| Н 2SО5 | |
| Н2 S2О8 | |
| Н2 S3 О11 |
| V2 | К3AsO3, K2Cr2O7 жне ккірт ышылы ерітінділеріні рекеттесуі нтижесінде тзілетін осылыстар |
| К3AsO4 | |
| Cr2(SO4)3 | |
| K2SO4 |
| V2 | Алюминийді асиеттері |
| Амфотерлі асиеттер крсетеді | |
| осылыстарда катионны рамында кездесуі ммкін | |
| осылыстарда анионны рамында кездесуі ммкін |
| V2 | Алюминий сйытылан азот ышылымен арынды рекеттесіп, мынадай осылыстар тзіледі... |
| Al(NO3)3 | |
| N2O | |
| H2O |
| V2 | Алюминий зіні асиеттері бойынша бордан крт ерекшеленеді. Атап айтса.... |
| Атомный лкен млшерімен | |
| электрондарды бос d-дегейге те алу ммкіндігі электрондарды еркіндігін, делокализациялану дрежесін арттырады | |
| Жоары электро- жне жылуткізгіштікке ие |
| V2 | АlCl3 ерітіндісіне осылан зат оны гидролизін арттырады |
| Na2CO3 | |
| NaОН | |
| КОН |
| V2 | АlCl3 ерітіндісіне осылан зат тзды гидролизін тмендетеді |
| НСl | |
| Н2SO4 | |
| HBr |
| V2 | рамында мынадай блшектер бар ерітінділерді электролизі кезінде су молекулалары анодта тотыатын болады |
| SO4 2-, SO3 2- | |
| NO3-, PO43- | |
| СО32 |
| V2 | Электролиздеу арылы тздарыны сулы ерітінділерінен алуа ммкін емес металдар |
| Натрий | |
| Барий | |
| Алюминий |
| V2 | Еритін анод ретінде олдануа болатын металдар |
| Zn | |
| Sn | |
| Pb |
| V2 | орасын аккумуляторыны негізін райтын химиялы осылыстар (е арапайым трде) |
| Pb | |
| PbO2 | |
| H2SO4 |
| V2 | орасынды аккумуляторды зарядтау кезінде мынадай заттарды тзілуімен деріс жреді: |
| Pb | |
| PbO2 | |
| H2SO4 |
| V2 | Кобальтті кміртек (ІІ) оксиді атмосферасында 150-200°С температура жне 250 атм. ысым кезінде суда ерімейтін, біра органикалы еріткіштерде еритін карбонил типті осылыстар тзіледі. Бл осылыстарды рамы мен байланыс трі мынандай ... |
| Органикалы еріткіштерде осылыс димер Со2(СО)8 трінде кездеседі | |
| Со жне СО арасындаы байланыс донорлы – акцепторлы механизм бойынша, екі кобальт атомдарыны бос электрондарды жптасуы арылы тзіледі | |
| Карбонилдарда кобальт атомыны валенттігі 0 те |
| V2 | Германий топшасыны Ge – Sn – Pb атарындаы элементтер жай заттарыны химиялы активтігіні згеруін сипаттаыз |
| Германий топшасыны элементтеріні металды асиеттері артады | |
| Ge – Sn – Pb атарында металды активтілік (электрондарды беру абілеті) жалпы задылы бойынша артады | |
| Сйкесінше, аталан атарда химиялы активтілік артады |
| V2 | ышылдарды сйытылан сулы ерітінділерінде сутек иондарымен, тотыатын германий топшасыны элементтері |
| Ge – Sn – Pb атарында металлды асиеттері артады, сондытан осы атардаы активтігі тменірек германий сутек иондарымен тотыады | |
| Ge – Sn – Pb атарында металлды асиеттері артады, сондытан осы атардаы активтігі жоары алайы сутек иондарымен тотыады | |
| Ge – Sn – Pb атарында металлды асиеттері артады, сондытан осы атардаы активтігі жоары орасын сутек иондарымен тотыады |