Вечный двигатель (perpetuum mobile) первого рода невозможен. В любой изолированной системе общее количество энергии постоянно
Согласно этому закону, в любом процессе изменение внутренней энергии некоторой системы ΔU = U2 – U1 равно количеству тепла, которое сообщается системе за вычетом работы, которую совершает система:
ΔU = Q – A
Это уравнение можно рассматривать, как математическое выражение первого начала термодинамики.
При переходе системы из одного состояния в другое:
А = А' + р∙ΔV, где
А' - полезная работа, которую совершает система
р∙ΔV – работа против внешних сил, действующих на систему, кроме внешнего давления.
Подставим эти значения в уравнения первого начала термодинамики:
Q = ΔU + р∙ΔV + А'
Если система находится под воздействием внешнего давления, то уравнение примет вид:
Q = ΔU + р∙ΔV.
Энергетический эффект химической реакции может проявляться как чисто тепловой, связанный с изменением внутренней энергии системы, например реакция нейтрализации в разбавленном растворе: H+ + OH- = H2O + 57 кДж.
Для этого случая можно записать, что весь тепловой эффект ΔQ при постоянном объеме (изохорный процесс) равен изменению внутренней энергии ΔU: ΔQv = ΔU (количество тепла, подводимое к системе идёт на изменение внутренней энергии).
Однако если смешать в пробирке водные растворы карбоната натрия и соляной кислоты и быстро закрыть пробирку пробкой, то через некоторое время система совершит механическую работу, "«выстрелив"» пробкой. При этом температура растворов после реакции практически не изменяется. Работа совершается, когда повышенное давление в закрытой пробирке уравнивается с атмосферным после вылетания пробки. Таким образом, можно описать работу, как работу расширения газа, совершенную при постоянном давлении (изобарный процесс):
ΔQp = p∙ΔV (количество тепла идёт на работу против сил внешнего давления)
В общем случае, работа, совершаемая химической реакцией при постоянном давлении, состоит из изменения внутренней энергии и работы расширения: ΔQp = ΔU + p∙ΔV
Для большинства химических реакций, проводимых в открытых сосудах, удобно использовать функцию состояния, приращение которой равно теплоте, полученной системой в изобарном процессе. Эта функция называется энтальпия (от греч. "«энтальпо"»– нагреваю):
ΔQp = ΔH = ΔU + p∙ΔV
Другое определение: разность энтальпий в двух состояниях системы равна тепловому эффекту изобарного процесса.
Знак энтальпии определяется "«с точки зрения» самой системы: при выделении теплоты изменение энтальпии отрицательно, при поглощении теплоты изменение энтальпии положительно.
Энтальпия
Многочисленные химические процессы принято разделять на эндотермические и экзотермические с присущими им тепловыми эффектами. Очевидно, что можно ввести некоторые величины, которые позволят характеризовать способность вещества к поглощению или выделению энергии. Были введены две такие величины с учетом условий проведения процесса.
 Реакцию, протекающую при постоянном объеме (в замкнутом реакторе),
Реакцию, протекающую при постоянном объеме (в замкнутом реакторе),
|
характеризуют внутренней энергией (U), а при постоянном давлении в открытом сосуде – энтальпией (Н).
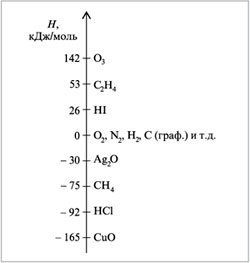
Для тех, кто проводит реакции в открытых сосудах, более важной величиной является энтальпия образования, обозначенная буквой Н (от англ. heat – теплота). Была введена шкала, позволяющая сопоставлять энтальпии образования всех веществ. Принято, что нулю на данной шкале соответствуют простые вещества (рис. 6.1).
Если простое вещество способно существовать в нескольких аллотропных формах, то нуль на указанной шкале обычно относится к наиболее устойчивой из них. Так, нулевую энтальпию образования имеет кислород, а не озон, графит, а не алмаз. Поскольку в результате превращения озона в кислород энергия выделяется, энтальпия образования озона больше.
Если при образовании сложного вещества из простых энергия затрачивается, то значение энтальпии для данного вещества положительное, а если выделяется, то отрицательное. Поскольку абсолютную энтальпию образования вещества определить невозможно, оперируют только с их разностями  H в искусственно введенной шкале.
H в искусственно введенной шкале.
На шкалу энтальпий наносят значения (обычно в кДж/моль), отнесенные к единице количества вещества. Так, значение  H для Ag2O, равное –30 (см. рис. 6.1), говорит о том, что при образовании 1 моль этого соединения из простых веществ (Ag и O2) выделяется энергия 30 кДж.
H для Ag2O, равное –30 (см. рис. 6.1), говорит о том, что при образовании 1 моль этого соединения из простых веществ (Ag и O2) выделяется энергия 30 кДж.
Разница энтальпий образования соединений обычно зависит от температуры, при которой проводится процесс. В связи с этим в справочниках, как правило, указывают стандартное (относящееся к температуре 25 °С) значение энтальпии, что обозначают верхним индексом (0). Обозначение энтальпии образования соединения (из простых веществ) снабжают также нижним индексом (f) (от англ. formation – образование). Тогда для стандартной энтальпии образования воды имеем:
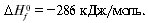
Кроме энтальпий образования в справочниках приводят и другие виды энтальпий, например, стандартные энтальпии сгорания, показывающие, сколько энергии выделяется при сгорании 1 моль вещества.
Тепловые эффекты (энтальпии) получают обычно на основе экспериментальных данных. В специальном приборе, который назван калориметром или калориметрической бомбой, проводят химическую реакцию с точно известными массами реагентов. Зная теплоемкость прибора, по изменению температуры в нем можно определить тепловой эффект реакции и занести найденное значение в справочник.
Не все вещества можно получить, помещая простые вещества непосредственно в реактор. Например, глюкозу С6Н12О6 нельзя получить при непосредственном контакте углерода, кислорода и водорода. Это вещество возникает в результате биохимических процессов в живой клетке.
В таких случаях приходит на помощь закон Гесса, который гласит, что тепловой эффект химической реакции определяется разностью энергетических состояний продуктов и реагентов и не зависит от пути реакции.