Призначення та властивості марганцю і середньовуглецевого феромарганцю
СПЕЦІАЛЬНА ЧАСТИНА
Марганець знаходиться в сьомій групі періодичної системи елементів Д.І. Менделєєва, порядковий номер 25, відносна атомна маса 54,938, атомний радіус 0,13 нм. Особливості енергетичного стану електронів ізольованого атома марганцю обумовлює і аномальні властивості його як металу (для ізольованого марганцю характерно заповнення рівня 4S² при наявності тільки п'яти електронів на 3d-рівні, на відміну від заліза, що має на 3d-рівні 6 електронів). Марганець-метал сріблястого кольору. Щільність марганцю 7,3 г / см ³, температура плавлення 1244 ° C, температура кипіння 2095 ° C, теплота плавлення 14,6 МДж / г атом, теплота випаровування 224,8 МДж / г атом. У рідкому стані залізо і марганець повністю взаємно розчинні, хімічних сполук не утворюють. Сплави заліза з 75-85% Mn легкоплавкі, температура плавлення ~ 1380 ° C. [1;2]
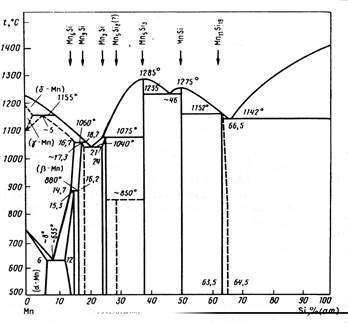
З вуглецем марганець утворює карбіди наступного складу: Mn2C6 (5,4% C), Mn3C (6,77% C), Mn5C2 (8,03% C) і Mn7C3 (8,57% C). Виділені області існування твердих розчинів вуглецю в твердому марганці на основі всіх його алотропних форм і карбідної ε-фази, що має широку область гомогенності. У системі Mn-C відзначені чотири перитектичні рівноважні реакції (рис.2.1):
Перитектична точка: Реакція Температура, °C
Р1 ж+δ-Mn↔γ-Mn 1120
P2 ж+ε-фаза↔γ-Mn 1240
P3 ж+Mn C ↔ε-фаза 1307
P4 ж+C ↔Mn7C3 1340
Підтверджено існування карбіду Mn3C у вузькому температурному інтервалі 980-1040 ° C. Експериментально вивчено термодинаміку карбідів марганцю, стабільних <1100 К. Зміна енергії Гіббса реакцій утворення Mn7C3, Mn5C2 і Mn23C6 одно -84540, -63430, -24960 Дж / моль відповідно. Ентальпія освіти Mn23C6 з реакції:
23Mnт +6 Cгр = Mn23C6 (T), (2.1)
дорівнює ΔH0298К =- 24550 Дж / моль.
Ентальпія утворення Mn7C3 з реакції:
7Mn +3 C = Mn7C3, (2.2)
дорівнює ΔH0298К =- 112400 Дж / моль.
 |
[1]
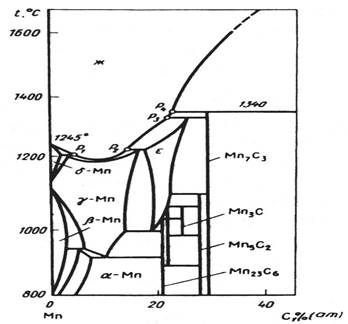
Рис. 2.1 - Діаграма рівноважного Рис. 2.2 - Діаграма рівноважного
стану системи Mn-С стану системи Mn-Si
Уточнена діаграма стану системи Mn-Si показана на рис.2.2 При побудові
цієї діаграми враховано існування силіциду Mn6Si, Mn9Si2 і Mn11Si19, які раніше не були відомі. Силіциди марганцю мають дещо меншу термодинамічну міцність, ніж силіциди заліза. Теплоти утворення Mn3Si, Mn5Si3, MnSi, MnSi17 відповідно дорівнюють 17,0; 24,85; 30,5 і 28,15 кДж / моль. [6]
Відомі силіциди марганцю: Mn6Si, Mn9Si2, Mn5Si3, MnSi та ін. Найбільш міцним з них є MnSi (33,8% Si), ΔH = 60,60 МДж / моль, температура плавлення 1170 ° C. Оскільки силіциди марганцю міцніші його карбіду, то зі збільшенням вмісту кремнію в сплаві вміст вуглецю знижується. Щільність рідких сплавів системи Mn-Si з підвищенням концентрації кремнію зменшується. При 1773К і атомному вмісту кремнію 30% і 60% щільність сплавів складає 5,31 і 4,35 г /см³. Висока ступінь мікронеоднорідності розплавів особливо в сфері концентрації кремнію 25-70% є наслідком спрямованої взаємодії між атомами марганцю, заліза і кремнію. Наявність в розплавах Mn-Si істотних ковалентних зв'язків підтверджується і характером розчинності водню в цих сплавах. Концентраційні залежності розчинності та коефіцієнт активності водню, а також зміна ентальпії та ентропії розчинення водню в розплавах мають екстремальний вид з похилим максимумом, відповідним атомного утримання кремнію 40-70%. Активність марганцю і кремнію в розплавах системи Mn-Si залежить від складу сплаву і температури.
З киснем марганець утворює чотири оксиди: MnO2, Mn2O3, Mn3O4, MnO. З них найбільш міцний MnO, температура дисоціації якого > 3000 ° C і теплота утворення ΔH0298К = 385,186 МДж / моль. Рівняння для розрахунку розчинності кисню в рідкому марганці при MnO = 1 має вигляд:
lg [O] Mn = (-4823 / T) +1,159, (2.3)
Евтектиці при 1515 К відповідає вміст кисню 0,0095%.Температурі 1273К незалежно від величини рО відповідає рівноважна фаза α-Mn3O4. При рО = 20 кПа виключається можливість утворення рівноважної фази манганозіта (MnO), а β-Mn3O4 при 1450ºС переходить у MnO, а перетворення MnOт → розплав наступає при 1657ºС . [1;2]
За сучасними уявленнями фосфор не утворює твердих розчинів у марганці, не дивлячись на порівняно високу розчинність в рідкому марганцю. У процесі кристалізації розплавів системи утворюються фосфіди. Відомі Фосфіди марганцю: Mn3P, Mn2P, Mn3P3, MnP. У розплавах системи Mn-P має місце сильна міжчастинкова взаємодія марганцю з фосфором, характеризується значним негативним відхиленням від закону Рауля. Досліджена активність фосфору в рідкому марганці при 1593К. Зниження концентрації фосфору в марганці з 15 до 0,5% супроводжується зменшенням його активності з 0,041 до 3*10-5 при одночасному збільшенні активності марганцю з 0,59 до 0,98. Концентраційна залежність коефіцієнтів активності марганцю γ-Mn і фосфору γ-Р при 1573 К в сплавах системи Mn-P описується рівняннями:
lg γMn= -4,29/[1+0,455(xMn/xP)2] , (2.4)
lg γР=18,88{[1+0,455(xMn*xP)]-1-[1+0,455(x2Mn/xP)]-1} , (2.5)
Випромінювання процесів випаровування сплавів Mn-P методом високотемпературної мас-спектроскопії показало, що випаровування фосфідів марганцю Mn3P і Mn2P відбувається конгруентно з подальшою дисоціацією в газовій фазі на Mnг і Pг. [3]
З представленої на рис.2.3 діаграми випливає, що існує велика область твердого розчину на основі γ-Fe і γ-Mn. Розчини на основі α-Mn і β-Mn з'являються при концентрації марганцю 68-70% і більше. Найнижча температура плавлення сплавів в системі Mn-Fe становить 1232 º С при атомному утриманні марганцю 87%. При 1300К активність заліза і марганцю до концентрації 50% змінюється по прямій лінії і підкоряється закону ідеальних розчинів. Інтегральна ентальпія змішування досягає максимуму - 8360 Дж / моль при хMn = 0,7.
 |
У загальній структурі споживання марганцю понад 90% його використовують у чорній металургії, при виплавці сталі, у вигляді різних марганцевих феросплавів. Одним з поширених марганцевих феросплавів є середньовуглецевий феромарганець, який за хімічним складом повинен задовольняти ДСТУ 3547-97, наведений в табл.2.1 [4]
Рис. 2.3 - Діаграма рівноважного стану системи Mn-Р
Таблиця 2.1-Хімічний склад середньовуглецевого феромарганцю, згідно з ДСТУ 3547-97
| Марка сплаву | Масовий зміст , % | |||||
| Mn | C | Si | P(A) | P(Б) | S | |
| марка А | Марка Б | |||||
| ФМн88 | більше 85,0 до 88,0 вкл. | 1,8 | 2,5 | 0,10 | 0,40 | н.б.0,35 |
Середньовуглецевий феромарганець представляє групу рафінованих дорогих марганцевих феросплавів і застосовується для легування низьковуглецевих конструкційних низько-і високолегованих високоякісних сталей. На замовлення споживачів середньовуглецевий феромарганець марки ФМн88 може поставлятися з вмістом вуглецю до 2,0% із вмістом фосфору до 0,1%, а внаслідок погіршення якості марганцевої сировини розширена межа по концентрації фосфору до 0,4%. У зв'язку з невиправданими витратами і подорожчанням сплаву при більш глибокому рафінуванні його від кремнію. У зв'язку з низьким вмістом вуглецю і невисоким вмістом фосфору в середньовуглецевому феромарганцю при його виробництві необхідно застосовувати сілікотермічний процес і низькофосфористу вихідну сировину.
Марганець використовується як: [6]
-Розкислювач: взаємодія марганцю з рідким залізом, що містить кисень, приводить до розкислення металу по реакції:
[Mn] Fe + [O] Fe = (MnO), (2.6)
KMn = aMnO / (aMn ao), (2.7)
де КMn-константа рівноваги реакції розкислення заліза марганцем; MnO, Mn, O-активності оксиду марганцю, марганцю і кисню.
При введенні в рідке залізо феромарганцю рівновага реакції розкислення встановлюється майже миттєво, що пояснюється великою швидкістю розчинення марганцевих феросплавів (це обумовлено відсутністю утворення шару з тугоплавких оксидів). Раскислювальна здатність марганцю нижче, ніж у кремнію, однак, кремній не завжди створює умови для формування бажаних оксидних включень.
-Десульфуратор: із сіркою, розчиненою в залізі і розплавах Fe-C, марганець утворює термодинамічно міцний сульфід, який має малу розчиненість у залізі і його сплавах, тому марганець застосовують у вигляді марганцевих концентратів у складі шихти для виплавки чавуну зі зниженим вмістом сірки.
-Легуючий елемент: у промислових нелегованих сталях міститься 0,4-0,8% Mn, в високолегованих - до 12-16% і навіть до 25-30%, в аустенітних чавунах - від 4 до17%. Тому для будівництва магістральних газопроводів розроблені і виплавляються у великому обсязі високоміцні низьколеговані сталі з марганцем, молібденом. При збільшенні вмісту марганцю від 1 до 1,8% розмір зерна фериту в марганець-молібденових сталях з 0,09% зменшується від 216 до 65 мкм, критична температура крихкості знижується з -58 до -118 ˚ C. У аустенітних сталях марганець у поєднанні з азотом заміняє дефіцитний і дорогий нікель. Марганець застосовують для одержання сплавів на залізній основі, наприклад, 75ГНД (75% Mn), легування кремнієво-алюмінієвих сплавів. Для легування сталей необхідно застосовувати марганцеві феросплави з низьким вмістом фосфору, так як марганець сильно знижує активність в рідкому залізі (εРMn = -7,17) і утворює надлишкові фази на межах зерен. [3]