
Категории:
АстрономияБиология
География
Другие языки
Интернет
Информатика
История
Культура
Литература
Логика
Математика
Медицина
Механика
Охрана труда
Педагогика
Политика
Право
Психология
Религия
Риторика
Социология
Спорт
Строительство
Технология
Транспорт
Физика
Философия
Финансы
Химия
Экология
Экономика
Электроника
Каталитический риформинг углеводородного сырья как химическое производство
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ №21
1. Каталитический риформинг углеводородного сырья как химическое производство
2. Математическая модель (кинетическое уравнение) процесс гидрокрекинга смеси парафиновых (Р), нафтеновых (N) и ароматических (А) углеводородов:
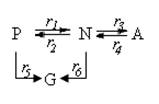
где G – газообразные углеводороды.
3. Неизотермический процесс в химическом реакторе (организация теплообмена в реакторе и температурные режимы).
4. Концепция минимизации отходов при синтезе ХТС и создании химических производств.
Каталитический риформинг углеводородного сырья как химическое производство
С помощью каталитического риформинга в нефтехимическом комплексе осуществляются одни из самых важных процессов:
1) превращение низкооктановых бензиновых фракций с получени ем высокооктановых компонентов бензина;
2) получение ароматических углеводородов.
Каталитический риформинг проводят в среде водорода при высоких температурах (740-800 °С), сравнительно низких давлениях (2-4 МПа) с применением специальных катализаторов. В процессе образуется избыточное количество водорода, которое выводится в виде водородсодержащего газа (до 80% Н2) и используется для процессов гидрирования.
Каталитический риформинг - сложный химический процесс, в котором протекают реакции, приводящие к образованию ароматических углеводородов:
дегидрирование шестичленных нафтенов
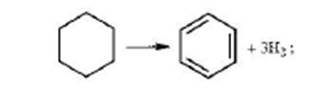
дегидроизомеризация пятичленных нафтенов

дегидроциклизация (ароматизация) нафтенов

Изомеризация парафинов и ароматических углеводородов

Основные реакции каталитического риформинга дегидрирование нафтенов и дегидроциклизация парафинов - протекают со значительным тепловым эффектом. Теплота дегидрирования метилцикло- гексана в толуол при рабочей температуре 800 К составляет 2212 кДж/кг, а дегидрирования н-гептана в толуол — 2539 кДж/кг.
Основные реакции ароматизации в процессе риформинга сопровождаются изомеризацией и гидрокрекингом углеводородов. Теплота реакций изомеризации невелика, а гидрокрекинг протекает с выделением теплоты, которая частично компенсирует эндотермический эффект основных реакций риформинга.
Исходя из термодинамики, повышение давления в процессе риформинга препятствует ароматизации сырья. Однако высокое давление водорода оказывается необходимым для насыщения непредельных углеводородов, образующихся в побочных реакциях крекинга. Повышенное давление и избыток водорода препятствуют коксообразованию. Компромиссным решением является организация циркуляции водородсодержащего газа, получаемого входе риформинга.
Молярное соотношение циркулирующего водородсодержащего газа и жидкофазного углеводородною сырья находится в пределах от 6 : 1 до 10 : 1, что соответствует кратности от 900 до 1500 м3 газа на 1 м3 сырья. Повышение кратности циркуляции водорода приводит к увеличению расхода энергии на компримирование циркулирующего газа и расхода топлива в трубчатой печи для подогрева этого газа. Оптимальная объемная концентрация водорода в циркулирующем газе составляет 80-90%.
В каталитическом риформинге применяют гетерогенные бифункциональные катализаторы. Эти катализаторы содержат металлы (платину, платину и рений, платину и иридий), которые инициируют реакции дегидрирования и гидрирования. Носителем катализаторов служит промотированный галогенами оксид алюминия, который облачает кислотными свойствами и катализирует реакции изомеризации и крекинга углеводородов. На катализаторах риформинга также протекают реакции дегидротшклизации парафиновых углеводородов.
Каталитический риформинг, основные из реакции которого относятся к эндотермическим, осуществляют в адиабатических реакторах. Реакторный блок промышленных установок риформинга обычно состоит из трех или четырех последовательно работающих реакторов с промежуточным подогревом парогазовой смеси в печи. Технологичес кая схема установки риформинга представлена на рис. 6.4. Работа установки характеризуется следующими показателями:

На установках риформинга с производительностью по бензину 600 тыс. т в год адиабатический реактор с аксиальным проходом реакционной смеси имеет внутренний диаметр корпуса 3 м и высоту 9,4 м. Перепад давления в нем достигает 1,6 МПа. Для установок мощностью 1 млн т сырья в год снижение гидравлического сопротивления достигается использованием реакторов с цилиндрическим слоем катализатора и радиальным ходом газа (см. разд. 5.6.8 и рис. 5.42). По мере работы катализатор в реакторе риформинга дезактивируется коксом, поэтому периодически проводится его окислительная регенерация.
Циркуляцию водородсодержащего газа осуществляют с помощью центробежных компрессоров с приводом от электродвигателя или паровой турбины.

Катализат процесса риформинга перерабатывают по схеме нефтехимического комплекса по двум альтернативным вариантам: получение автомобильного бензина или получение ароматических углеводородов.
При осуществлении первого варианта дополнительно проводится стабилизация бензина, связанная с удалением из него газов - пропана и бутана. Во втором варианте ароматические углеводороды выделяются из катализата избирательными растворителями, чаще диэтиленгли- колем, три этилен гликолем и сульфоланом. В последнее время промышленный интерес представляет N-метилпирролидол, который обладает улучшенной избирательностью и позволяет получить ароматические углеводороды повышенной концентрации. Схема экстракции ароматических углеводородов представлена на рис. 6.5.
Освобожденная от растворителя неароматическая часть катализата называется рафинатом и представлена смесью парафиновых углеводородов нормального и изостроения; изопарафины (52%), н-парафины (37%), нафтены (11%), ароматические углеводороды (1%). Рафинат используют как сырье в процессе пиролиза в производстве олефинов или при получении растворителей для различных отраслей народного хозяйства.

Смесь ароматических углеводородов разделяют четкой ректификацией с получением товарного бензола, толуола, этилбензола и о-ксилола. Изомеры м- и n-ксилола разделить ректификацией практически невозможно - для этого применяют низкотемпературную кристаллизацию, используя значительную разницу в их температуре замерзания (соответственно минус 47,9 °С и плюс 13,3 °С). Технологическая схема данного процесса довольно сложна, а использование холода существенно повышает экономические затраты, поэтому в последнее время низкотемпературную кристаллизацию заменяют десорбционным разделением на цеолитах. Таким образом в промышленности реализован процесс, именуемый «Парекс», который осуществляется в адсорбере с неподвижным слоем цеолита при температуре 150-180 °С и давлении 0,8-1,0 МПа. В качестве десорбента используют n-диэтилбензол. Экстракт, полученный после десорбции, представляет смесь л-ксилола и десорбента— n-диэтилбензола, разница в температурах кипения которых (138 °С и 183,6 °С соответственно) позволяет легко произвести отгонку. Десорбент циркулирует в замкнутом контуре: десорбция -отгонка - десорбция.
2. Математическая модель (кинетическое уравнение) процесс гидрокрекинга смеси парафиновых (Р), нафтеновых (N) и ароматических (А) углеводородов:

Кинетические модели могут представлять очень сложные зависимости, которые можно построить на основе механизма реакции. Приведем примеры простейших кинетических уравнений.
Каталитическая реакция А + В =R всегда состоит не менее, чем из двух элементарных стадий:

где к - катализатор; Ак - промежуточное соединение А с катализатором; к1, к2 - константы скорости элементарных стадий.
Скорость каждой стадии описывается кинетическим уравнением в соответствии с законом действующих масс подобным уравнению
(3.57) . Обозначим долю поверхности катализатора, занятую промежуточным соединением через (концентрация Ак). Тогда (1 - ) - концентрация активных центров катализатора. В стационарном состоянии скорости первой и второй элементарных стадий равны:

Из этого уравнения получаем

Скорость превращения А в R будет равна скорости второго этапа реакции:

 (3.61)
(3.61)
Из сопоставления кинетических уравнений для элементарной реакции (3.57) и для многостадийной (3.61) становится очевидным различие в зависимости скорости реакции от концентрации (рис. 3.10). Скорость элементарной реакции линейно растет с увеличением концентрации исходного компонента А (прямая 1 на рис. 3.10), тогда как

зависимость двухстадийной реакции имеет линейный характер до момента насыщения катализатора промежуточным веществом Ак (кривая 2 на рис. 3.10), Дальнейшее увеличение концентрации компонента А практически не влияет ни на скорость первой, ни на скорость второй стадии реакции.
Процессы нефтепереработки представляют собой многокомпонентную реагирующую систему, в которой протекают сотни реакций. Представить покомпонентный состав, детальную схему превращений и кинетические уравнения каждой реакции представляет собой чрезвычайно трудоемкую задачу. В этом случае нужно выделить группы компонентов, сходных по своим химическим свойствам, представить каждую группу псевдокомпонентами и определить возможность превращения между ними. Например, в наиболее простом варианте гидрокрекинга углеводородов можно выделить парафиновые (Р), нафтеновые (N) и ароматические (А) углеводороды, газообразные продукты крекинга (G) и представить следующую схему превращений между ними:

Скорости w превращения выделенных псевдокомпонентов представлены уравнениями, характерными дня превращения индивидуальных компонентов.
Например, для конверсии нафтенов в парафины

где рА, рN, ,рн2 - парциальные давления соответствующих фупп углеводородов и водорода; k, Кp - константы скорости и равновесия реакции.