ГЛАВА I. ЛАБОРАТОРНЫЙ ПРАКТИКУМ
БИОЛОГИЧЕСКАЯ ХИМИЯ
рабочая тетрадь
для студентов 1-2 курсов медицинского факультета
специальностей «Лечебное дело» и «Педиатрия»
Петрозаводск
Издательство ПетрГУ
Рассмотрено и утверждено к печати на заседании
редакционной комиссии медицинского факультета по отрасли науки и техники «Биология» 15 декабря 2011 г.
Печатается по решению редакционно-издательского совета
Петрозаводского государственного университета
Составители:
В. В. Осташкова, канд. биол. наук;
Н. С. Зыкина, канд. биол. наук;
О. В. Курмышкина.
 |
ПРЕДИСЛОВИЕ
Целью биологической химии является формирование знаний об основных закономерностях протекания метаболических процессов в организме человека, определяющих состояние его здоровья и адаптации на молекулярном, клеточном и органном уровне, а также умение применять полученные знания в своей профессиональной деятельности
Учебный процесс направлен на приобретение студентом такой общекультурной компетенции, как способность и готовность анализировать социально значимые проблемы и процессы, использовать на практике методы гуманитарных, естественнонаучных, медико-биологических и клинических наук в различных видах профессиональной и социальной деятельности (ОК-1). Кроме того, изучение основ биохимии формирует такие профессиональные компетенции как способность и готовность к работе с медико-технической аппаратурой, используемой в работе с пациентами, владеть компьютерной техникой, получать информацию из различных источников, работать с информацией в глобальных компьютерных сетях; применять возможности современных информационных технологий для решения профессиональных задач (ПК-9), а также способность и готовность к постановке диагноза на основании результатов биохимических исследований биологических жидкостей и с учётом законов течения патологии по органам, системам и организму в целом (ПК-15).
В задачи учебного процесса по данной дисциплине входит:
· приобретение знаний о химической природе входящих в состав живых организмов веществ, их превращениях и взаимосвязи с функцией различных органов и тканей, регуляции метаболических процессов и нарушениях;
· формирование у студентов умений пользоваться лабораторным оборудованием и реактивами с соблюдением правил техники безопасности, анализировать полученные данные результатов биохимических исследований и использовать полученные знания для объяснения характера возникающих в организме человека изменений и диагностики заболевания;
· формирование навыков работы с учебной, научной информативно-справочной литературой, умений применения современных информационных технологий и диагностических методов для решения профессиональ-ных задач.
В результате освоения дисциплины студент должен:
Знать:
· правила работы и техники безопасности в химических лабораториях, с реактивами, приборами, животными;
· строение и биохимические свойства основных классов биологически важных соединений: белков, нуклеиновых кислот, углеводов, липидов, витаминов;
· основные метаболические пути их певращения; ферментативный катализ; основы биоэнергетики;
· роль клеточных мембран и их транспортных систем в обмене веществ в организме человека;
· химико-биологическую сущность процессов, происхо-дящих на молекулярном и клеточном уровне в организме человека;
· основные механизмы регуляции метаболических превращений белков, нуклеиновых кислот, углеводов, липидов;
· диагностически значимые показатели биологических жидкостей (плазмы крови и мочи) у здорового человека.
Уметь:
· пользоваться учебной, научной, научно-популярной литературой, сетью Интернет для профессиональной деятельности, лабораторным оборудованием;
· проводить математический обсчёт полученных данных;
· интерпретировать результаты наиболее распростра-нённых методов лабораторной и функциональной диагностики;
· выполнять тестовые задания в любой форме, решать ситуационные задачи на основе теоретических знаний.
Владеть:
· базовыми технологиями преобразования информации: текстовые, табличные редакторы; техникой работы в Интернет для профессиональной деятельности;
· медико-функциональным понятийным аппаратом;
· навыками постановки предварительного диагноза на основании результатов лабораторного обследования пациентов.
Рабочая тетрадь по биологической химии содержит учебно-методический материал для выполнения лабораторных и практических занятий студентами 1-2 курсов медицинского факультета специальностей «Лечебное дело» и «Педиатрия».
На лабораторных занятиях студенты овладевают методами экспериментальных исследований, закрепляют теоретические знания, анализируют полученные результаты. В каждой лабораторной работе излагаются цель и задачи, поставленные перед студентом, принцип используемого метода, ход работы, предлагается проанализировать результаты проведённых исследований и сделать выводы.
В целях повышения эффективности работы при самоподготовке и на практических занятиях представлены основные вопросы по изучаемой теме, перечень заданий для самостоятельной работы.
В приложении студент может ознакомиться с вариантами контрольных работ, основными вопросами экзаменационных билетов и типовыми задачами по темам, технологической картой учебного процесса (планом всех видов работ по дисциплине по неделям 2- и 3-го семестра), а также подвести итоги своей деятельности в балльно-рейтинговой системе.
ГЛАВА I. ЛАБОРАТОРНЫЙ ПРАКТИКУМ
Й семестр
РАЗДЕЛ 1 БЕЛКИ
Состав и свойства белков
РАБОТА 1. ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ
Цель работы: ознакомиться с основными наиболее распространён-ными цветными реакциями на белки и доказать, что с их помощью можно выявить сходство и различия в аминокислотном составе исследуемых белков (на примере яичного альбумина и желатина).
Задачи:
· провести цветные реакции на белки с раствором яичного альбумина и желатина;
· определить, какой из исследуемых белков является полноценным;
· отметить, какие из проведённых реакций являются универсальными, а какие – специфическими;
· сравнить результаты проведённых исследований и сделать выводы.
Цветные реакции на белки являются качественными реакциями, обусловленными специфическими группами – радикалами. Некоторые из таких реакций широко используются в биохимической практике для изучения структуры и аминокислотного состава белков, их количественного определения.
1. Биуретовая реакция (на обнаружение пептидных связей в белках)
Принцип метода. Белки (пептиды) в щелочном растворе в присутствии солей меди (II) образуют комплексные её соединения, окрашенные в сине-фиолетовый или красно-фиолетовый цвет.
Для пептидной (амидной) группы характерна лактам-лактимная таутомерия:
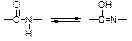
В щелочной среде преобладающая лактимная (енольная) форма полипептида взаимодействует с гидроксидом меди (II) с образованием стабильного окрашенного комплекса:
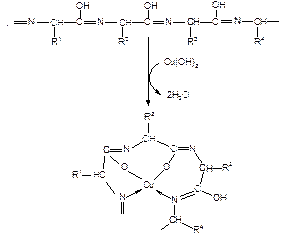
Ход работы. К 1 мл 1%-го раствора белка добавляют 1 мл 10%-го раствора щёлочи (NaOH или KOH) и 1 каплю 1%-го раствора сульфата меди. Появляется сине-фиолетовое или красно-фиолетовое окрашивание.
2. Нингидриновая реакция
(на аминогруппу, находящуюся в α-положении)
Принцип метода. Белки, полипептиды и свободные a-амино-кислоты при нагревании реагируют с нингидрином (трикетогидрин-ден-гидратом) с образованием продукта конденсации, окрашенного в фиолетовый цвет:


Ход работы. К 1 мл 1%-го раствора белка прибавляют 0,5 мл 0,5%-го раствора нингидрина и нагревают до кипения. Появляется сине-фиолетовое окрашивание.
3. Реакция Сакагучи (на аргинин)
Принцип метода. Белки, содержащие аргинин, в присутствии щелочи дают красное окрашивание с гипобромитом и a-нафтолом. Гуанидиновая группа аргинина окисляется гипобромитом, и окисленный аргинин при взаимодействии с a-нафтолом образует продукт конденсации красного цвета:

Ход работы. К 0,5 мл 1%-го раствора белка добавляют 0,5 мл 10%-го раствора щелочи, 3 капли 0,1%-го спиртового раствора a-нафтола и после перемешивания – 2-3 капли 2%-го раствора гипобромита натрия. Появляется красное окрашивание.
4. Реакция Фоля (на цистеин и цистин)
Принцип метода. При кипячении белка со щёлочью от цистеина (цистина) легко отщепляется сера в виде сероводорода, который в щелочной среде образует сульфид натрия:

Для выявления сульфида натрия используют ацетат свинца, который при взаимодействии с гидроксидом натрия превращается в тетрагидроксоплюмбат натрия:
Pb(CH3COO)2 + 4NaOH ® Na2[Pb(OH)4]+ 2CH3COONa.
В результате взаимодействия ионов серы и свинца образуется сульфид свинца чёрного или бурого цвета:
Na2S + Na2[Pb(OH)4] ® PbS¯ + 4NaOH.
Ход работы. К 1 мл 1%-го раствора белка или кусочку шерстяной нити добавляют 1 мл 30%-й щёлочи и 3-4 капли 5%-го раствора ацетата свинца. При интенсивном кипячении жидкость окрашивается в бурый или чёрный цвет.
5. Ксантопротеиновая реакция (на ароматические аминокислоты)
Принцип метода. При нагревании с концентрированной азотной кислотой белки дают жёлтое окрашивание. Реакция обусловлена наличием в белках ароматических аминокислот (фенилаланина, тирозина и триптофана) и основана на образовании нитропроизводных этих аминокислот, имеющих жёлтую окраску:

Нитропроизводные аминокислот в щелочной среде образуют соли хиноидной структуры, окрашенные в оранжевый цвет:

Ход работы. К 1 мл 1%-го раствора альбумина или яичного белка добавляют 5 капель концентрированной азотной кислоты. Появляется осадок. При осторожном нагревании смесь окрашивается в жёлтый цвет. После охлаждения осторожно добавляют 10 капель концентрированного раствора аммиака (или 30%-й раствор едкого натра), при этом жёлтая окраска переходит в оранжевую.
Проделывают эту реакцию с 1%-м раствором желатина, сравнивают результаты и делают выводы.
6. Реакция Милона (на тирозин)
Принцип метода. Реакция Милона открывает в белке тирозин, в составе которого имеется фенольный гидроксил. При нагревании белка с реактивом Милона (смесь нитратов и нитритов ртути (I) и (II), растворённых в концентрированной азотной кислоте) образуется осадок, окрашенный сначала в розовый, а затем в красный цвет. Реактив Милона даёт окрашивание почти со всеми фенолами:

Ход работы. К 1 мл 1%-го раствора яичного белка добавляют 3-5 капель реактива Милона и осторожно нагревают до образования окрашенного в красный цвет осадка.
Аналогично проделывают реакцию с растворами желатина. Полученные результаты сравнивают и делают вывод.
7. Реакция Паули (на гистидин и тирозин)
Принцип метода. Реакция Паули позволяет обнаружить в белке аминокислоты гистидин и тирозин, которые образуют с диазобензолсульфокислотой соединения вишнёво-красного цвета. Диазобензолсульфокислота образуется в реакции диазотирования при взаимодействии сульфаниловой кислоты с нитритом натрия (или калия) в кислой среде:

Ход работы. К 1 мл 1%-го раствора сульфаниловой кислоты (готовится на 5%-м растворе соляной кислоты) прибавляют 2 мл 0,5%-го раствора нитрита натрия, тщательно перемешивают, добавляют 2 мл 1%-го раствора яичного белка и после перемешивания 6 мл 10%-го раствора карбоната натрия. После перемешивания смесь окрашивается в вишнёво-красный цвет.
Реакцию проделывают с яичным альбумином и желатином, сравнивают полученные результаты и делают вывод.
Выводы:
Техника безопасности
Ø Категорически запрещается отмеривать концентрированные кислоты и щелочи обыкновенными пипетками – для отмеривания реактивов использовать мерные пробирки.
Ø Будьте внимательны при наливании концентрированных кислот и щелочей.
Ø В процессе нагревания постоянно перемешивайте жидкость, используйте пробки с газоотводными трубками для предотвращения выброса её из пробирки.
Ø Соблюдайте правила пожарной безопасности.
РАБОТА 2. РАСТВОРИМОСТЬ И РЕАКЦИИ ОСАЖДЕНИЯ БЕЛКОВ
Цель работы: изучение важного свойства белков - способности к растворению и реакциям осаждения.
Задачи:
· выделить основные фракции из яичного белка и доказать, что альбумин, входящий в его состав, хорошо растворяется в дистиллированной воде, а глобулин - в растворе солей;
· провести предложенные реакции необратимого осаждения белков;
· с помощью реакций высаливания разделить белки плазмы крови на основные фракции (фибриноген, альбумины и глобулины);
· доказать, что высаливание - обратимый процесс, при котором сохраняются свойства нативного белка, а денатурация - необратимый;
· проанализировать полученные результаты и сделать выводы.
1. Растворимость белков
Многие белки растворяются в воде, что обусловлено наличием на поверхности белковой молекулы свободных гидрофильных групп. Растворимость белка в воде зависит от структуры белка, реакции среды, присутствия электролитов. В кислой среде лучше растворяются белки, для которых характерны кислотные свойства, а в щелочной - белки, обладающие основными свойствами. Альбумины хорошо растворяются в дистиллированной воде, а глобулины растворимы в воде только в присутствии электролитов. Не растворяются в воде белки опорных тканей (коллаген, кератин, эластин и др.).
Ход работы
1. К 2 каплям неразведённого яичного белка прибавляют 1 мл дистиллированной воды и перемешивают. При этом яичный альбумин растворяется, а яичный глобулин выпадает в виде небольшого осадка.
2. К 2 каплям яичного белка прибавляют 1 мл 5%-го раствора хлорида калия. В слабом солевом растворе растворяются как альбумины, так и глобулины.
3. Проверяют растворимость в воде и 5%-м растворе хлористого калия белка кератина, содержащегося в шерсти и волосах.
2. Реакции осаждения белков
Реакции осаждения белков могут быть необратимыми и обратимыми.
А. Необратимое осаждение белков (денатурация)
Принцип метода. Необратимые реакции осаждения приводят к денатурации белков, при этом разрушается пространственная структура молекулы и белки утрачивают свои естественные биологические и физико-химические свойства. Денатурацию белков можно вызвать физическими воздействиями (кипячение, замораживание, высокое давление, вибрация, радиоактивное излучение и др.) и химическими осадителями.
1. Осаждение белков неорганическими осадителями
Осаждение беков минеральными кислотами
Ход работы. В пробирку осторожно наливают около 1 мл концентрированной азотной кислоты. Затем, наклонив пробирку, медленно по стенке добавляют 1 мл 1%-го раствора белка. На границе двух жидкостей появляется осадок в виде белого кольца.
Такую же реакцию проделывают с концентрированной соляной и серной кислотами.