Земля, как химическая лаборатория.
Санкт-Петербургский Государственный Университет.
Реферат по физике.
Данные о химическом составе Земли и тел Солнечной системы.
Выполнил студент первой группы
Козлов Глеб Александрович
Санкт-Петербург 2012г.
Оглавление.
1. Введение…………………………………………………...стр 2
2. Земля, как химическая лаборатория ………………… стр.3 -7
3. Химический состав Солнечной системы………...…..стр.8-12
4. Химический состав вселенной……………….……...стр.13-15
5. Список использованной литературы………..………….стр.16
Всё вещества на Земле, неважно, относится ли они к литосфере, атмосфере или гидросфере состоит из различных сочетаний небольшого числа химических элементов, а именно около 90, встречающихся в природе. Их эволюцию, распространение в земной коре, элементарный состав и свойства изучают множество дисциплин, главной из них остаётся геохимия. Суть этой науки наилучшим образом охарактеризовал В. И. Вернадский: «Геохимия научно изучает химические элементы, т. е. атомы земной коры и насколько возможно - всей планеты. Она изучает их историю, их распределение и движение в пространстве – времени, их генетические на нашей планете соотношения».
До сих пор геохимия остаётся наукой в буквальном смысле «поверхностной», так как для качественного и детального изучения доступна лишь маленькая часть Земли – кора. Только в последние десятилетий XX века учёные приступили к бурению сверхглубоких скважин. Однако, достичь земных полюсов, оказаться на дне Марианской впадины, и достичь Луны оказалось проще, чем «заглянуть поглубже под собственные ноги» - туда, где и по сей день во многом загадочная граница Мохо, отделяющая земную кору от мантии, ещё более загадочная сама мантия, и наконец, сердце Земли – Ядро.
Важно установить принцип распространения химических элементов в земной коре и почем одни из них встречаются часто, другие редко, а третьи и вовсе встречаются в исключительных случаях?
Земля, как химическая лаборатория.
Как таковое понятие химический элемент стало складываться ещё в XVII веке. Геохимия, как наука появилась только тогда, когда было открыто уже значительное число элементов периодической таблицы Д. И. Менделеева. Изучение химического состава десятков и сотен минералов позволило дать предварительную оценку распространённости элементов в земной коре.
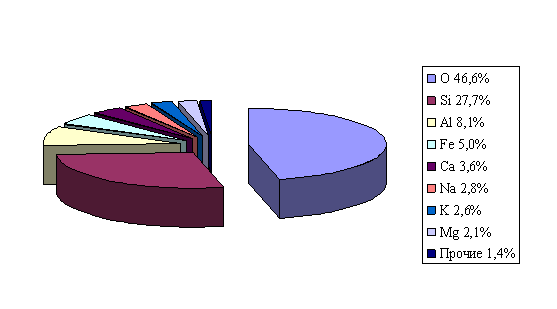
Первая попытка установить распространённость элементов предпринял английский минеролог Уильям Филипс в начале XIX века. Им было рассмотрено всего 10 элементов, которые чаще других встречаются в природе: кислород, кремний, алюминий, железо, водород, углерод, азот, кальций, калий и магний. Филипс заключил, что в неорганическом мире резко преобладает кислород, кремний, алюминий и железо, а в живой природе царствует четверка «органогенов» - элементов, составляющих основу органических веществ: углерод, водород, углерод и азот. Подсчёты Филипса не вызвали интереса. По мнению многих специалистов, следовало бы изучать особенности химического состава минералов и горных пород, а не определять какие-то, никому не нужные, «отвлечённые цифры». С подобным непониманием столкнулся на первых порах и главный химик геологической службы США Франк Уиглсуорт Кларк (1847-1931), когда в 70-х гг. XIX века он начал многолетнюю работу по точному определению содержания элементов в земной коре. Только потом, со временем, стало ясно, что то, что он сделал, был настоящий научный подвиг. Сам Кларк поводил мало химических анализов – он занимался статистикой, обобщением полученных ранее данных. Учёный рассуждал так: чем шире распространены горные породы, тем чаще отбираются их образцы, а значит, проводится больше их анализов. Если тщательно обработать все имеющиеся на данный момент данные, можно получить точное представление об элементарной составляющей земной коры. Не всей, конечно, но только верхней части. Кларк условно проводит её границу на 14 км. Эта же цифра используется и в современных расчётах. За 20 лет Кларк обобщил исследования более тысячи учёных и результаты свыше 5 тысяч анализов. И вот к каким выводам он пришёл. Если оценивать среднее содержание элементов в процентах от массы земной коры, то наиболее распространёнными оказываются следующие: кислород (47,00%), кремний (29,5%), алюминий (8,05%), железо (4,65%), кальций (2,96%), натрий (2,50%), калий (2,50%) и магний (1,87%). Это — современные данные, но они в незначительной степени отличаются от данных Кларка. В сумме все эти числа дают 99,03%. Следовательно, на долю всех прочих элементов приходится менее 1%. Отсюда следует важнейшее заключение: химические элементы в земной коре встречаются крайне неравномерно. И ещё: все перечисленные элементы располагаются в верхней части периодической системы; из них наибольший порядковый номер — 26 — имеет железо.
Попытку заглянуть глубже и оценить содержание элементов в мантии и ядре предпринял. американский исследователь Б. Мэйсон, основываясь на существующих гипотезах о внутреннем строении Земли. По Мэйсону, в первую десятку наиболее распространённых элементов нашей планеты в целом вошли железо (38,8%), кислород (27,17%), кремний (13,84%), магний (11,25%), сера (2,74%), никель (2,7%), алюминий (1,07%), кальций (1,07%), натрий (0,51%) и кобальт (0,2%).
Работы Кларка основательно подогрели интерес к количественной геохимии. Содержание химических элементов в земной коре стало такой же важной их характеристикой, как порядковый номер и атомный вес. В 1933 г. Ферсман предложил называть эти величины кларками.
Немногие учёные удостаивались такой чести — навечно сохранить своё имя в названии той или иной количественной величины.
Многие существенные закономерности химии Земли позволяет выявить и понять анализ кларков. Да и не только Земли: ведь и в Солнечной системе, и во всей Вселенной «живут» и находятся в постоянном развитии те же самые химические элементы, которые составляют нашу планету.
Если взглянуть на таблицу Менделеева, то можно увидеть, что под символами элементов проставлены их кларки (хотя и далеко не всегда). Так же можно увидеть, что содержание элементов в земной коре уменьшается при движении от начала таблицы к её концу. Конечно, не всё так просто, но суть примерно такая. Другую примечательную закономерность обнаружил в 1914 г. итальянский физик Дж. Оддо. В земной коре преобладают элементы с четным порядковым номером и четной атомной массой. Более подробно это явление было изучено американским ученым У. Гаркинсом. Оно получило название правила Оддо – Гаркинса и формулируется так: из двух соседних элементов в периодической таблице содержание четного в земной коре будет больше. Это можно легко заметить на примере восьми главных элементов, образующих 99 % массы земной коры. Из них четные элементы составляют 86 %, а нечетные – всего 13 %.
В вступительной части упоминалось что некоторые минералы широко распространены в земной коре, вторые редки, а третьи исключительны. Разберёмся с, так сказать, «Геохимическими редкостями». Обратим внимание на самую правую колонку таблицы Менделеева. Она состоит из так называемых благородных (или инертных) газов, которые вместе с кислородом, азотом и водородом входят в состав земной атмосферы. Это гелий, неон, аргон, криптон, ксенон и радон. Под символами этих элементов (за исключением радона) кларки даже не проставлены. И не случайно: благородные газы (и то не все) с большим трудом вступают в химические взаимодействия. Это объясняется особенностями строения их атомов. Немногим более 30 лет прошло с тех пор, как в лабораторных условиях удалось получить химические соединения ксенона и криптона. В природе же благородные газы совершенно не способны соединяться с другими элементами и входить в состав минералов и горных пород, потому и не могут задерживаться в них. Более того, они постоянно рассеивались, улетучиваясь из атмосферы Земли в космическое пространство. Лишь аргон имеет своеобразный источник пополнения: он постоянно образуется из калия благодаря радиоактивному распаду одного из его изотопов (т.е. разновидностей атомов с одинаковым числом протонов и различными числами нейтронов). Поэтому содержание аргона в 100 раз больше, чем всех остальных инертных газов вместе взятых.
А вот другая область «геохимических редкостей» — радиоактивные элементы: у них все изотопы нестабильны и распадаются, превращаясь в конце концов в изотопы свинца. Это элементы, находящиеся в конце периодической системы, начиная с полония (порядковый номер 84). Следующий за ним астат вообще на Земле отсутствует (он был получен искусственно в результате ядерных реакций). Затем следует радон (радиоактивный инертный газ), франций, радий, актиний, протактиний... Кларки их ничтожно малы.
Объяснение этому простое. Первоначальные «запасы» полония, радона, радия, актиния, протактиния, которые имелись на планете в далёкие времена её образования, давным-давно «съедены» радиоактивностью. Те же их количества, которые мы ныне обнаруживаем в земных минералах, имеют вторичное происхождение. Они постоянно воспроизводятся благодаря радиоактивному распаду урана и тория. Торий и уран отличаются от прочих элементов конца периодической системы несравненно большей продолжительностью своей жизни, которая измеряется миллиардами лет. Поэтому «первозданные» уран и торий сохранились на Земле. И их открывали в природных минералах как обычные стабильные элементы. По кларкам они принадлежат к элементам средней распространённости. А вот тех вторичных радиоактивных элементов, которые из них образовались, в 16-километровой толще земной коры ничтожно мало — немногим более 1 млн т.
Геохимики широко пользуются понятием «редкие элементы». Обычно к ним относят те, чей кларк имеет порядок 105%. Однако это понятие не очень строгое. Наглядный пример: германий, элемент с порядковым номером 32, один из тех, которые были предсказаны Менделеевым. Кларк германия составляет 104%, что позволяет отнести его к элементам-«середнякам». Между тем он был открыт только в 1886 г., гораздо позже, чем очень многие куда менее распространённые его «собратья». Немецкий химик Клеменс Винклер извлёк германий из очень редкого минерала аргиродита. Лишь позже выяснилось, что аргиродит — представитель весьма немногочисленных собственных минералов германия, таких, в которые он входит в качестве главной составной части. В основном же германий буквально распылён, рассеян по минералам и рудам различных элементов. Те элементы, которые фактически не имеют собственных минералов, получили название рассеянных. К их числу помимо германия принадлежат скандий, галлий, рубидий, цезий, индий, гафний и некоторые другие.
В 20-х гг. XX в. норвежский геохимик Виктор Гольдшмидт создал геохимическую классификацию элементов, которая опирается на периодическую систему и связана с особенностями построения электронных оболочек атомов.
Четыре группы элементов предложил учёный.
Самая большая из них включает 54 элемента, т.е. более половины из встречающихся в природе. Они называются литофилъными, что в дословном переводе с греческого означает «камнелюбивые». Эти элементы с лёгкостью образуют содержащие кислород минералы и составляют основу большинства горных пород. «Литофилы» в свободном состоянии в земной коре не встречаются. Среди них — щелочные и щёлочноземельные металлы, алюминий, кремний, титан, торий, уран и другие.
Далее следует группа из 19 халькофильных («меднолюбивых») элементов. Так их назвали потому, что в своём геохимическом поведении (т.е. в процессе образования минералов) они похожи на медь — например, охотно вступают в соединения с серой. Наряду с медью к «халькофилам» относятся серебро, золото, цинк, ртуть, германий, свинец. Некоторые из них встречаются в природе в виде простых веществ.
К 11 сидпрофильным («железолюбивым») элементам принадлежат железо, кобальт, никель, платиновые металлы, молибден и рений. Самородное состояние для большинства из них вполне обычно.
И наконец, 8 элементов — водород, азот, кислород и благородные газы — составляют земную атмосферу. Это — атмофильные (т.е. «любящие пар») элементы.
Такая классификация не только раскладывает элементы по геохимическим «полочкам», она позволяет нагляднее объяснить ход процессов, которые в течение миллиардов лет формировали состав и строение земных недр. Эта геохимическая классификация элементов оказывает большую помощь при изучении сложнейших процессов химической дифференциации различных веществ и соединений в толще земной коры и в метеоритах. Она объясняет распределение отдельных элементов по различным слоям Земли. Можно провести аналогию с плавкой шихты в доменной печи. При доменной плавке вверх удаляются газы, сверху
расплава всплывает шлак, под шлаком накапливаются сульфидные соединения, а в нижней части домны образуется металлическое железо. Мы видим, что происходит как бы отчетливое разделение элементов па четыре геохимические группы. Наверху - газовая фаза (атмофилы), ниже - шлаки, скопление разных оксидов (литофилы), еще ниже - сульфиды (халькофилы) и, наконец, в самом низу - металлическое железо (сидерофилы).
Ученые полагают, что на заре своего образования планета Земля была холодной и лишь со временем составляющее ее вещество расплавилось под влиянием гравитационного сжатия и теплоты распада радиоактивных элементов. Земля стала представлять собой нечто вроде гигантской доменной печи. На ее “дне” - в самом центре планеты -оседали расплавленные железо, кобальт и никель, типичные сидерофильные элементы. От центра к поверхности располагались “сульфиды” и “шлаки”, составляющие мантию и земную кору. В состав земной атмосферы вошли выделявшиеся в ходе этой гигантской плавки газы - атмофилы. Затем начался процесс остывания, возникла “земная твердь”, появились водоемы. Вероятно, жизнь на Земле могла возникнуть лишь тогда, когда образовалась земная кора и появилась гидросфера - водная оболочка Земли.
В процессе “доменной плавки” образовывались многочисленные минералы и руды, изучение распределения и состава которых входит в задачи геохимии. Здесь она тесно связана с геологией. В XX столетии возникла еще одна научная дисциплина на стыке наук - биогеохимия. Основателем ее был В. И. Вернадский. Она изучает геохимические процессы, связанные с живым веществом. Живые организмы играют огромную роль в миграции атомов. Результатом деятельности живых организмов является образование еще одной оболочки Земли-биосферы. И наконец, назовем еще гидрохимию - химию гидросферы: она тоже ведь составная часть геохимии. Каждая из этих геохимических “ветвей” своими методами изучает историю атомов химических элементов. Существующая модель земного шара “земная кора – мантия - ядро” ныне общепринята. Более или менее установились представления относительно состава этих сфер Земли. Правда, достижения экспериментальной геохимии в последнее время несколько поколебали сложившиеся представления. При бурении скважины на Кольском полуострове выяснилось, что температура земных недр растет с глубиной быстрее, чем это предполагалось; несколько иными оказались состав и строение пород, залегающих на больших глубинах.
А что же ожидает ученых дальше по мере проникновения в еще большие земные глубины?
По мере удаления от поверхности Земли увеличивается сжатие, которому подвергается вещество. Расчеты показывают, что в земном ядре давление должно достигать 3 млн. атм. При таком колоссальном постоянно действующем давлении очень многие вещества как бы металлизируются, переходят в металлическое состояние. Появлялась даже гипотеза, что ядро нашей планеты состоит из металлического водорода. (Кстати, не так давно в США ученым удалось получить водород в металлическом состоянии.) Все это очень проблематично,
но если считать, что Земля имеет железоникелькобальтовое ядро, то свойства этих металлов в условиях колоссальных давлений должны быть необычными. При таких сжатиях могут наблюдаться и еще более удивительные явления: может изменяться электронная структура атомов химических элементов, прежде всего внешние электронные оболочки.
Каждый из вас без труда изобразит строение атома калия. У него 19 электронов: два на К-оболочке, восемь на L-оболочке, а также восемь на М-оболочке и один электрон на внешней N-оболочке. Но, как известно, М-оболочка остается еще не заполненной и располагает десятью “вакантными” местами. Теоретики предполагают, что при сверхвысоких давлениях единственный электрон из внешней оболочки атома калия может быть перемещен на одно из свободных мест в предыдущей недостроенной оболочке. Образуется необычный атом: он имеет заряд ядра такой же, как у калия, ядро атома остается неизменным, но электронная конфигурация перестраивается. В ней вместо четырех оболочек оказывается три, распределение электронов в которой 2-8-9. Если бы такой “неокалий” удалось каким-то образом приготовить в лаборатории и сохранить его в таком необычном состоянии, то, очевидно, свойства его оказались бы весьма своеобразными. Ведь химические особенности элементов зависят прежде всего от строения внешних электронных оболочек их атомов. Вполне допустимо и подтверждается расчетами, что на больших глубинах такого рода электронные перестройки реальны и там действительно могут существовать атомы разных химических элементов с необычными электронными конфигурациями. Поэтому сейчас уже можно говорить о новой области геохимической науки - геохимии высоких давлений.
Многие задачи решает современная геохимия. Особенно велика ее роль в поисках полезных ископаемых. Но не менее важно и одно из ее теоретических значений - создание важнейших обобщений относительно эволюции вещества Земли в связи с эволюцией атомов в космосе. Ведь химический состав нашей планеты -это своеобразное отражение давно протекавших космических процессов, в том числе образования химических элементов в звездах. Геохимическая история атомов на Земле тесно связана с их историей космической, которую изучает наука космохимия.