Гиббс энергиясы. Гельмгольц энергиясы
ИП №6 от 14 июня 2007 г.
араанды мемлекеттік медицина университеті
Химия курсымен фармацевтикалы пндер кафедрасы
ДРІС
Таырыбы: Термодинамика жне химиялы реакцияларды кинетикасы.
Пн: Химия
Маманды: 5В130100 «Жалпы медицина»
Курс: 1
Уаыт (затыы): 50 минут
араанды 2014
Кафедраны жиналысында бекітілген
_27_._06_. 2014. № _10_ Хаттама
Курса жауапты Власова Л.М.
Таырыбы: Термодинамика жне химиялы реакцияларды кинетикасы.
Масаты:
Студенттерге термодинамиканы негізгі тсініктері мен задарын таныстырып, химиялы реакцияларды кинетикасы жне тірі организмдегі катализді ролі туралы тсінік беру.
Дрісті жоспары:
1. Термодинамика. Негізгі тсініктері мен задарын
2. Химиялы кинетика жне катализ.
Дріс тезисі: :
Термодинамика жне химиялы реакцияларды кинетикасы.
1.1.1 Термодинамиканы негізгі бастамалары жне задары
Кез-келген химиялы згеріс барысында жылу белініп не сііріледі, немесе химиялы реакция нтижесінде зге бip жмыстар атарылады. Мысалы, зіміз білетін бензинні жануы барысында жылу белініп, двигатель жмыс істейді, машина озалыса ие болады.
Міне, осы жылу жне жмыс шамалары бойынша химиялы реакцияны жруін санды трде сипаттауа ммкіндік туындайды екен жне осы мселемен айналысатын ілімді химиялы термодинамика деп атайды.
Жйе (система) - зіміздіоршаан ортаны кеістіктегі блігі, дене тобы, зат немесе заттар жиыны.
Термодинамикалы жйе - сырты оршаан ортадан ойша белініп
арастырылатын, зара жылу жне механикалы серлесуде болатын дене не заттар жиыны, тобы.
Термодинамикалы жйені жабы, ашы жне ошауланан деп шке бледі.
Жйе - зін оршаан ортамен зат алмаспай тек энергиясымен ана алмасса - жабы, ал зат алмасуы да орын алса - ашы жйе деп аталады.
Ошауланан (изолированный) жйеде - оршаан ортамен зат жне энергия алмасуы орын алмайды.
Жйені райтын дене бліктері белгілі бip кеістік блігінде бетпен шектеліп, жне де сол блікті н бойында химиялы рамы, рылымы, термодинамикалы асиеттері бірдей болса, онда осы блікті – фаза – деп атайды.
Жйе райтын фазалар бірдей агрегатты кйде болса - біртекті (гомогенді), ал ртрлі кйде болса - ртекті (гетерогенді) деп блінеді.
Жалпы термодинамикалы жйе тыылыты сипаттау шін, оны физикалы - химиялы асиеттерінен, яни клемі, ысымы, температурасы, химиялы рамы жне т.б. хабардар болуымыз керек. Осы орайда зімізге таныс кй тедеулеріні туелділігінен зара байланыста болатын шамалар туралы дйекті ым алуымыза ммкіндік туындайды.
Аталан кй тедеулерінде кездесетін айналмалылар кй шамалары (параметрі) деп аталынады.
Кез-келген кй шамаларыныц згepici термодинамикалы былыс (процесс) деп аталынады да кй шамасыны тратылыына арай тмедегіше жіктелінеді:
р = const – изобарлы,
V = const – изохорлы,
Т = const – изотермиялы,
Сырты оршаан ортамен жылу жне зат алмаспай жретін былыс – адиабатты деп аталып pV = const тедеуімен рнектеледі. Мндаы – адиабата крсеткіші жне бл былыс ошауланан жйелерде орын алады.
1.1.2 Термодинамиканы бірінші заы
Термодинамиканы бірінші тануыны негізгі трі былай айтылады:
- Трлі энергиялар бір-біріне те эквиваленттілік атынаста айналады.
- Оашаланан кйде энергияны р тріні ысымы згермейді.
- Бір трден екінші трге айналанда энергия жоалмайды да, жаадан пайда болмайды.
- Жмысты жотан шыаратын машина жасау ммкін емес.
Термодинамикалы жйемен энергия алмасуы - жылу мен жмыс трінде орын алатындытан аталан шамалар ішкі энергия згерісімен туелді байланыста болады.
Жйеге, жылу трінде берілген энергия, жйе ішкі энергиясын згертіп, белгілі бip жмыс атаруа жмсалады.
Кнделікті мірде, трмыста орын алатын жылу, жмыс жне ішкі энергия шамаларыны зара байланыстыы термодинамика іліміні бірінші бастамасы деген атпен тмендегінше тжырымдалады.
Ошауланан жйені энергиясы траты шама: U ~ const.
Жйеге оршаан ортадан жылу трінде берілген энергия - оны ішкі энергиясын згертіп, белгілі бip жмыс атарады жне бл математикалы тілде тмендегідей рнектеледі:
Q = U + A,
мндаы: 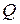 - жылу млшері;
- жылу млшері;
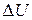 - ішкі энергия згерісі;
- ішкі энергия згерісі;
 - жмыс шамасы;
- жмыс шамасы;
T,p=const
A=pV

осыдан шыатыны


Міне осыдан,  – осындысы Н – энтальпия деп атайды. Демек, энтальпия термодинамикалы жйені толытау сипаттайтын энергетикалы шама.
– осындысы Н – энтальпия деп атайды. Демек, энтальпия термодинамикалы жйені толытау сипаттайтын энергетикалы шама.  – боландытан, энтальпия шамасы да кй функциясы болып табылады, оан ішкі энергия асиеттеріні брі де тн.
– боландытан, энтальпия шамасы да кй функциясы болып табылады, оан ішкі энергия асиеттеріні брі де тн.
1.1.3 Термодинамиканы екінші заы
з бетінше жретін процестерді баыты. Энтропия
Термодинамиканы 1 заы бойынша, кез келген процесті барысында, оны ішінде, жанды азаларда жретін процестерде де энергия шпейді жне жотан пайда болмайды. Энергияны ртрлі формалары бір-біріне эквивалентті млшерде айналады. Біра термодинамиканы 1 заы энергияны тасымалдануына негізделген процесті баыты, энергияны ауысуы аншалыты толы жретіндігі жне химиялы процесті орындалу шегі туралы апарат бермейді. Сондытан бл мселелерді шешу шін баса термодинамикалы факторларды пайдалану керек.
Неге реакция кері баытта жрмейді. Бл процесті тсіндіру шін Ю.Томсен жне М.Бертло сынан максимал жмыс аидасын пайдалануа болады. Ол бойынша, жылуды бле жретін реакциялар ана з бетінше жруі ммкін. Біра, орыс алымдары Д.И.Менделеев жне А.Л.Потылицин бл аидаа баынбайтын кптеген фактлерді келтіріп, з бетінше жретін эндотермиялы реакцияларды да болатындыын длелдеді.
Химиялы жне физикалы-химиялы процестерді з бетінше жруі жйені з ішкі энергиясын минимума жеткізіп, энергияны арты млшерін барынша сырты ортаа блуге мтылуына байланысты болатындыы айын. Табии процестерді з бетінше орындалуыны екінші себебіне жйені максимум ретсіздікке мтылуы жатады.
Осыдан, барлы з бетінше жретін процестер мынадай екі негізгі фактора байланысты орындалады:
- жйені минимум энергияа мтылуы;
- жйені максимум ретсіздікке, ммкіншілігі жоары кйге мтылуы.
Жйені ммкіншілігі жоары кйіні немесе ретсіздік шамасыны сипаттамасына энтропия S, Дж/моль К жатады. Энтропия да температура, ысым, ішкі знергия жне энтальпия сияты жйені немесе затты табиатына жне кйіне байланысты болады. Термодинамикалы жйені белгілі бір кйіне энтропияны белгілі бір мні сйкес келеді жне жйені аталан кйіні ммкіншілігі нерлым жоары болса, энтропия да сорлым жоары болады.
Кптеген микроблшектерден ралан жйені макрокйіні ммкіншілігі микроблшектерді (атомдар, молекулалар, т.б.) орналасу амалдарыны жне дістеріні санына байланысты болады. Нерлым микроблшектер кп болса, сорлым оларды макрожадайды туындататын орналасу дістері кп, сорлым энтропия жоары жне сорлым жйені ішкі энергиясыны ны тмен. Осыдан, энтропия жйені ішкі энергиясыны салыстырмалы ндылыын сипаттайтын фактор болып табылады. Егер реакция барысында энтропия жоарылайтын болса, жйені жалпы энергия оры згермесе де, оны пайдалану жне жмысты орындау ммкіншілігі азаяды.
Энтропияа мынадай факторлар сер етеді:
1. Температура жоарылаанда, энтропия жоарылайды, себебі температура артанда, ретсіздік артады.
2. Заттар кристалданан кйден аморфты кйге немесе сйыа, сйытан газа айналанда, энтропия крт жоарылайды, себебі ретсіздік артады.
3. ысымны жоарылауы энтропияа температураны тмендеуі сияты сер етеді.
Химиялы реакцияны энтропия згерісі энтальпияны згерісі сияты есептеледі:
S = Sт.з. Sб.з.
Гиббс энергиясы. Гельмгольц энергиясы
Химиялы жйелердегі энтальпиялы жне энтропиялы факторларды арасындаы айырма G = Н ТS химиялы процестерді белгілі бір баытта жру абылетін анытауа ммкіндік береді. Егер G < О болса, процесс з бетінше жреді, ал G > О болса, реакцияны жруі ммкін емес.
G = Н – ТS шамасы Гиббс энергиясы деп аталады, брын изобарлы изотермиялы потенциал деп аталан, ал медицинада еркін энергия деп аталады, негізінде траты ысымдаы еркін энергия деп атау керек. Себебі химиялы термодинамикада еркін энергия болып Гельмгольц энергиясы немесе изохорлы изотермиялы потенциал есептеледі:
= U ТS
Бл энергия траты клемде жретін процестерді сипаттайды, оны Гиббс энергиясынан рV млшеріне айырмашылыы бар:
G = + рV
G траты ысымдаы еркін энергия.
траты клемдегі еркін энергия.
Гиббс жне Гельмгольц энергиялары тмендесе, экзэргоникалы, ал олар жоарыласа, эндэргоникалы процестер орындалады.
Траты ысым мен температурада жретін химиялы процестерді еркін энергиясыны згерісі G бастапы заттар мен тзілген німдерді рамына жне кйіне туелді болады, біра процесті жру дісіне байланысты болмайды жне мына тедеу бойынша есептеледі:
G = G т.з. – G б.з.
Термодинамиканы екінші заыны ртрлі анытамалары бар. Бл заны бір тедеуіне G = Н ТS жатады. Сондытан да химиялы термодинамикада олданылатын олайлы анытама былай оылады: траты температура мен ысымда (немесе клемде) Гиббс энергиясы (немесе Гельмгольц энергиясы) теріс мнге ие болатын процестер, яни жйе сырты кштерге арсы жмыс жасай алатын процестер ана з бетінше жруі ммкін.
Кез келген термодинамикалы жйені жмыса абылеті ажетті градиенттерді (температура, ысым, концентрация, электр потенциалы т.б.) болуымен сипатталады. Жйеде термодинамикалы тепе-тедік орнаанда, градиенттер жойылып, жйе жмыс жасауа абылетсіз болады. Осыан байланысты мынадай анытама беруге болады : тйыталан жйені кйін згертетін наты процестер градиенттерді жойылу баытында орындалады.
Тйыталан жйелерде Н = 0. Олай болса, G = – ТS. Мндай жйелерде процестерді з бетінше жруі (G < 0) энтропия жоарылаанда ана орындалады (Ѕ > 0). Сонда ана G < 0. Осыан байланысты тйыталан жйені энтропиясы максимума мтылады.
1.1.5 Термодинамиканы шінші заы
Конденсацияланан жйелерде жретін реакцияларды ртрлі температуралардаы жылу эффектлерін салыстыранда, оларды жылу эффектлері тменгі температуралар аймаындаы абсолютті нольге жаындаанда бір біріне жуытайды.
Осыдан термодинамиканы III заы немесе температураны абсолюттік нольге жуытамау аидасы туындайды. Ол бойынша абсолюттік нольге жаындаанда барлы заттарды жылу сиымдылыы те аз болады. Абсолюттік нольде конденсацияланан жйелердегі рекеттесуші заттарды энтропиялары нольге те болады: Ѕ = 0.
Дрыс тзілген кристалдарды немесе таза кйдегі осылыстарды абсолюттік нольдегі энтропиялары нольге те, ал затты кез келген баса кйіндегі энтропиясы нольден лкен болады. Термодинамиканы бл заы энтропияны абсолюттік мндерін анытау шін кеінен олданылады.
1.2 ХИМИЯЛЫ КИНЕТИКА
Химиялы реакциялар жылдамдыы жне оны р трлі факторлара туелділігін зерттеумен химияны ерекше блімі химиялы кинетика шылданады.
Химиялы реакцияны жылдамдыын кесімді уаыт ішінде (секунд, саат, жыл) рекеттесуші заттарды концентрациясыны згеруімен лшейді.
Концентрация дегеніміз клем бірлігіндегі затты млшері кбінесе 1 литрдей моль саны. Мысалы, реакция басталмас брын затты концентрациясы Со (3 моль), реакция басталанына t(5) минут ткеннен кейін лшегенімізде Сt (2 моль) болсын, сонда реакцияны жылдамдыы:

Химиялы реакцияны жылдамдыына рекеттесуші заттарды табии асиеттерден баса, реакция жруіне туызан жадай да сер етеді. Реакция жадайыны бастылары: рекетесуші заттарды табиаты, ысым, температура, рекеттесуші заттарды концентрациясы жне катализатор.
Осы жадайларды серлеріне туелді химиялы реакцияны жылдамдыыны згеруін, химиялы кинетика блімі зерттейді.
Иллюстрациялы материалдар: презентация
Таблицалар, слайдтар.
дебиеттер:
Негізгі:
1. Сейтембетов Т.С. Химия – Алматы: Эверо, 2010 ж
2. Веренцова . Бейорганикалы коллойдты жне физикалы химия – Алматы: Эверо,
2010 ж
осымшалар:
1. А:Ж: Сарсенбекова Химия: Дріс курсы. Оу-дістемелік рал. араганды 2010ж
2. Ж:М: Тулегенова Л:А:Смакова: Химия пнінен тжірибелік тапсырмаларды
жинаы. Оу - дістемелік. араанды 2011ж
3.Патсаев .. Бейорганикалы жне физколлоидты химия. Алматы,2004.
4.Патсаев .К., Шитыбаев С.А. Бейорганикалы жне физ.коллоидты химияны тжірибелік-зертханалы сабатарына олданба. Шымкент, 2006 .
Баылау сратары (кері байланыс)
1. Тірі организмде ферментті ролі андай?