Визначення температури помутніння розчину неіоногенної ПАР у воді
Мета роботи: визначення точки помутніння неіонних ПАР, вивчення впливу електроліту на температуру помутніння.
Поверхнево-активні речовини – дифільні сполуки, що містять у своєму складі ліпофільний вуглеводневий радикал і гідрофільну функціональну групу. Дифільна будова молекул ПАР визначає їх характерні колоїдні властивості: здатність адсорбуватисяна межі розділу фаз, знижуючи поверхневий (міжфазний) натяг, і асоціювати в рідкійфазіз утворенням міцел різної структури.
У концентрованих розчинах колоїдних ПАР спостерігаються структурні переходи, пов'язані зі зміною форми міцел (сфера > циліндр > ламела) і відповідним утворенням різних мезоморфних фаз (наприклад, гексагональної або ламелярної). Перехід від одного типу структури до іншого здійснюється головним чином при зміні концентрації або температури. Структурні переходи можуть бути викликані введенням електролітів або со-ПАР, що використовується в технології шампунів.
Структурні переходи супроводжуються помітною зміною фізичних (оптичних, гідродинамічних, електричних і т.д.) властивостей системи.
Для іоногеннихПАР характерною колоїдно-хімічною характеристикою є, так звана, точка Крафта. Точкою Крафта (Тк) називають температуру, при якій розчинність сполуки чисельно дорівнює значенню ККМ ПАР (рис. 3.1). Нижче точки Крафта, через низьку розчинність ПАР, утворення міцел неможливо, тоді як при температурі вище Тк відбувається утворення міцелярних структур, термодинамічно більш стійких, ніж гідратоване тверде ПАР. При цьому фактичний вміст (колоїдна розчинність) ПАР в розчині може значно перевищувати його істинну (молекулярну) розчинність.

Рис. 3.1. Фазова діаграма іоногенної ПАР в області точки Крафта
(А – область існування кристалічної гідратованої ПАР; В – область “істинного” розчину ПАР; С – область міцелярного розчину ПАР)
У гомологічному ряду ПАР існує кореляція між значеннями точки Крафта і температурою топлення відповідних вуглеводнів. Так само, як і температура топлення, точка Крафта знижується в присутності різних домішок. Це знаходить застосування при виготовленні твердих і рідких мил.
Для неіонних ПАР (НПАР)спостерігається зниження розчинності при підвищених температурах через дегідратацію оксиетильних груп. При певній температурі, яку називають температурою помутніння (Тп), відбувається розшарування системи на органічну фазу (концентрат ПАР із незначним вмістом води) і водну фазу з низьким вмістом молекулярно розчиненої ПАР. Цей перехід носить оборотний характер, тобто при Т < Тп система знову стає однорідної і прозорою. Температура помутніння залежить від сполуки вуглеводневого радикала і ступеня оксіетилювання ПАР. Як правило, значення Тп зменшується з ростом довжини вуглеводневого ланцюга й/або зменшенням числа оксиетильних груп. При збільшенні числа оксиетильних груп у молекулі НПАР, температура помутніння може бути вище 1000С. У цьому випадку визначення Тп проводять під тиском або в присутності висолюючих домішок (наприклад, неорганічних солей). Екстраполюючи знайдені значення Тп до нормального тиску або нульової концентрації домішки, знаходять температуру помутніння ПАР.
Вплив складу і температури на стан мезоморфних фаз може бути представлений за допомогою фазових діаграм. На рис. 3.2 наведена типова фазова діаграма неіонної ПАР.
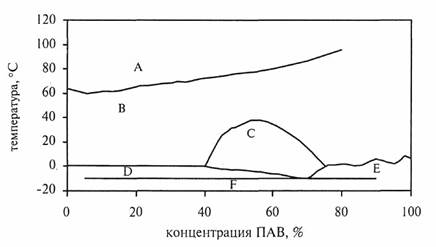
Рис. 3.2. Фазова діаграма оксиетильованої карбонової кислоти
Область В являє собою прозору ізотропну систему, що містить сферичні міцели. В області А співіснують дві фази: органічна (яка містить надлишок ПАР і незначну кількість води) і водна (з невеликою кількістю молекулярно розчиненої ПАР). Області А та В розділяє лінія помутніння. Як видно, температура помутніння (Тп) залежить від концентрації неіонної сполуки. Перехід А ↔ В носить оборотний характер, тобто при температурах нижче Тп система знову стає однорідною і прозорою. Утворення циліндричних міцелярних структур (область С) обумовлює виникнення анізотропної фази. В областях D і F кристали ПАР співіснують із водою або льодом відповідно. При низькому вмісті води (область Е) ПАР перебуває у формі кристалогідратів різного складу.
Знання особливостей фазового поводження ПАР важливо при розробці косметичних композицій. Так, наприклад, в області температури помутніння спостерігається підвищена взаємна розчинність контактуючих рідких фаз, а в емульсійних системах має місце інверсія фаз. Ці явища знаходять застосування при виготовленні рідких косметичних виробів.
Методика роботи. У склянці за чергою готують розчини ПАР з різним вмістом хлориду натрію відповідно до таблиці 3.1.
Таблиця 3.1 – Результати вимірювання Тп
| Номер розчину | ||||
| Об'єм розчину ПАР, мл | ||||
| Об'єм розчину NaCl, мл | ||||
| Об'єм дистильованої води, мл | ||||
| Концентрація хлориду натрію, мас.% | ||||
| Температура помутніння Т1 при підвищенні температури | ||||
| Температура помутніння Т2 при зниженні температури | ||||
| Температура помутніння: Тп = 0,5(Т1+Т2) |
Для визначення температури помутніння досліджуваний розчин заливають у колбу, встановлюють термометр та ставлять на водяну баню. Розчин повільно нагрівають і періодично розглядають на просвіт для виявлення помутніння розчину або розшарування фаз. Записують температуру розчину, при якій він став мутним. Потім колбу виймають із термостата і охолоджують на повітрі, періодично струшуючи, і знову відзначають температуру, при якій розчин став прозорим. Тричі повторюють визначення температури помутніння при підвищенні та зниженні температури розчину. Знайдені значення температур не повинні відрізнятися більш ніж на 3–50С. Визначають температуру помутніння для інших розчинів. Дані заносять у таблицю 3.1.
Проводять аналіз отриманих даних і пояснюють вплив неорганічних солей на температуру помутніння розчинів оксиетильованих ПАР.
Контрольні запитання
1. Які чинники впливають на перехід від одного типу структури ПАР до іншого?
2. Що характеризує точка Крафта?
3. Від чого залежить розчинність неіонних ПАР?
4. Як визначають температуру помутніння?
Лабораторна робота 4