ОСНОВНІ ПОНЯТТЯ ТА ЗАКОНИ ХІМІЇ
КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
1.1 Перелічіть стійкі ступені окислення елементу:
01 – Нітроген; 02 – Магній; 03 – Натрій; 04 – Хлор; 05 – Сульфур; 06 – Титан; 07 –Карбон; 08 – Цинк; 09 – Купрум; 10 – Манган; 11 – Хром; 12 – Бром; 13 – Кальцій; 14 – Алюміній; 15 – Калій; 16 – Аргентум; 17 – Барій; 18 – Силіцій; 19 – Кадмій; 20 – Літій; 21 – Нікол;
22 - Гідроген; 23 – Літій; 24 – Станум; 25 – Фосфор; 26 – Стибій; 27 – Бор; 28 – Ферум;
29 - Меркурій ; 30 – Іод.

1.2. Складіть емпіричні та графічні формули можливих оксидів елементу, вказаного у розділі 1.1, і назвіть ці оксиди.
1.3. Визначте тип оксидів (солетворний, несолетворний, основний, кислотний або амфотерний), вказаних у розділі 1.2.
1.4. Напишіть рівняння реакцій солеутворення, що доводять характер оксидів (основний, кислотний або амфотерний), визначений у розділі 1.3.
1.5. Напишіть емпіричні, графічні формули та назву гідроксидів оксидів, складених за розділом 1.2.
1.6. Дайте назву сполук за міжнародною номенклатурою:
01- 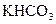 ; 02-
; 02-  ; 03-
; 03-  ; 04-
; 04-  ; 05 -
; 05 -  ; 06 -
; 06 -  ; 07 -
; 07 -  ; 08 -
; 08 -  ; 09 -
; 09 -  ; 10 -
; 10 -  ; 11 -
; 11 -  ; 12 -
; 12 -  ; 13 -
; 13 -  ; 14 -
; 14 -  ; 15 -
; 15 -  ; 16 -
; 16 -  ; 17 -
; 17 -  ; 18 -
; 18 -  ; 19 -
; 19 -  ; 20 -
; 20 -  ; 21 -
; 21 -  ; 22 -
; 22 -  ; 23 -
; 23 -  ; 24 -
; 24 -  ; 25 -
; 25 -  ; 26 -
; 26 -  ; 27 -
; 27 -  ; 28 -
; 28 -  ; 29 -
; 29 -  ; 30 -
; 30 -  .
.
1.7. Визначте ступінь окислення елементів, утворюючих сполуки, зазначені у розділі 1.6.
1.8. Напишіть емпіричну та графічну формули кислоти:
01 – борної; 02 – карбонатної; 03 – нітритної; 04 – фосфатної; 05 – сульфатної; 06 – нітратної; 07 – сульфідної; 08 – оцтової; 09 – силікатної; 10 – сульфітної; 11 – хлоридної; 12 – нітратної; 13 – фосфатної; 14 – силікатної; 15 – карбонатної; 16 – бромводневої; 17 – фтороводневої; 18 – хромової; 19 – борної; 20 – манганової; 21 – сульфатної; 22 – фосфатної; 23 – бромоводневої; 24 – сульфітної; 25 – нітритної; 26 – йодоводневої; 27 – хромової; 28 – нітратної; 29 – оцтової; 30 – манганової.
1.9. Напишіть емпіричну та графічну формули основи:
01 – нікол (ІІІ) гідроксид; 02 – кальцій гідроксид; 03 – ферум (ІІІ) гідроксид; 04 – стронцій гідроксид; 05 – натрій гідроксид; 06 – ферум (ІІ) гідроксид; 07 – бісмут (ІІІ) гідроксид; 08 – купрум (І) гідроксид; 09 – нікол (ІІІ) гідроксид; 10 – кобальт (ІІІ) гідроксид; 11 – калій гідроксид; 12 – цезій гідроксид; 13 – барій гідроксид; 14 – кадмій гідроксид; 15 – магній гідроксид; 16 – манган (ІІ) гідроксид; 17 – францій гідроксид; 18 – купрум (ІІ) гідроксид; 19 – бісмут (ІІІ) гідроксид; 20 – нікол (ІІІ) гідроксид; 21- меркурій (ІІ) гідроксид; 22 – літій гідроксид; 23 – барій гідроксид; 24 – радій гідроксид; 25 – цирконій (ІІІ) гідроксид; 26 – купрум (ІІ) гідроксид; 27 – хром (ІІ) гідроксид; 28 – ітрій (ІІІ) гідроксид; 29 – рубідій гідроксид; 30 – талій (ІІІ) гідроксид.
1.10. Напишіть емпіричну та графічну формули солі:
01 – літій нітрат; 02 – кальцій карбонат; 03 – калій сульфат; 04 – натрій нітрат; 05 – цинк сульфіт; 06 – літій хлорид; 07 – натрій силікат; 08 – берилій фторид; 09 – барій сульфід;
10 – натрій дихромат; 11 – магній гідрогенсульфід; 12 – кальцій дигідрогенфосфат; 13 – ферум (ІІІ) гідрогенсульфат; 14 – алюміній гідроксосульфат; 15 – хром (ІІІ) дигідроксонітрат; 16 – калій цинкат; 17 – алюміній дигідрогенфосфат; 18 – стронцій дихромат; 19 – алюміній дигідроксосульфат; 20 - калій гідрогенкарбонат; 21 - ферум (ІІІ) гідроксохлорид; 22 - кальцій гідрогенфосфат; 23 – алюміній дигідроксохлорид; 24 - натрій гідрогенфосфат; 25 – кадмій карбонат; 26 - стронцій гідрогенсульфат; 27 - меркурій (ІІ) нітрат; 28 – барій хлорид; 29 – станум (ІІ) сульфат; 30 - аргентум хромат.
ОСНОВНІ ПОНЯТТЯ ТА ЗАКОНИ ХІМІЇ
2.1. Атомна маса, молекулярна маса, моль, мольна маса .
2.1.1. Визначте масу в г та в а.о.м. атома елемента:
01 – Титану; 02 –Карбону; 03 – Цинку; 04 – Купруму; 05 – Мангану; 06 – Хрому; 07 – Брому; 08 – Кальцію; 09 – Алюмінію; 10 – Калію; 11 – Аргентуму; 12 – Барію; 13 – Силіцію; 14 – Літію; 15 – Ніколу; 16 – Меркурію ; 17 – Іоду; 18 - Гідрогену; 19 – Літію; 20 – Стануму; 21 – Фосфору; 22 – Стибію; 23 – Бору; 24 – Феруму; 25 – Нітрогену; 26 – Магнію; 27 – Натрію; 28 – Хлору; 29 – Сульфуру; 30 – Кадмію.
2.1.2. . Визначте масу в г та в а.о.м. молекули речовини:
01 – карбонатної кислоти; 02 – сульфатної кислоти; 03 – нітритної кислоти; 04 – амоній гідроксиду; 05 – цинк гідроксиду; 06 – калій сульфату; 07 – літій сульфат; 08 – нітратної кислоти; 09 – барій сульфіду; 10 – кальцій гідрогенсульфату; 11 – алюміній гідрогенсульфату; 12 – натрій гідрогенкарбонату; 13 – аргентум гідроксиду; 14 – сульфітної кислоти; 15 – сірководневої кислоти; 16 – барій гідроксиду; 17 – купрум (ІІ) гідроксиду; 18 – натрій силікату; 19 – магній гідрогенсульфіду; 20 – аргентум хромату;
21 – натрій хлориду; 22 – кальцій нітрату; 23 – калій сульфіту; 24 – ферум (ІІІ) гідрогенсульфату; 25 – амоній нітриту; 26 – алюміній фосфату; 27 – хром (ІІІ) дигідроксохлориду; 28 – натрій хромату; 29 – алюміній сульфату; 30 – кальцій карбонату.
2.1.3. Обчисліть, скільки атомів вміщується в :
01 – 15 г титану; 02 – 0,3 г вуглецю; 03 – 17 г цинку; 04 – 24 г міді; 05 – 0,01 г мангану; 06 – 7 г хрому; 07 – 5 г брому; 08 – 10 г кальцію; 09 – 50 г алюмінію; 10 – 15 г калію;
11 – 24 г срібла; 12 – 22 г барію; 13 – 16 г силіцію; 14 – 0,9 г літію; 15 – 27 г нікелю;
16 – 41,2 г ртуті ; 17 – 12,7 г іоду; 18 – 25,7 г водню; 19 – 24,3 г літію; 20 – 16,8 г олова; 21 – 35,1 г фосфору; 22 – 33,5 г стибію; 23 – 20,6 г бору; 24 – 33,9 г заліза; 25 – 36,8 г азоту; 26 – 43,6 г магнію; 27 – 0,66 г натрію; 28 – 1,23 г хлору; 29 – 2,27 г сірки; 30 – 23,2 г кадмію.
2.1.4. Обчисліть, скільки молекул вміщується в :
01 – 100 г кальцій карбонату; 02 – 54 г хром (ІІІ) дигідроксохлориду; 03 – 22 г натрій хромату; 04 – 82 г алюміній сульфату; 05 – 4,8 г ферум (ІІІ) гідрогенсульфату; 06 – 30 г амоній нітриту; 07 – 58 г алюміній фосфату; 08 – 0,64 г натрій хлориду; 09 – 53 г кальцій нітрату; 10 – 21 г калій сульфіту; 11 – 87 г аргентум хромату; 12 – 5,21 г купрум (ІІ) дигідроксиду; 13 – 15,8 г натрій силікату; 14 – 5,4 г магній гідрогенсульфіду; 15 – 73 г сульфітної кислоти; 16 – 10,2 г сірководневої кислоти; 17 – 16,7 г барій гідроксиду; 18 – 22,5 г алюміній гідрогенсульфату; 19 – 36,2 г натрій гідрогенкарбонату; 20 – 42,8 г аргентум гідроксиду; 21 – 51,3 г нітратної кислоти; 22 – 66,3 г барій сульфіду; 23 – 72,2 г кальцій гідрогенсульфату; 24 –23,6 г амоній гідроксиду; 25 – 44,6 г цинк гідроксиду; 26 – 85,3 г калій сульфату; 27 – 44,9 г літій гидроксиду; 28 – 1,3 г карбонатної кислоти; 29 – 0,66 г сульфатної кислоти; 30 – 36,8 г нітритної кислоти;
2.1.5. Скільки молей складає кількість речовини, вказаної у розділі 2.1.4.
2.1.6. . Визначте масу в г :
01 – 2 молей натрій хромату; 02 – 0,3 моля алюміній сульфату; 03 – 3,4 моля кальцій карбонату; 04 – 6,3 моля алюміній фосфату; 05 – 5,1 моля хром (ІІІ) дигідроксохлориду;
06 – 3 молей калій сульфіту; 07 – 2,5 моля ферум (ІІІ) гідросульфату; 08 – 3,2 моля амоній нітриту; 09 – 6 молей натрій хлориду; 10 – 2,8 моля кальцій нітрату; 11 – 10 молей аргентум хромату; 12 – 7,3 моля купрум (ІІ) гідроксиду; 13 – 0,43 моля натрій силікату; 14 – 3,8 моля магній гідрогенсульфіду; 15 – 11,5 моля сульфітної кислоти; 16 – 6,22 моля сірководневої кислоти; 17 – 0,7 моля барій гідроксиду; 18 – 3 молей алюміній гідрогенсульфату; 19 – 1,4 моля натрій гідрогенкарбонату; 20 – 22 молей аргентум гідроксиду; 21 – 1,8 моля нітратної кислоти; 22 – 2,27 моля барій сульфіду; 23 – 1,3 моля кальцій гідрогенсульфату; 24 – 2,9 моля амоній гідроксиду; 25 –0,22 моля цинк гідроксиду; 26 – 112 молей калій сульфату; 27 – 44 молей літій сульфату; 28 – 39 молей карбонатної кислоти; 29 – 0,88 моля сульфатної кислоти; 30 – 5 молей нітритної кислоти;