Как пример самопроизвольно возникающих нанодисперсий
Д.х.н., проф. Л.Н. Мизеровский; П.Р. Смирнов
Институт химии растворов им. Г.А. Крестова Российской академии наук
Доклад посвящён термодинамическому анализу систем инертный
газ – жидкость при изохорно-изотермических условиях. Анализ основан на следующих положениях.
1. Согласно [1], растворимость инертных газов в жидкостях (в молях на моль жидкости) описывается уравнением
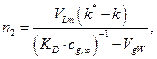
| (1) |
где VLm - мольный объём жидкости, м3·моль-1; k - коэффициент её молекулярной упаковки, рассчитываемый по методу [2]; k* - предельное значение этого параметра, отвечающее условию n2 = 0; cg,∞ - равновесная концентрация газа в собственной фазе, моль·м-3; а KD – константа распределения частиц газа между этой фазой и доступным для их диффузионных перемещений объёмом межмолекулярного пространства жидкости, VL,f*, определяемого из соотношения
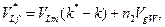
| (2) |
где VgW - ван-дер-ваальсов объём моля частиц газа.
2. Мольная энергия Гиббса газа (Gg) при температуре Т и концентрации газа, равной cg, подчиняется уравнению
| Gg = Gg0 ± kh (cg – 1) + T ks ln cg, | (3) |
где Gg0 – стандартная (при концентрации газа 1 моль·м-3) мольная энергия Гиббса газа при температуре Т, а kh и ks – эмпирические константы.
3. Реальный процесс переноса частиц газа в объём жидкости аппроксимируется гипотетическим процессом, состоящим из двух стадий: переноса некоторого количества молей газа из собственной фазы в физический микрообъём, численно равный Vl,,f*, и распределения этих частиц газа по отдельным полостям последнего.
Проверка модели проведена на примере данных по растворимости благородных газов и азота в н-декане при 280 – 300 K.
В результате установлено:
• возникающие при контакте инертных газов с жидкостями двухфазные бикомпонентные системы термодинамически неустойчивы;
• возрастание энергии Гиббса этих систем связано с переходом жидкой компоненты в объёмно-напряжённое состояние в результате образования в ней второй (газовой) фазы;
• жидкость, насыщенную инертным газом, можно считать дисперсией газовых кластеров, самопроизвольно сформировавшихся в полостях её межмолекулярного пространства;
• энергетические затраты на образование полостей для газовых кластеров компенсируются извне – за счет поддержания в системе постоянной температуры.