Основные элементы диаграммы
Цели и задачи
Целью данной работы является:
1. Изучение методики построения диаграмм по фигуративным точкам;
2. Решение практических задач по диаграммам равновесия двух компонентным системам.
К основным задачам отчета относятся:
1. Повторения основных элементов диаграммы.
2. Изучения видов диаграмм двух компонентных систем.
3. Объяснения принципа правила рычага для двух компонентных систем.
4. Научиться определять:
¾ какие фазы находятся в равновесии;
¾ состав равновесных фаз;
¾ количественное соотношение фаз.
Раздел 1. Теоретическая часть
Основные элементы диаграммы
Диаграмма состоит из вертикальной оси – ось температуры, горизонтальной оси – ось концентрации компонентов.
Внешний вид диаграммы приведен на рисунке 1. Левый конец горизонтальной оси концентраций компонентов, обозначенный буквой А, соответствует 100% содержанию компонента А, правый – 100% содержанию компонента В.
Та и Тв – соответственно температуры плавления чистых компонентов А и В. Если точка состава находится на одной из вертикальных осей диаграммы (на А или В), то в этом случае мы рассматривает процессы, происходящие в однокомпонентной системе.
Кривые Та – Е и Е – Тв носят название кривых ликвидуса. Кривые ликвидуса представляют собой температурные зависимости перенасыщения расплава по отношению к какому-либо компоненту или химическому соединению. Кривая Та – Е показывает температуру начала кристаллизации в системе компонента А из расплава при его охлаждении, кривая Е – Тв – соответственно начала кристаллизации компонента В.
Точка Е носит название точки эвтектики и характеризует состав расплава с минимальной для данной системы температурой существования жидкой фазы, расплав эвтектического состава. Этот расплав пересыщен одновременно по отношению к обоим компонентам А и В. При кристаллизации расплава эвтектического состава компоненты выделяются в твердой фазе всегда в строго определенном соотношении, определяемом положением точки эвтектики.
Горизонтальная линия, проведенная при температуре Т2 от линии ликвидуса до вертикали выпадающей твердой фазы, носит название конноды.
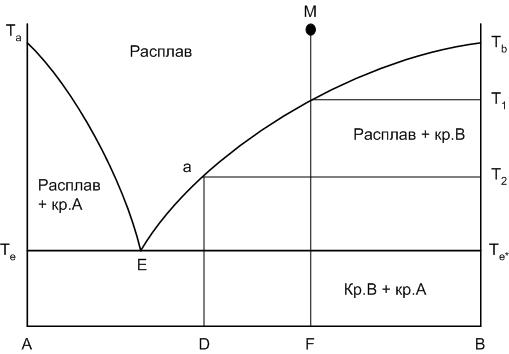
Рисунок 1. Диаграмма двухкомпонентной системы
Линия Те – Е – Те* носит название линии солидуса. Это линия окончания кристаллизации или начала плавления любого бинарного состава системы. Ниже линии солидуса в равновесии могут находиться только фазы в твердом состоянии. Следует также отметить, что линия солидуса не всегда горизонтальна.
Точка состава расплава, образующаяся при плавлении химических элементов называется перитектикой (на рисунке 1 она изображена в виде точки а).
Основными элементами кривых охлаждения являются точка перегиба и горизонтальная площадка.
Точка перегиба кривой охлаждения при постоянной скорости охлаждения появляется в том случае, когда изменяется скорость охлаждения. А это, в свою очередь, связано с началом протекания в системе процессов, сопровождающихся тепловыми эффектами, имеющих, как правило, экзотермический характер при охлаждении системы. Дополнительное выделение тепла снижает скорость охлаждения системы и угол наклона (между кривой охлаждения и абсциссой графика) увеличивается.
Для бинарных систем изменение угла наклона кривой охлаждения связано прежде всего с началом кристаллизации одной кристаллической фазы: компонента или химического соединения.